DOI: https://doi.org/10.3847/2041-8213/adc911
PMID: https://pubmed.ncbi.nlm.nih.gov/41103619
تاريخ النشر: 2025-04-30
اكتشاف الهيدروكربون العطري متعدد الحلقات ذو السبعة حلقات سيانكورونين (C 24 H 11 CN) في ملاحظات GOTHAM لـ TMC-1
الملخص
نقدم تخليق وطيف الدوران المختبري للهيدروكربونات العطرية متعددة الحلقات ذات السبع حلقات
1. المقدمة
تمت مناقشة الأشرطة بين النجوم المنتشرة (DIBs). تم اقتراح الكورونين المنزوع الهيدروجين، والمُؤيّن، والمُؤيّن كحاملين محتملين للأشرطة (Pathak & Sarre 2008؛ Malloci et al. 2008)، لكن هذه الفرضيات تم دحضها (Garkusha et al. 2011؛ Useli-Bacchitta et al. 2010؛ Hardy et al. 2017). ومع ذلك، لا تزال بعض توزيعات PAHs مرشحة واعدة كحاملين للأشرطة بسبب علاقتها الوثيقة بعائلة الفوليرين (Campbell et al. 2015).
2. التركيب
3. الطيفية المخبرية
| معامل | B3LYP aug-cc-pVTZ | تجريبي
|
|
|
335.393 | ٣٣٣.٨٥٢٩٨٩(٢٤٩) |
|
|
٢٢٢٫٠٣٥ | 221.2700880(838) |
|
|
١٣٣٫٥٩٤ | ١٣٣.١٠٨١٠١٥(١٢٢) |
|
|
0.669 | [0.669] |
|
|
-0.617 | [-0.617] |
|
|
0.011 | [0.011] |
|
|
-0.120 | [-0.120] |
|
|
-0.494 | [-0.494] |
|
|
71 | |
|
|
٣٨ | |
|
|
٢.٥٩٥ | |
|
|
|
|
ثوابت دورانية،
4. الملاحظات
5. التحليل الفلكي
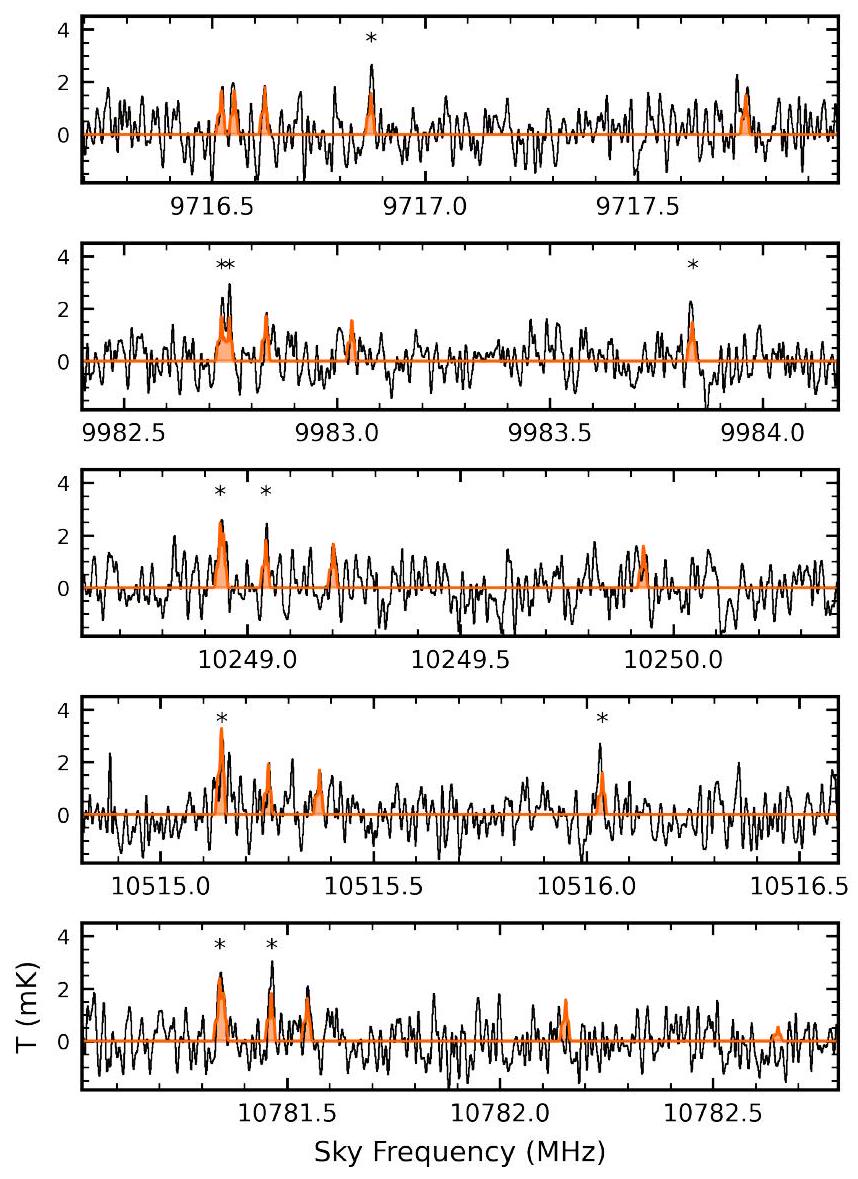
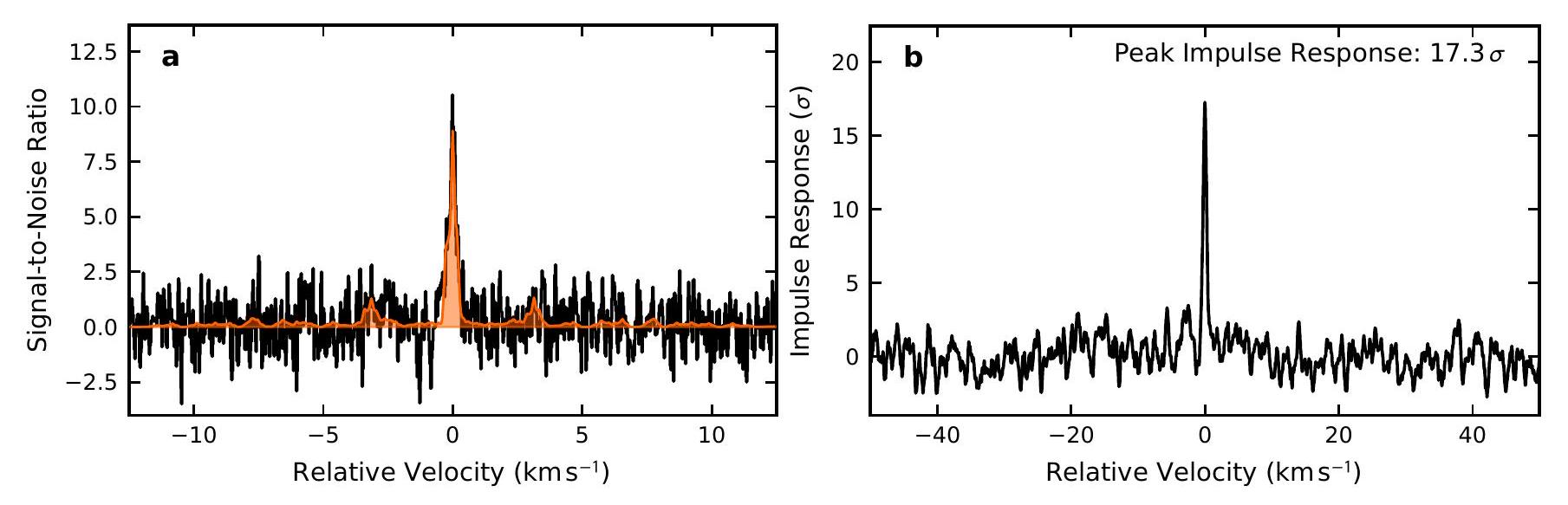
6. المناقشة
مسار تشكيل الطور لبايرين، بدءًا من الجذري 4-فينانثرينيل. في الواقع، الفينانثرين هو أيضًا عضو في أكثر مسارات بوليمرة PAH استقرارًا من الناحية الديناميكية الحرارية (انظر الشكل 5). ومع ذلك، لم تكن عمليات البحث السريعة عن مشتقه CN- 9-سيانوفيتانثرين، الذي يُعرف طيفه الدوراني (ماكنوتون وآخرون 2018)، ناجحة حتى الآن في ملاحظاتنا باستخدام GOTHAM. قد يكون ذلك بسبب أن الطيفية لواحد فقط من خمسة سيانوفيتانثرين المحتملة…

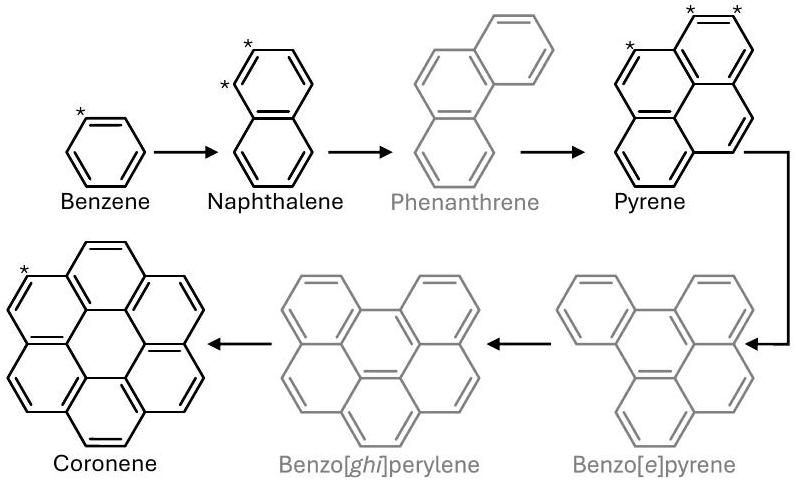
ويدل بول وآخرون (2025) على أن الهيكل الأساسي لمركبات PAH يمكن الحفاظ عليه من خلال التبريد الإشعاعي الفعال، مما يفتح إمكانية نوع من “إعادة التدوير” الكيميائي لمركبات PAH التي ستساهم بالتأكيد في الوفرة العالية الملحوظة، على سبيل المثال، السيانكورونين. عند الانتقال إلى النقص في الحبوب، أجرى دارتوا وآخرون (2022) تجارب على إنتاجية التبخير لمركب بيرلين الصلب والكورونين الذي تعرض لقصف من أيونات نشطة، وهو ما يشبه تعرض الأنواع لأشعة كونية في غلاف الثلج لحبوب الغبار. وقد وجدوا أن هذا التبخير الناتج عن الأشعة الكونية فعال تحت ظروف الوسط بين النجوم، ويتوقعون حتى وفرة جزئية في الطور الغازي للكورونين.
7. الاستنتاجات
8. الوصول إلى البيانات والرمز
المرافق: GBT
الشكر والتقدير
جائزة بيكمان للشباب الباحثين. يود ز.ت.ب.ف. و ب.أ.م. أن يعربا عن امتنانهما لدعم عائلة شميت. يقر إ.ر.س. بالدعم المقدم من جامعة كولومبيا البريطانية ومجلس أبحاث العلوم الطبيعية والهندسة في كندا (NSERC). يقر إ.ر.س. و ت.هـ.س. بالدعم المقدم من وكالة الفضاء الكندية (CSA) من خلال منحة 24AO3UBC14. يتلقى ب.ج.س. الدعم من NIST. المرصد الوطني للراديو الفلكي هو منشأة تابعة لمؤسسة العلوم الوطنية وتديرها اتفاقية تعاونية مع الجامعات المرتبطة، إنك. المرصد في غرين بانك هو منشأة تابعة لمؤسسة العلوم الوطنية وتديرها اتفاقية تعاونية مع الجامعات المرتبطة، إنك.
REFERENCES
Baer, T., & Hase, W. L. 1996, Unimolecular Reaction Dynamics: Theory and Experiments (Oxford University Press). https://academic.oup.com/book/40815
Bahou, M., Wu, Y.-J., & Lee, Y.-P. 2014, Angewandte Chemie, 126, 1039, doi: 10.1002/ange. 201308971
Bakes, E. L. O., & Tielens, A. G. G. M. 1998, The Astrophysical Journal, 499, 258, doi: 10.1086/305625
Balle, T. J., & Flygare, W. H. 1981, Review of Scientific Instruments, 52, 33, doi: 10.1063/1.1136443
Balucani, N., Asvany, O., Huang, L. C. L., et al. 2000, The Astrophysical Journal, 545, 892, doi: 10.1086/317848
Bauschlicher, C. W. 1998, The Astrophysical Journal, 509, L125, doi: 10.1086/311782
Becke, A. D. 1988, Physical Review A, 38, 3098, doi: 10.1103/PhysRevA.38.3098
-. 1993, The Journal of Chemical Physics, 98, 5648, doi: 10.1063/1.464913
Becke, A. D., & Johnson, E. R. 2006, The Journal of Chemical Physics, 124, 221101, doi: 10.1063/1.2213970
Bernstein, M. P., Elsila, J. E., Dworkin, J. P., et al. 2002, The Astrophysical Journal, 576, 1115, doi: 10.1086/341863
Berné, O., Foschino, S., Jalabert, F., & Joblin, C. 2022, Astronomy & Astrophysics, 667, A159, doi: 10.1051/0004-6361/202243171
Boschman, L., Cazaux, S., Spaans, M., Hoekstra, R., & Schlathölter, T. 2015, Astronomy & Astrophysics, 579, A72, doi: 10.1051/0004-6361/201323165
Burkhardt, A. M., Long Kelvin Lee, K., Bryan Changala, P., et al. 2021, The Astrophysical Journal Letters, 913, L18, doi: 10.3847/2041-8213/abfd3a
Caldeweyher, E., Bannwarth, C., & Grimme, S. 2017, The Journal of Chemical Physics, 147, 034112, doi: 10.1063/1.4993215
Campbell, E. K., Holz, M., Gerlich, D., & Maier, J. P. 2015, Nature, 523, 322, doi: 10.1038/nature14566
Carelli, F., & Gianturco, F. A. 2012, Monthly Notices of the Royal Astronomical Society, 422, 3643, doi: 10.1111/j.1365-2966.2012.20876.x
Cazaux, S., Boschman, L., Rougeau, N., et al. 2016, Scientific Reports, 6, 19835, doi: 10.1038/srep19835
Cernicharo, J., Agúndez, M., Cabezas, C., et al. 2021a, Astronomy and Astrophysics, 649, L15, doi: 10.1051/0004-6361/202141156
Cernicharo, J., Agúndez, M., Kaiser, R. I., et al. 2021b, Astronomy & Astrophysics, 652, L9, doi: 10.1051/0004-6361/202141660
—. 2021c, Astronomy & Astrophysics, 655, L1, doi: 10.1051/0004-6361/202142226
Cernicharo, J., Fuentetaja, R., Agúndez, M., et al. 2022, Astronomy & Astrophysics, 663, L9, doi: 10.1051/0004-6361/202244399
Cernicharo, J., Cabezas, C., Fuentetaja, R., et al. 2024, Astronomy & Astrophysics, 690, L13, doi: 10.1051/0004-6361/202452196
Chai, J.-D., & Head-Gordon, M. 2008, The Journal of Chemical Physics, 128, 084106, doi: 10.1063/1.2834918
Chen, T., Luo, Y., & Li, A. 2020, Astronomy & Astrophysics, 633, A103, doi: 10.1051/0004-6361/201936873
Clar, E. 1964, Polycyclic Hydrocarbons (Berlin, Heidelberg: Springer Berlin Heidelberg), doi: 10.1007/978-3-662-01668-8
-. 1983, in Mobile Source Emissions Including Policyclic Organic Species, ed. D. Rondia, M. Cooke, & R. K. Haroz (Dordrecht: Springer Netherlands), 49-58, doi: 10.1007/978-94-009-7197-4_4
Cooke, I. R., Gupta, D., Messinger, J. P., & Sims, I. R. 2020, The Astrophysical Journal Letters, 891, L41, doi: 10.3847/2041-8213/ab7a9c
Crabtree, K. N., Martin-Drumel, M.-A., Brown, G. G., et al. 2016, The Journal of Chemical Physics, 144, 124201, doi: 10.1063/1.4944072
Dale, T. J., & Rebek, J. 2006, Journal of the American Chemical Society, 128, 4500, doi: 10.1021/ja057449i
Dartois, E., Chabot, M., Koch, F., et al. 2022, A&A, 663, A25, doi: 10.1051/0004-6361/202243274
Davidson, E. R. 1996, Chemical Physics Letters, 260, 514, doi: 10.1016/0009-2614(96)00917-7
Davies, J. W., Green, N. J. B., & Pilling, M. J. 1986, Chemical Physics Letters, 126, 373, doi: 10.1016/S0009-2614(86)80101-4
Dopfer, O. 2011, EAS Publications Series, 46, 103, doi: 10.1051/eas/1146010
Dunning, Jr., T. H. 1989, The Journal of Chemical Physics, 90, 1007, doi: 10.1063/1.456153
Dwek, E., Arendt, R. G., Fixsen, D. J., et al. 1997, The Astrophysical Journal, 475, 565, doi: 10.1086/303568
Frisch, M. J., Trucks, G. W., Schlegel, H. B., et al. 2016, Gaussian~16 revision C. 01
Garkusha, I., Fulara, J., Sarre, P. J., & Maier, J. P. 2011, The Journal of Physical Chemistry A, 115, 10972, doi: 10.1021/jp206188a
Gatchell, M., Ameixa, J., Ji, M., et al. 2021, Nature Communications, 12, 6646, doi: 10.1038/s41467-021-26899-0
Georgievskii, Y., & Klippenstein, S. J. 2005, The Journal of Chemical Physics, 122, 194103, doi: 10.1063/1.1899603
Glowacki, D. R., Liang, C.-H., Morley, C., Pilling, M. J., & Robertson, S. H. 2012, The Journal of Physical Chemistry A, 116, 9545, doi: 10.1021/jp3051033
Grimme, S., Ehrlich, S., & Goerigk, L. 2011, Journal of Computational Chemistry, 32, 1456, doi: 10.1002/jcc. 21759
Habart, E., Natta, A., & Krügel, E. 2004, Astronomy and Astrophysics, 427, 179, doi: 10.1051/0004-6361:20035916
Hardy, F.-X., Rice, C. A., & Maier, J. P. 2017, The Astrophysical Journal, 836, 37, doi: 10.3847/1538-4357/836/1/37
Hill, G. 2016, ccRepo. http: //www.grant-hill.group.shef.ac.uk/ccrepo/index.html
Holbrook, K. A., Pilling, M. J., Robertson, S. H., & Robinson, P. J. 1996, Unimolecular reactions, Wiley
Hudgins, D. M., & Allamandola, L. J. 1995, The Journal of Physical Chemistry, 99, 3033, doi: 10.1021/j100010a011
Hyodo, K., Togashi, K., Oishi, N., Hasegawa, G., & Uchida, K. 2017, Organic Letters, 19, 3005, doi: 10.1021/acs.orglett.7b01263
Ishida, K., Morokuma, K., & Komornicki, A. 1977, The Journal of Chemical Physics, 66, 2153, doi: 10.1063/1.434152
Joblin, C., Boissel, P., Léger, A., D’Hendecourt, L., & Defourneau, D. 1995, Astronomy & Astrophysics, 299, 835. http://adsabs.harvard.edu/abs/1995A%26A…299..835J
Joblin, C., Wenzel, G., Castillo, S. R., et al. 2020, Journal of Physics: Conference Series, 1412, 062002, doi: 10.1088/1742-6596/1412/6/062002
Johnson, R. I. 2022, NIST computational chemistry comparison and benchmark database. http://cccbdb.nist.gov/
Jurečka, P., Šponer, J., Černý, J., & Hobza, P. 2006, Physical Chemistry Chemical Physics, 8, 1985, doi: 10.1039/B600027D
Kendall, R. A., Dunning, Jr., T. H., & Harrison, R. J. 1992, The Journal of Chemical Physics, 96, 6796, doi: 10.1063/1.462569
Kesharwani, M. K., Brauer, B., & Martin, J. M. L. 2015, The Journal of Physical Chemistry A, 119, 1701, doi: 10.1021/jp508422u
Le Page, V., Snow, T. P., & Bierbaum, V. M. 2009, The Astrophysical Journal, 704, 274, doi: 10.1088/0004-637X/704/1/274
Lee, C., Yang, W., & Parr, R. G. 1988, Physical Review B, 37, 785, doi: 10.1103/PhysRevB.37.785
Lee, K. L. K., Changala, P. B., Loomis, R. A., et al. 2021, The Astrophysical Journal Letters, 910, L2, doi: 10.3847/2041-8213/abe764
Liakos, D. G., & Neese, F. 2012, The Journal of Physical Chemistry A, 116, 4801, doi: 10.1021/jp302096v
Linstrom, P., & Mallard, W. 2024, NIST chemistry WebBook, NIST standard reference database number 69. https://doi.org/10.18434/T4D303
Loomis, R. A., Burkhardt, A. M., Shingledecker, C. N., et al. 2021, Nature Astronomy, 5, 188, doi: 10.1038/s41550-020-01261-4
Loru, D., Cabezas, C., Cernicharo, J., Schnell, M., & Steber, A. L. 2023, Astronomy & Astrophysics, 677, A166, doi: 10.1051/0004-6361/202347023
Lourderaj, U., & Hase, W. L. 2009, The Journal of Physical Chemistry A, 113, 2236, doi: 10.1021/jp806659f
Léger, A., & Puget, J. L. 1984, Astronomy & Astrophysics, 500, 279. https: //ui.adsabs.harvard.edu/1984A&A…137L…5L/abstract
Malloci, G., Mulas, G., Cecchi-Pestellini, C., & Joblin, C. 2008, Astronomy & Astrophysics, 489, 1183, doi: 10.1051/0004-6361:200810177
McCarthy, M. C., Lee, K. L. K., Loomis, R. A., et al. 2021, Nature Astronomy, 5, 176, doi: 10.1038/s41550-020-01213-y
McGuire, B. A., Xue, C., Lee, K. L. K., El-Abd, S., & Loomis, R. A. 2024, molsim, v0.5.0, Zenodo, doi: 10.5281/zenodo. 12697227
McGuire, B. A., Burkhardt, A. M., Loomis, R. A., et al. 2020, The Astrophysical Journal, 900, L10, doi: 10.3847/2041-8213/aba632
McGuire, B. A., Loomis, R. A., Burkhardt, A. M., et al. 2021, Science, 371, 1265, doi: 10.1126/science.abb7535
McNaughton, D., Jahn, M. K., Travers, M. J., et al. 2018, Monthly Notices of the Royal Astronomical Society, 476, 5268, doi: 10.1093/mnras/sty557
Mennella, V., Hornekær, L., Thrower, J., & Accolla, M. 2012, The Astrophysical Journal Letters, 745, L2, doi: 10.1088/2041-8205/745/1/L2
Miller, W. H. 1979, Journal of the American Chemical Society, 101, 6810, doi: 10.1021/ja00517a004
Neeman, E. M., Lesarri, A., & Bermúdez, C. 2025, ChemPhysChem, in press, e202401012, doi: 10.1002/cphc. 202401012
Neese, F. 2022, WIREs Computational Molecular Science, 12, e1606, doi: 10.1002/wcms. 1606
Oomens, J., Sartakov, B. G., Tielens, A. G. G. M., Meijer, G., & Helden, G. v. 2001, The Astrophysical Journal, 560, L99, doi: 10.1086/324170
Pathak, A., & Sarre, P. J. 2008, Monthly Notices of the Royal Astronomical Society: Letters, 391, L10, doi: 10.1111/j.1745-3933.2008.00544.x
Perdew, J. P. 1986, Physical Review B, 33, 8822, doi: 10.1103/PhysRevB. 33.8822
Pickett, H. M. 1991, Journal of Molecular Spectroscopy, 148, 371, doi: 10.1016/0022-2852(91)90393-O
Pinski, P., Riplinger, C., Valeev, E. F., & Neese, F. 2015, The Journal of Chemical Physics, 143, 034108, doi: 10.1063/1.4926879
Rauls, E., & Hornekær, L. 2008, The Astrophysical Journal, 679, 531, doi: 10.1086/587614
Reizer, E., Viskolcz, B., & Fiser, B. 2022, Chemosphere, 291, 132793, doi: 10.1016/j.chemosphere.2021.132793
Riplinger, C., Pinski, P., Becker, U., Valeev, E. F., & Neese, F. 2016, The Journal of Chemical Physics, 144, 024109, doi: 10.1063/1.4939030
Sabbah, H., Bonnamy, A., Papanastasiou, D., et al. 2017, The Astrophysical Journal, 843, 34, doi: 10.3847/1538-4357/aa73dd
Sabbah, H., Quitté, G., Demyk, K., & Joblin, C. 2024, Natural Sciences, 4, e20240010, doi: 10.1002/ntls. 20240010
Sephton, M. A., Love, G. D., Watson, J. S., et al. 2004, Geochimica et Cosmochimica Acta, 68, 1385, doi: 10.1016/j.gca.2003.08.019
Siebert, M. A., Lee, K. L. K., Remijan, A. J., et al. 2022, The Astrophysical Journal, 924, 21, doi: 10.3847/1538-4357/ac3238
Sita, M. L., Changala, P. B., Xue, C., et al. 2022, The Astrophysical Journal, 938, L12, doi: 10.3847/2041-8213/ac92f4
Stein, S. 1978, The Journal of Physical Chemistry, 82, 566, doi: 10.1021/j100494a600
Stockett, M. H., Subramani, A., Liu, C., et al. 2025, Dissociation and radiative stabilization of the indene cation: The nature of the C-H bond and astrochemical implications. https://arxiv.org/abs/2503.20686
Thrower, J. D., Jørgensen, B., Friis, E. E., et al. 2012, The Astrophysical Journal, 752, 3, doi: 10.1088/0004-637X/752/1/3
Tielens, A. G. G. M. 2008, Annual Review of Astronomy and Astrophysics, 46, 289, doi: 10.1146/annurev.astro.46.060407.145211
Useli-Bacchitta, F., Bonnamy, A., Mulas, G., et al. 2010, Chemical Physics, 371, 16, doi: 10.1016/j.chemphys.2010.03.012
Weigend, F., & Ahlrichs, R. 2005, Physical Chemistry Chemical Physics, 7, 3297, doi: 10.1039/B508541A
Wenzel, G., Cooke, I. R., Changala, P. B., et al. 2024, Science, 386, 810, doi: 10.1126/science.adq6391
Wenzel, G., Speak, T. H., Changala, P. B., et al. 2025, Nature Astronomy, 9, 262, doi: 10.1038/s41550-024-02410-9
West, N. A., Millar, T. J., Van de Sande, M., et al. 2019, The Astrophysical Journal, 885, 134, doi: 10.3847/1538-4357/ab480e
Xue, C. 2024, GBT Spectral Line Reduction Pipeline. https://github.com/cixue/gotham-spectral-pipeline
Zeichner, S. S., Aponte, J. C., Bhattacharjee, S., et al. 2023, Science, 382, 1411, doi: 10.1126/science.adg6304
Zhao, L., Kaiser, R. I., Xu, B., et al. 2018, Nature Astronomy, 2, 413, doi: 10.1038/s41550-018-0399-y
Zhen, J., Rodriguez Castillo, S., Joblin, C., et al. 2016, The Astrophysical Journal, 822, 113, doi: 10.3847/0004-637X/822/2/113
الملحق
أ. مسار التخليق الكامل إلى سيانكورونين
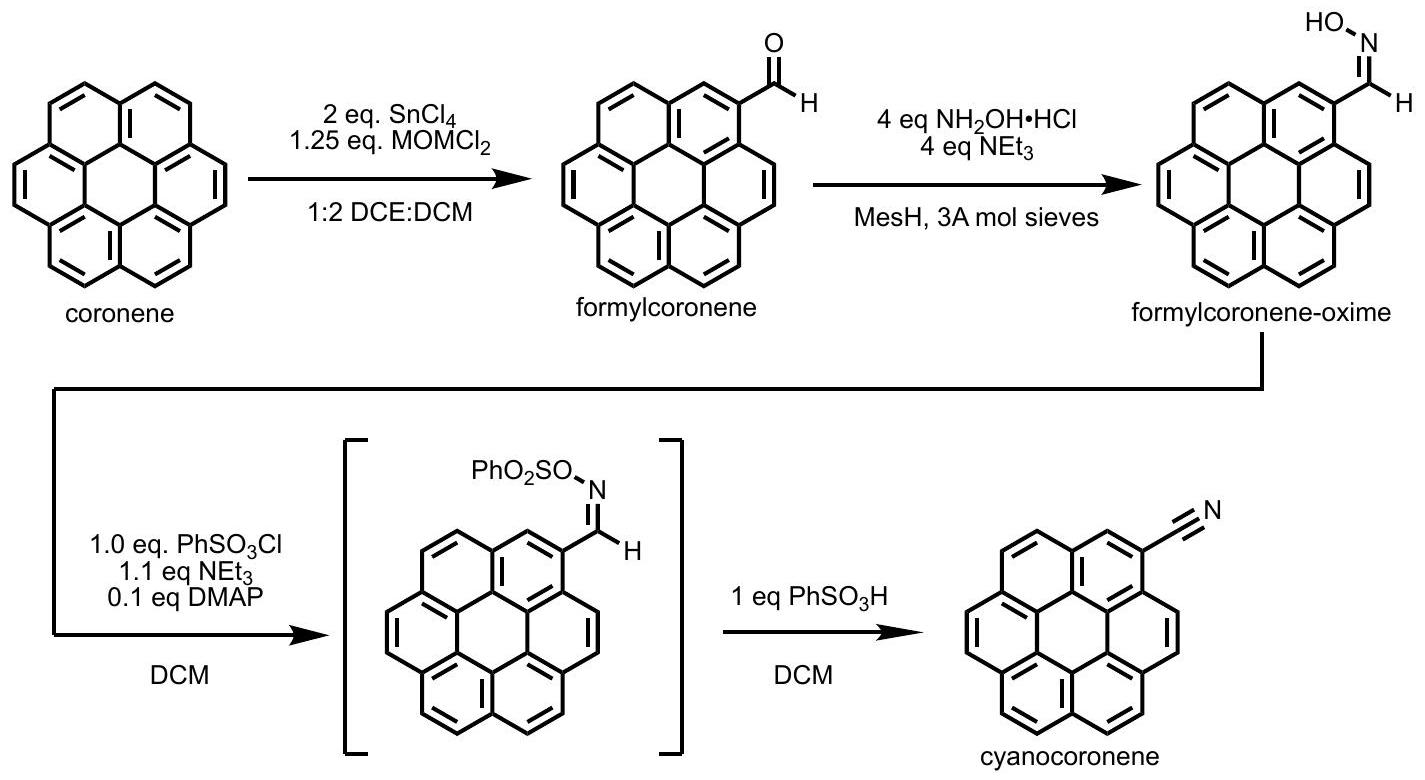
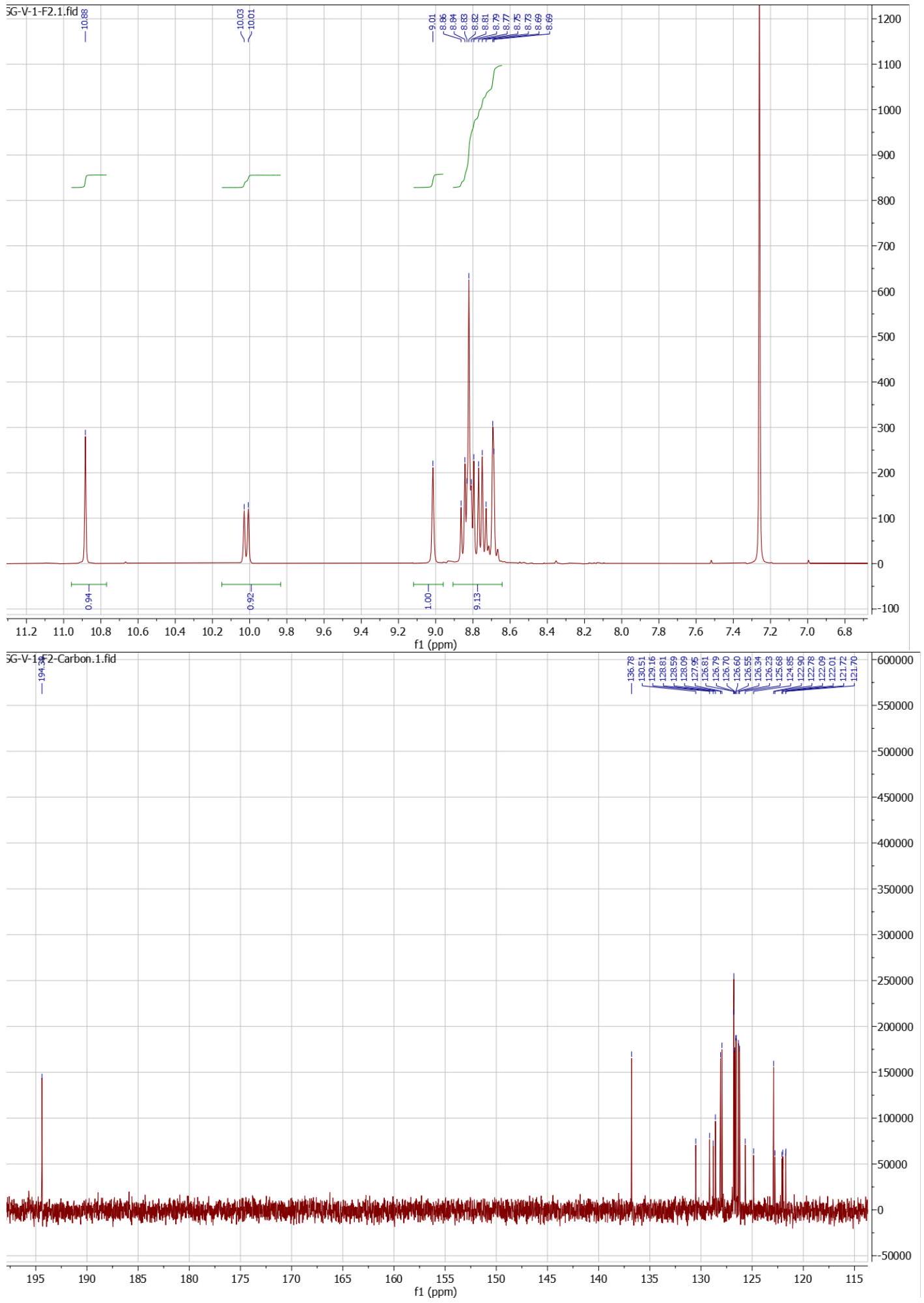
أ.1. تخليق الفورميلكورونين
- سوف تطلق التفاعل غاز HCl أثناء التسخين. يُنصح بالحذر.
- لم تُظهر التفاعل أي تحسين في العائد بعد مضاعفة المعادلة.
و . ومع ذلك، فإن معظم المواد الأولية قابلة للاسترداد. - المنتج والمواد الأولية غير المتفاعلة كلاهما ذو قابلية ذوبان ضعيفة في مجموعة واسعة من المذيبات العضوية. وبالتالي، فإن كميات كبيرة (قد تتجاوز 6 لترات) من DCM مطلوبة لإجراء الكروماتوغرافيا على هذا النطاق.
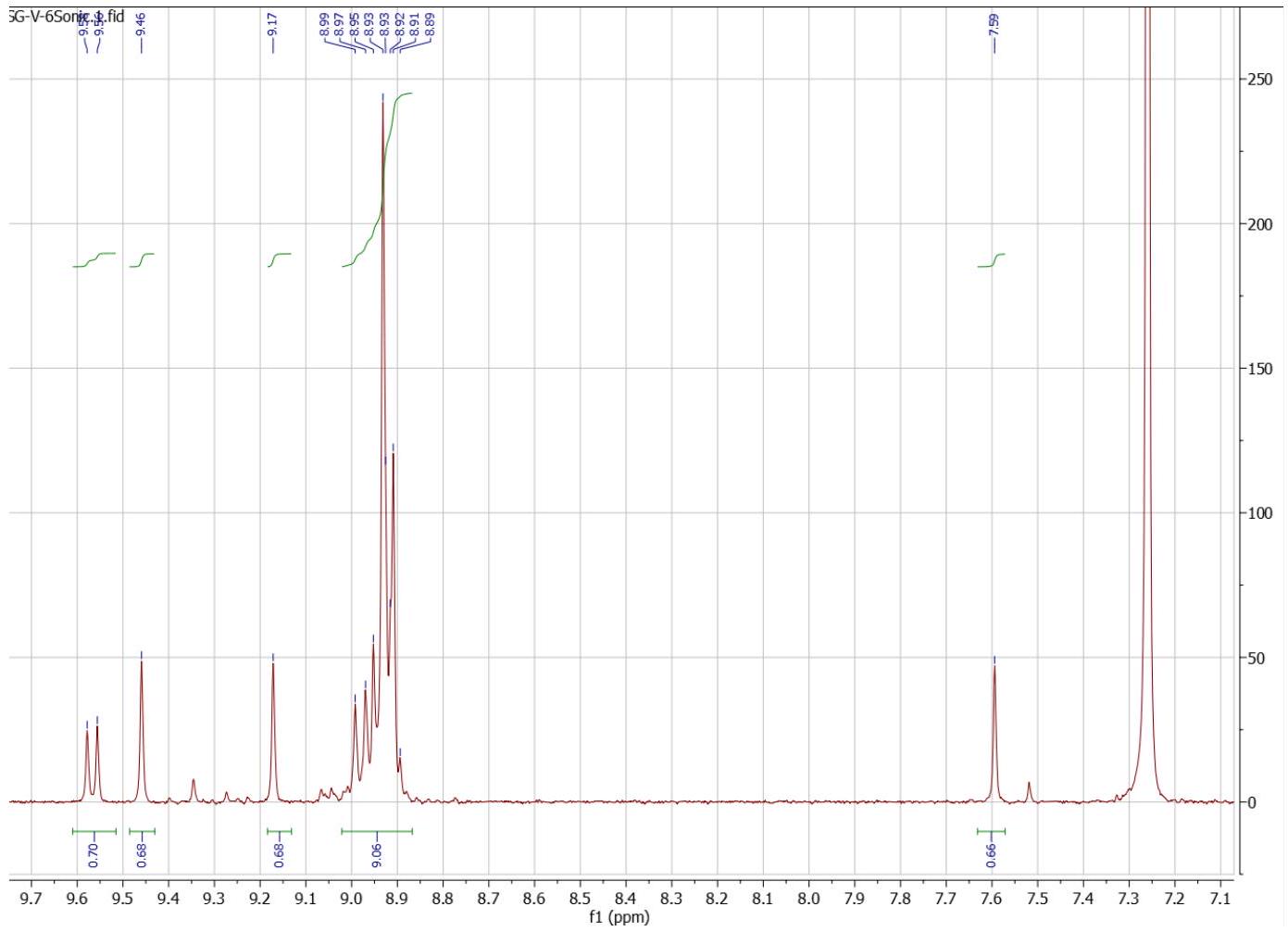
أ.2. تخليق الفورميلكورونين-أوكسيما
- خليط التفاعل غير متجانس ويمكن أن يلتصق بجدران الوعاء إذا تم تحريكه بعنف شديد، مما يؤدي إلى تفاعل غير مكتمل. يُفضل التحريك البطيء.
أ.3. تخليق السيانكورونين
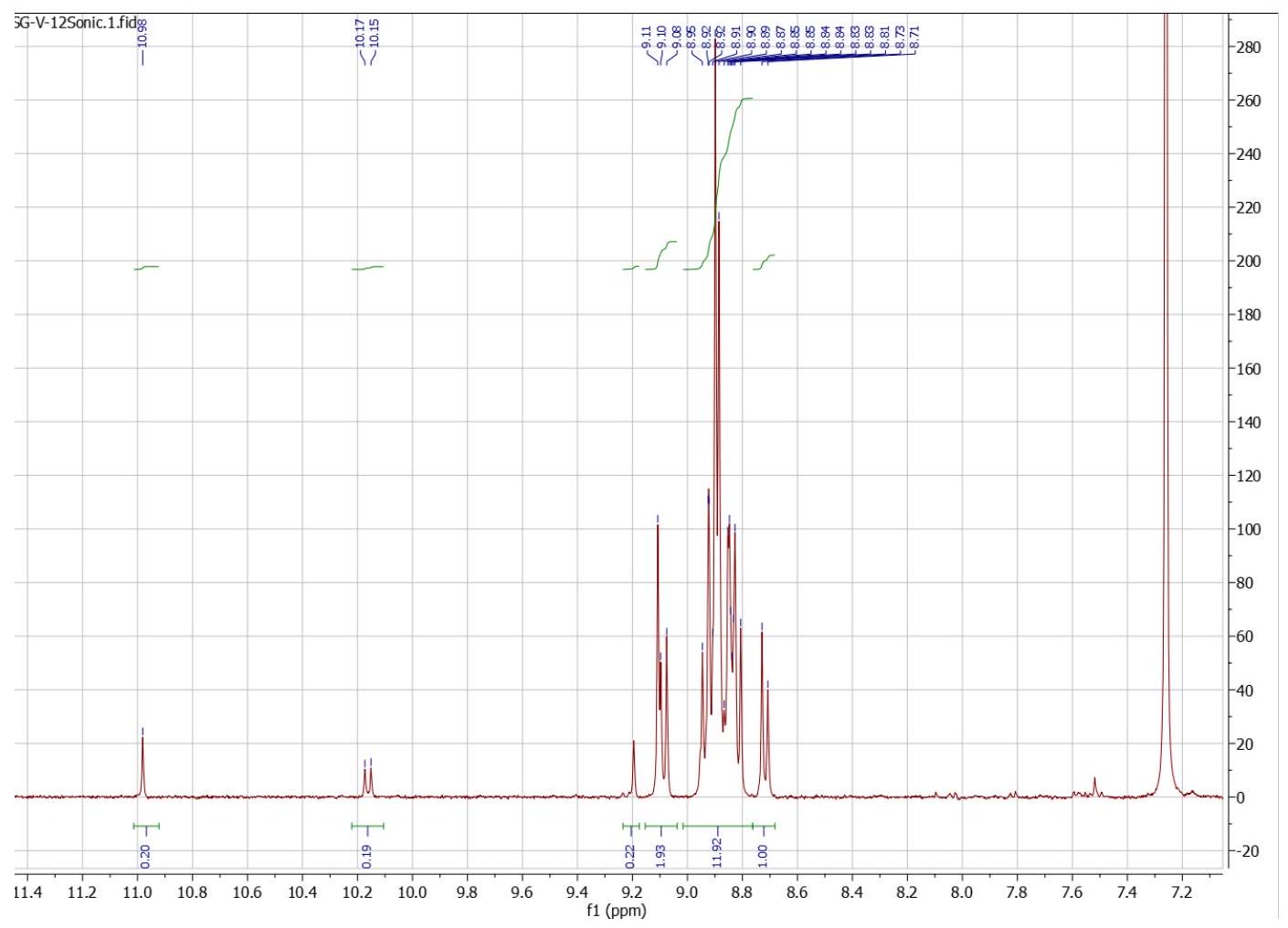
- التحويل المباشر للفورميلكورونين إلى سيانكورونين وفقًا لبروتوكول الأدبيات (هايو دو وآخرون 2017) صعب بسبب التفاعل المحدود للفورميلكورونين في درجة حرارة الغرفة. يتم تحقيق تحويل ملحوظ فقط بشكل موثوق في التولوين المغلي أو الكلوروبنزين أو الميسيتيلين. ومع ذلك، فإن ظروف التفاعل الحمضية المدمجة مع درجات الحرارة العالية غالبًا ما تؤدي إلى تدهور كبير في المادة الأولية وتقلل بشكل كبير من العوائد.
- المتوسط O-sulfonyl oxime حساس للتحلل المائي. لا يُوصى بعزله.
- خليط التفاعل غير متجانس ويمكن أن يلتصق بجدران الوعاء إذا تم تحريكه بعنف شديد، مما يؤدي إلى تفاعل غير مكتمل. يُفضل التحريك البطيء.
- كميات وفيرة
كان من الضروري إكمال عملية الكروماتوغرافيا بسبب انخفاض قابلية ذوبان المنتج. يمكن التخفيف من انسداد الترسيب عن طريق إزعاج الجزء العلوي من العمود برفق.
ب. معيار مستوى النظرية
| معامل | 1-سيانوبييرين | ||
| نظري | تجريبي
|
نظري + تجريبي
|
|
|
|
٨٥٠.١٤١ | 843.140191(128) | 843.141827(128) |
|
|
٣٧٢.٩٣١ | ٣٧٢.٥٠٠١٧٥(٥٦) | ٣٧٢.٥٠٠١٨٣(٥٦) |
|
|
٢٥٩٫٢١٩ | 258.4249175(164) | 258.4248913(164) |
|
|
1.977 | ٢.٢٤٠(٨٠) | 2.153(80)) |
|
|
-5.556 | -5.52(101) | -5.88(101) |
|
|
٢٠.٣١٠ | [0] | [20.310] |
|
|
0.724 | 0.826(40) | 0.795(40) |
|
|
٣.٠٥٩ | 5.26(74) | ٤.٢٠(٧٤) |
| معامل | 2-سيانوبييرين | ||
| نظري | تجريبي
|
نظري + تجريبي
|
|
|
|
١٠١٥٫٢٣٩ | 1009.19382(60) | 1009.19356(39) |
|
|
314.479 | 313.1345299(202) | 313.1345270(195) |
|
|
٢٤٠.١٠٥ | 239.0427225(184) | 239.0427270(167) |
|
|
0.706 | 0.7008(109) | 0.7023(106) |
|
|
٥.٣٧٥ | 5.814(94) | 5.818(94) |
|
|
8.785 | 15.3(114) | [8.785] |
|
|
0.184 | 0.1759(60) | 0.1766(59) |
|
|
٤.٥١٠ | 4.22(39) | ٤.١٢(٣٥) |
| معامل | 4-سيانوبييرين | ||
| نظري | تجريبي
|
نظري + تجريبي
|
|
|
|
652.155 | 651.383034(69) | 651.382955(64) |
|
|
٤٥٦٫٦٧٠ | 453.731352(45) | 453.731444(41) |
|
|
٢٦٨٫٥٩٠ | 267.5078168(224) | 267.5078004(221) |
|
|
1.893 | 1.780(98) | 2.026(69) |
|
|
-1.553 | 0.43(58) | [-1.553] |
|
|
14.821 | 10.89(73) | 12.61(53) |
|
|
0.756 | 0.677(49) | 0.803(35) |
|
|
1.971 | 2.56(33) | 2.40(33) |
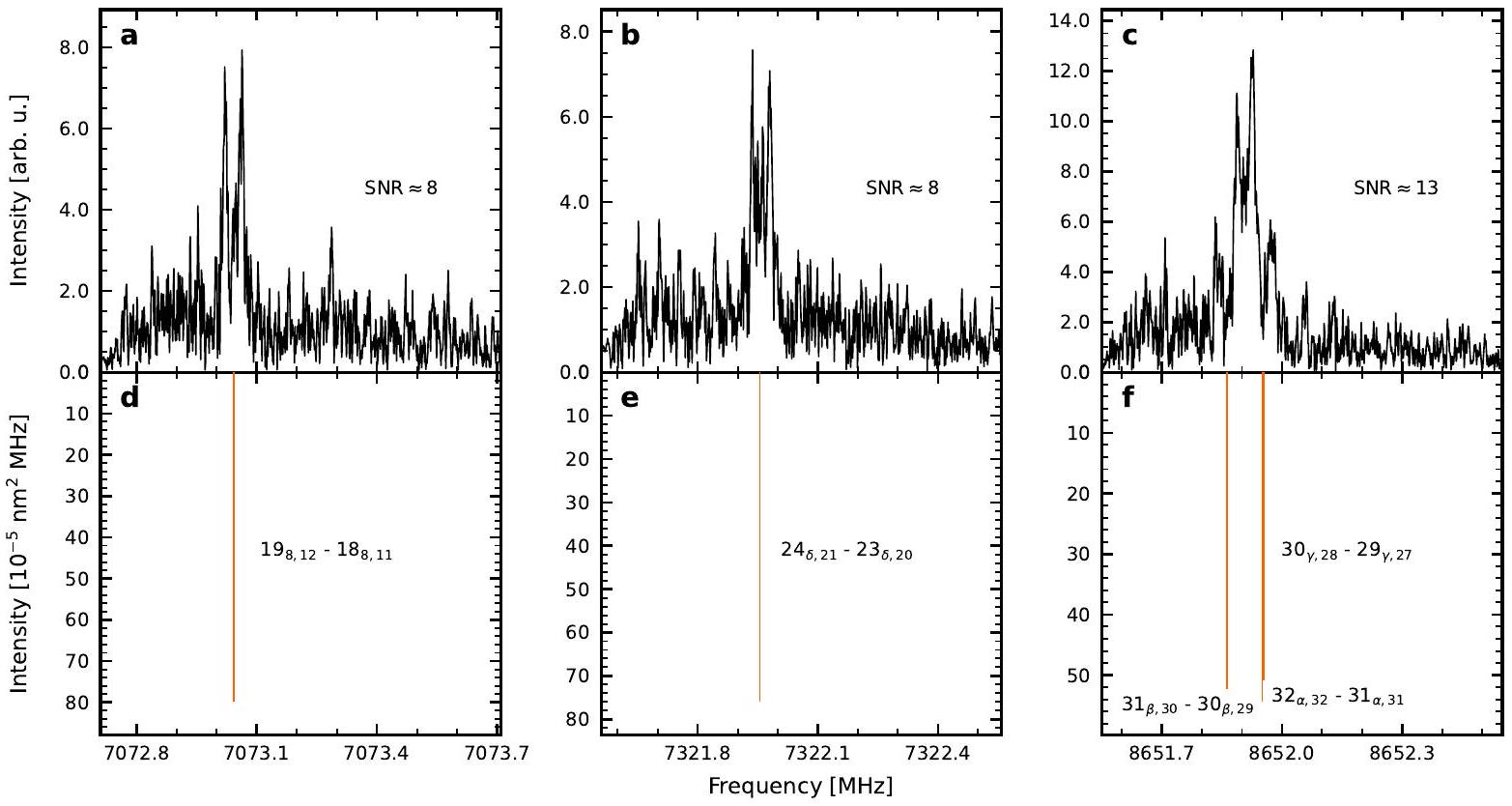
ج. خطوط قياس السيانكورونين
| الانتقال
|
التردد
|
|
|
6788.4098 |
|
|
6788.4098 |
|
|
6788.4443 |
|
|
6788.4443 |
|
|
6788.7145 |
|
|
6788.7145 |
|
|
6789.9187 |
|
|
6789.9187 |
|
|
6815.8858 |
|
|
7005.2518 |
|
|
٧٠٥٤.٦١٠٦ |
|
|
7054.6106 |
|
|
7054.6617 |
|
|
7054.6617 |
|
|
٧٠٥٤.٨٧٥٩ |
|
|
٧٠٥٤.٨٧٥٩ |
|
|
7055.9209 |
|
|
7055.9209 |
|
|
٧٠٥٨.٧٨٥٧ |
|
|
7058.7857 |
|
|
7073.0418 |
|
|
٧٠٨٠.٦٣٥٣ |
|
|
٧٠٨٨.٦٠٠٤ |
|
|
٧٢٩١.٤٧١٠ |
|
|
٧٣٢٠.٨١٧٩ |
|
|
٧٣٢٠.٨١٧٩ |
|
|
٧٣٢٠.٨٧٨٠ |
|
|
٧٣٢٠.٨٧٨٠ |
|
|
7321.0420 |
|
|
7321.0420 |
|
|
7321.9574 |
|
|
7321.9574 |
|
|
٧٣٢٤.٤٣٩٣ |
|
|
٧٣٢٤.٤٣٩٣ |
| الانتقال
|
التردد
|
|
|
7587.0283 |
|
|
7587.0283 |
|
|
7587.0875 |
|
|
7587.0875 |
|
|
8377.6038 |
|
|
٨٣٨٥.٦٥٠٥ |
|
|
٨٣٨٥.٦٥٠٥ |
|
|
٨٣٨٥.٧٣٤٧ |
|
|
٨٣٨٥.٧٣٤٧ |
|
|
٨٣٨٥.٧٦٣٦ |
|
|
٨٣٨٥.٧٦٣٦ |
|
|
8391.1806 |
|
|
8391.1806 |
|
|
8651.8594 |
|
|
٨٦٥١.٨٥٩٤ |
|
|
8651.9466 |
|
|
8651.9466 |
|
|
8651.9537 |
|
|
8651.9537 |
|
|
8652.4539 |
|
|
8652.4539 |
|
|
8653.7843 |
|
|
8653.7843 |
|
|
8656.7527 |
|
|
8656.7527 |
|
|
١٠٥١٥.٣٤٣٧ |
|
|
١٠٥١٥.٣٤٣٧ |
|
|
١٠٥١٥.٣٤٣٧ |
|
|
١٠٥١٥.٣٤٣٧ |
|
|
١٠٥١٥.٤٥٢٩ |
|
|
١٠٥١٥.٤٥٢٩ |
|
|
١٠٥١٦.٢٣٥٦ |
|
|
١٠٥١٦.٢٣٥٦ |
|
|
١٠٥١٧.٦٧٠٣ |
|
|
١٠٥١٧.٦٧٠٣ |
|
|
١٠٥٢٠.٤٣١٣ |
|
|
١٠٥٢٠.٤٣١٣ |
د. دالة التقسيم لسيانكورونين
| درجة الحرارة [ك] | دالة التقسيم |
| 1.0 | 1703.7230 |
| 2.0 | ٤٨١٣.٧٢٤٥ |
| 3.0 | 8840.2413 |
| ٤.٠ | ١٣٦٠٨.٠٣٣٣ |
| 5.0 | ١٩٠١٥.٧٨٩٧ |
| 6.0 | ٢٤٩٩٥.١٤٣٧ |
| 7.0 | 31495.9011 |
| 8.0 | 38479.1687 |
| 9.375 | ٤٨٨١٢.٤٩٢٩ |
| 18.75 | 138047.6140 |
| 37.5 | 390439.4924 |
| 75.0 | ١١٠٤٣١٧.٣٢٩٢ |
| 150.0 | ٣١٢٠٠٧٨.٨٦٥٧ |
| ٢٢٥.٠ | ٥٦٨٦٧٥٩٫١٢٤١ |
| ٣٠٠.٠ | ٨٥٨٩٥٢٦.٦٧٢٥ |
| ٤٠٠.٠ | ١٢٦٧٨٧٤٢.٢٠٦٠ |
| ٥٠٠.٠ | 16744897.1786 |
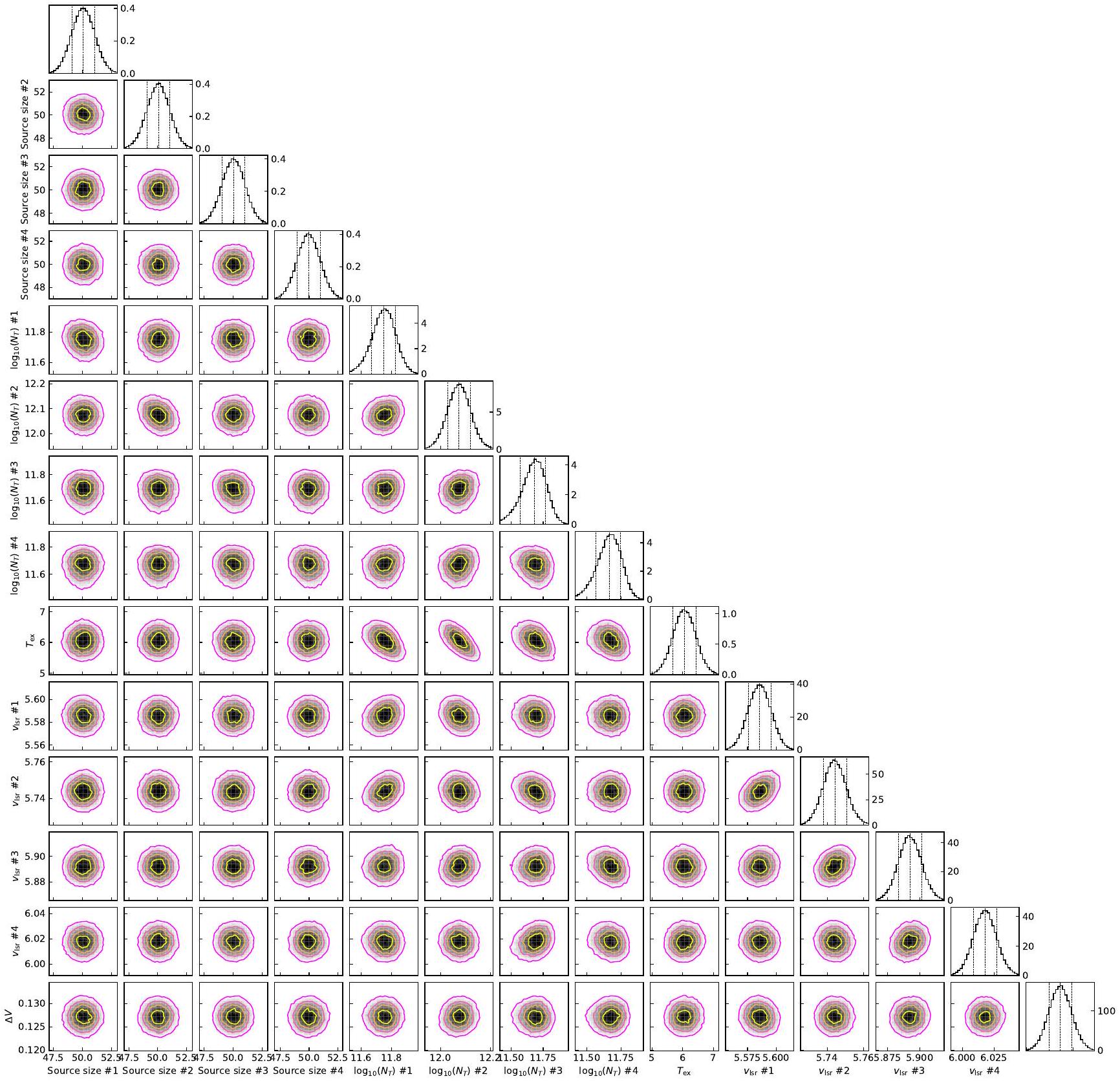
تحليل MCMC للسيانكورونين في TMC-1
| رقم المكون |
|
الحجم (“) |
|
|
|
| 1 |
|
||||
| ٢ |
|
|
|
|
|
| ٣ |
|
||||
| ٤ |
|
||||
| من | 0.0 | 1 | 10.0 | 3.0 | 0.1 |
| ماكس | 10.0 | 100 | ١٣.٠ | 15.0 | 0.3 |
| رقم المكون |
|
الحجم (“) |
|
|
|
| 1 |
|
50 |
|
|
|
| 2 |
|
50 |
|
||
| ٣ |
|
50 |
|
||
| ٤ |
|
٤٩ |
|
||
|
|
|||||
F. كثافات الأعمدة للهيدروكربونات الحلقية في TMC-1
| جزيء |
|
كثافة العمود (
|
مرجع |
|
|
٥ |
|
سيرنيتشارو وآخرون (2021أ) |
|
|
٦ |
|
سيرنيتشارو وآخرون (2021ب) |
|
|
٦ |
|
لي وآخرون (2021) |
|
|
٦ |
|
لي وآخرون (2021) |
|
|
٧ |
|
سيرنيتشارو وآخرون (2021ج) |
|
|
٧ |
|
سيرنيتشارو وآخرون (2021ج) |
|
|
٧ |
|
سيرنيتشارو وآخرون (2022) |
|
|
٧ |
|
مكغواير وآخرون (2021) |
|
|
٨ |
|
لور و آخرون (2023) |
|
|
9 |
|
سيتا وآخرون (2022) |
|
|
10 |
|
سيتا وآخرون (2022) |
|
|
11 |
|
ماكغواير وآخرون (2021) |
|
|
11 |
|
ماكغواير وآخرون (2021) |
|
|
١٣ |
|
سيرنيتشارو وآخرون (2024) |
|
|
١٣ |
|
سيرنيتشارو وآخرون (2024) |
|
|
17 |
|
وينزل وآخرون (2024) |
|
|
17 |
|
وينزل وآخرون (2025) |
|
|
17 |
|
وينزل وآخرون (2025) |
|
|
16 |
|
وينزل وآخرون (2025) |
|
|
25 |
|
هذا العمل |
|
|
٢٤ |
|
هذا العمل |
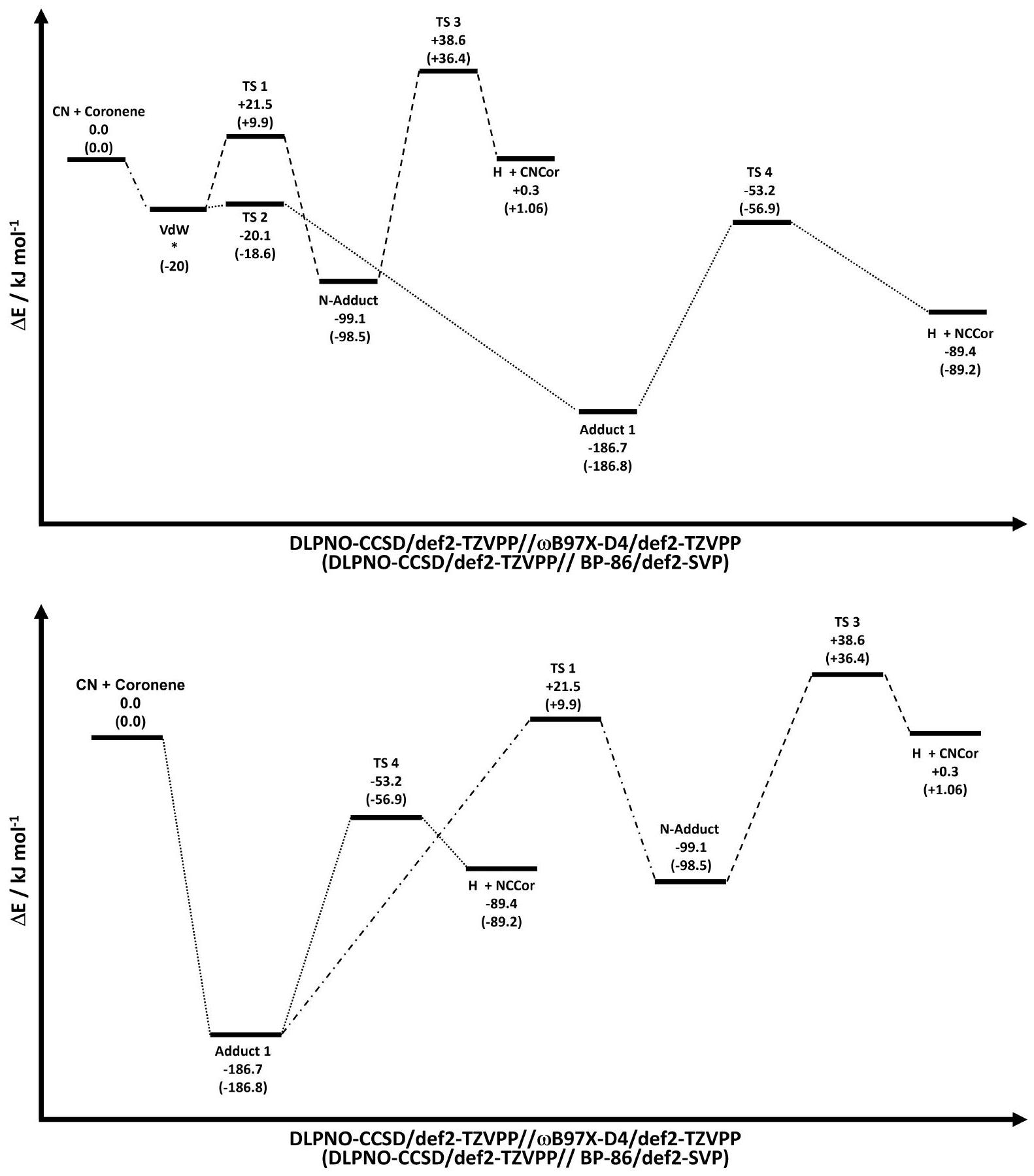
حسابات الكيمياء الكمومية من البداية
ج.1. المنهجية الحاسوبية
في هذه المسوحات، تم السماح لجميع الإحداثيات باستثناء الرابطة التي يتم مسحها بالاسترخاء بينما تم تغيير الإحداثية الممسوحة. تم استخدام القيم القصوى الناتجة كإدخالات للهندسة في تحسينات حالة الانتقال، وتم تحسين القيم الدنيا بعيدة المدى قبل إضافة CN إلى مركب مرتبط فضفاض في قناة الدخول.
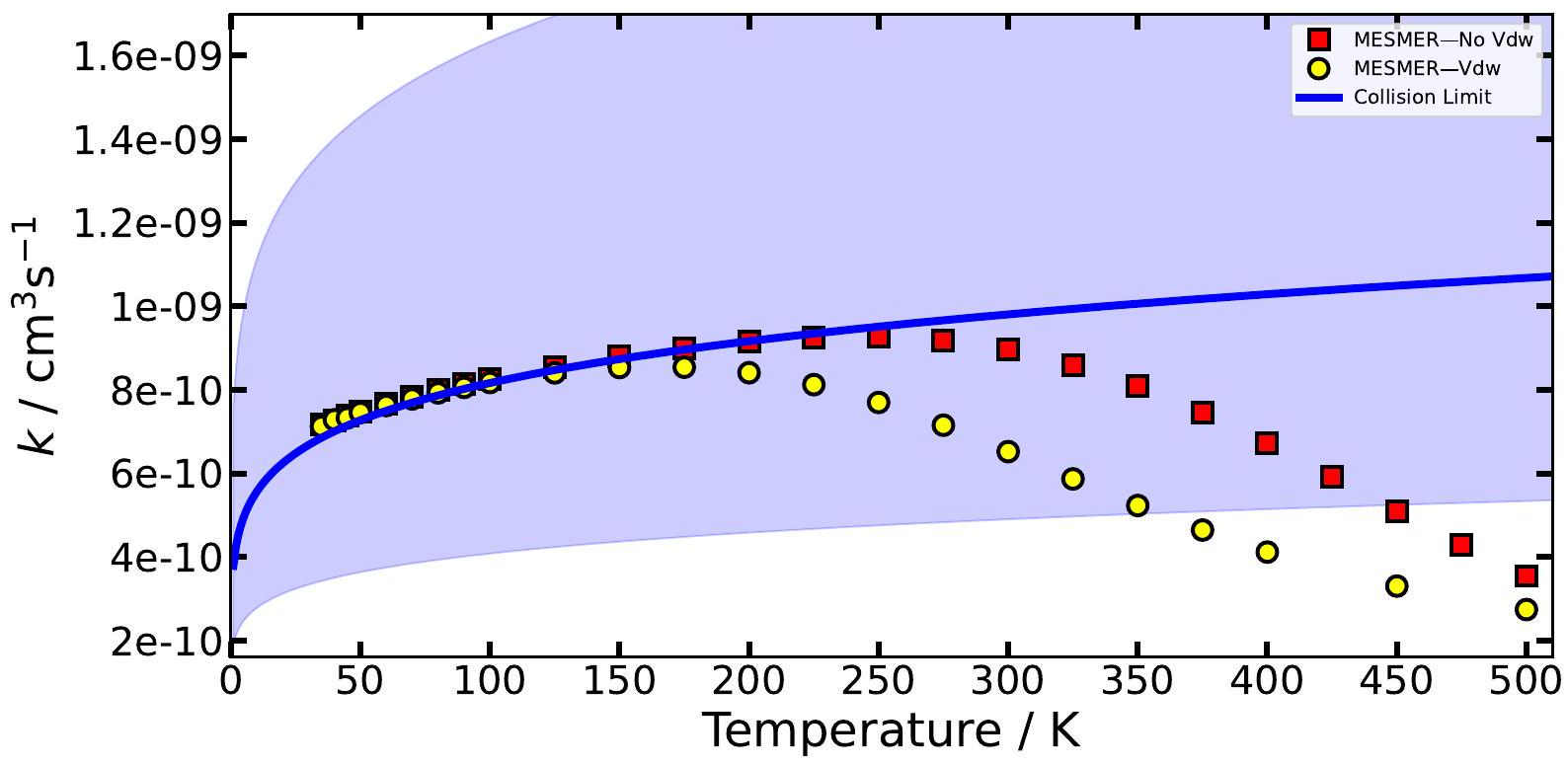
ج.2. توقعات الديناميكا للمعادلة الرئيسية
| 1-1 | 1-2 | 1-3 | 1-4 | 1-5 | 2-1 | 2-2 | 2-3 | 2-4 | 2-5 | |
| CN + كورونين | 0.0 | 0.00 | 0.0 | 0.0 | 0.0 | 0.0 | 0.00 | 0.0 | 0.0 | 0.0 |
| فدW | -20.57 | -20.26 | -25.82 | * | * | * | ||||
| TS 1 (إضافة CN) | 9.87 | 14.42 | 3.83 | 21.48 | 25.03 | 13.18 | ||||
| N-أدكت 1 | -98.48 | -90.90 | -98.57 | -99.08 | -91.60 | -101.41 | ||||
| إزالة TS 3 H | ٣٦.٣٥ | 42.57 | ٣٣.٣٨ | ٣٨.٥٥ | ٤٥.٣٧ | ٣٤.٢٣ | ||||
| H + إيزوسيانوكورونين | 1.06 | 0.14 | 1.72 | 1.12 | -١٦.٢٠ | 0.33 | -0.68 | 0.20 | 0.94 | -14.17 |
| TS 2 (إضافة NC) | -18.57 | -18.27 | -23.82 | -20.09 | -18.52 | -25.05 | ||||
| العضلة المضافة 1 | -186.80 | -179.23 | -184.50 | -186.68 | -179.22 | -186.00 | ||||
| إزالة TS 4 H | -56.87 | -50.57 | -57.91 | -53.20 | -٤٦.٢٧ | -54.98 | ||||
| H + سيانكورونين | -89.15 | -89.97 | -86.33 | -89.88 | -106.47 | -89.39 | -90.31 | -86.53 | -88.90 | -١٠٣.٦٧ |
https://greenbankobservatory.org/portal/gbt/gbt-legacy-archive/gotham-data/ عدم اليقين التجريبي هو 2 كيلوهرتز. - *تم التقدير باستخدام كثافات عمود السيانوبيرين والسيانكورونين، ومعاملات المعدل المحسوبة لإضافة CN، ونسبة CN/H قدرها 0.15 (انظر الملحق G و وينزل وآخرون 2025).
DOI: https://doi.org/10.3847/2041-8213/adc911
PMID: https://pubmed.ncbi.nlm.nih.gov/41103619
Publication Date: 2025-04-30
Discovery of the
Abstract
We present the synthesis and laboratory rotational spectroscopy of the 7 -ring polycyclic aromatic hydrocarbon
1. INTRODUCTION

diffuse interstellar bands (DIBs) has been debated. Dehydrogenated, protonated, and cationic coronene were proposed as potential carriers of DIBs (Pathak & Sarre 2008; Malloci et al. 2008), but these hypotheses were disproven (Garkusha et al. 2011; Useli-Bacchitta et al. 2010; Hardy et al. 2017). Nevertheless, some distribution of PAHs remain promising DIB carrier candidates due to their close relation to the fullerene family (Campbell et al. 2015).
2. SYNTHESIS
3. LABORATORY SPECTROSCOPY
| Parameter | B3LYP aug-cc-pVTZ | Experimental
|
|
|
335.393 | 333.852989(249) |
|
|
222.035 | 221.2700880(838) |
|
|
133.594 | 133.1081015(122) |
|
|
0.669 | [0.669] |
|
|
-0.617 | [-0.617] |
|
|
0.011 | [0.011] |
|
|
-0.120 | [-0.120] |
|
|
-0.494 | [-0.494] |
|
|
71 | |
|
|
38 | |
|
|
2.595 | |
|
|
|
|
rotational constants,
4. OBSERVATIONS
5. ASTRONOMICAL ANALYSIS


6. DISCUSSION
phase formation route for pyrene, starting from 4phenanthrenyl radical. Indeed, phenanthrene is also a member of the most thermodynamically stable PAH polymerization route (see Fig 5). However, cursory searches for its CN-derivative 9-cyanophenanthrene, whose rotational spectrum is known (McNaughton et al. 2018), in our GOTHAM observations have not yet been successful. This could be due to the fact that the spectroscopy of only one of the five possible cyanophenan-


and Bull et al. (2025) indicate that the underlying PAH backbone can be maintained via efficient radiative cooling, thereby opening up the possibility of a kind of chemical “recycling” of PAHs that would certainly contribute to the high observed abundance of, e.g., cyanocoronene. Turning to depletion onto grains, Dartois et al. (2022) conducted experiments on the sputtering yield of solidphase perylene and coronene bombarded by energetic ions, analogous to the cosmic ray exposure of species in dust-grain ice mantles. They found that such cosmic ray-induced sputtering is efficient under ISM conditions, and even predict a gas-phase fractional abundance of coronene over
7. CONCLUSIONS
8. DATA ACCESS & CODE
Facilities: GBT
ACKNOWLEDGMENTS
tion Beckman Young Investigator Award. Z.T.P.F. and B.A.M. gratefully acknowledge the support of Schmidt Family Futures. I.R.C. acknowledges support from the University of British Columbia and the Natural Sciences and Engineering Research Council of Canada (NSERC). I.R.C. and T.H.S. acknowledge the support of the Canadian Space Agency (CSA) through grant 24AO3UBC14. P.B.C. is supported by NIST. The National Radio Astronomy Observatory is a facility of the National Science Foundation operated under cooperative agreement by Associated Universities, Inc. The Green Bank Observatory is a facility of the National Science Foundation operated under cooperative agreement by Associated Universities, Inc.
REFERENCES
Baer, T., & Hase, W. L. 1996, Unimolecular Reaction Dynamics: Theory and Experiments (Oxford University Press). https://academic.oup.com/book/40815
Bahou, M., Wu, Y.-J., & Lee, Y.-P. 2014, Angewandte Chemie, 126, 1039, doi: 10.1002/ange. 201308971
Bakes, E. L. O., & Tielens, A. G. G. M. 1998, The Astrophysical Journal, 499, 258, doi: 10.1086/305625
Balle, T. J., & Flygare, W. H. 1981, Review of Scientific Instruments, 52, 33, doi: 10.1063/1.1136443
Balucani, N., Asvany, O., Huang, L. C. L., et al. 2000, The Astrophysical Journal, 545, 892, doi: 10.1086/317848
Bauschlicher, C. W. 1998, The Astrophysical Journal, 509, L125, doi: 10.1086/311782
Becke, A. D. 1988, Physical Review A, 38, 3098, doi: 10.1103/PhysRevA.38.3098
-. 1993, The Journal of Chemical Physics, 98, 5648, doi: 10.1063/1.464913
Becke, A. D., & Johnson, E. R. 2006, The Journal of Chemical Physics, 124, 221101, doi: 10.1063/1.2213970
Bernstein, M. P., Elsila, J. E., Dworkin, J. P., et al. 2002, The Astrophysical Journal, 576, 1115, doi: 10.1086/341863
Berné, O., Foschino, S., Jalabert, F., & Joblin, C. 2022, Astronomy & Astrophysics, 667, A159, doi: 10.1051/0004-6361/202243171
Boschman, L., Cazaux, S., Spaans, M., Hoekstra, R., & Schlathölter, T. 2015, Astronomy & Astrophysics, 579, A72, doi: 10.1051/0004-6361/201323165
Burkhardt, A. M., Long Kelvin Lee, K., Bryan Changala, P., et al. 2021, The Astrophysical Journal Letters, 913, L18, doi: 10.3847/2041-8213/abfd3a
Caldeweyher, E., Bannwarth, C., & Grimme, S. 2017, The Journal of Chemical Physics, 147, 034112, doi: 10.1063/1.4993215
Campbell, E. K., Holz, M., Gerlich, D., & Maier, J. P. 2015, Nature, 523, 322, doi: 10.1038/nature14566
Carelli, F., & Gianturco, F. A. 2012, Monthly Notices of the Royal Astronomical Society, 422, 3643, doi: 10.1111/j.1365-2966.2012.20876.x
Cazaux, S., Boschman, L., Rougeau, N., et al. 2016, Scientific Reports, 6, 19835, doi: 10.1038/srep19835
Cernicharo, J., Agúndez, M., Cabezas, C., et al. 2021a, Astronomy and Astrophysics, 649, L15, doi: 10.1051/0004-6361/202141156
Cernicharo, J., Agúndez, M., Kaiser, R. I., et al. 2021b, Astronomy & Astrophysics, 652, L9, doi: 10.1051/0004-6361/202141660
—. 2021c, Astronomy & Astrophysics, 655, L1, doi: 10.1051/0004-6361/202142226
Cernicharo, J., Fuentetaja, R., Agúndez, M., et al. 2022, Astronomy & Astrophysics, 663, L9, doi: 10.1051/0004-6361/202244399
Cernicharo, J., Cabezas, C., Fuentetaja, R., et al. 2024, Astronomy & Astrophysics, 690, L13, doi: 10.1051/0004-6361/202452196
Chai, J.-D., & Head-Gordon, M. 2008, The Journal of Chemical Physics, 128, 084106, doi: 10.1063/1.2834918
Chen, T., Luo, Y., & Li, A. 2020, Astronomy & Astrophysics, 633, A103, doi: 10.1051/0004-6361/201936873
Clar, E. 1964, Polycyclic Hydrocarbons (Berlin, Heidelberg: Springer Berlin Heidelberg), doi: 10.1007/978-3-662-01668-8
-. 1983, in Mobile Source Emissions Including Policyclic Organic Species, ed. D. Rondia, M. Cooke, & R. K. Haroz (Dordrecht: Springer Netherlands), 49-58, doi: 10.1007/978-94-009-7197-4_4
Cooke, I. R., Gupta, D., Messinger, J. P., & Sims, I. R. 2020, The Astrophysical Journal Letters, 891, L41, doi: 10.3847/2041-8213/ab7a9c
Crabtree, K. N., Martin-Drumel, M.-A., Brown, G. G., et al. 2016, The Journal of Chemical Physics, 144, 124201, doi: 10.1063/1.4944072
Dale, T. J., & Rebek, J. 2006, Journal of the American Chemical Society, 128, 4500, doi: 10.1021/ja057449i
Dartois, E., Chabot, M., Koch, F., et al. 2022, A&A, 663, A25, doi: 10.1051/0004-6361/202243274
Davidson, E. R. 1996, Chemical Physics Letters, 260, 514, doi: 10.1016/0009-2614(96)00917-7
Davies, J. W., Green, N. J. B., & Pilling, M. J. 1986, Chemical Physics Letters, 126, 373, doi: 10.1016/S0009-2614(86)80101-4
Dopfer, O. 2011, EAS Publications Series, 46, 103, doi: 10.1051/eas/1146010
Dunning, Jr., T. H. 1989, The Journal of Chemical Physics, 90, 1007, doi: 10.1063/1.456153
Dwek, E., Arendt, R. G., Fixsen, D. J., et al. 1997, The Astrophysical Journal, 475, 565, doi: 10.1086/303568
Frisch, M. J., Trucks, G. W., Schlegel, H. B., et al. 2016, Gaussian~16 revision C. 01
Garkusha, I., Fulara, J., Sarre, P. J., & Maier, J. P. 2011, The Journal of Physical Chemistry A, 115, 10972, doi: 10.1021/jp206188a
Gatchell, M., Ameixa, J., Ji, M., et al. 2021, Nature Communications, 12, 6646, doi: 10.1038/s41467-021-26899-0
Georgievskii, Y., & Klippenstein, S. J. 2005, The Journal of Chemical Physics, 122, 194103, doi: 10.1063/1.1899603
Glowacki, D. R., Liang, C.-H., Morley, C., Pilling, M. J., & Robertson, S. H. 2012, The Journal of Physical Chemistry A, 116, 9545, doi: 10.1021/jp3051033
Grimme, S., Ehrlich, S., & Goerigk, L. 2011, Journal of Computational Chemistry, 32, 1456, doi: 10.1002/jcc. 21759
Habart, E., Natta, A., & Krügel, E. 2004, Astronomy and Astrophysics, 427, 179, doi: 10.1051/0004-6361:20035916
Hardy, F.-X., Rice, C. A., & Maier, J. P. 2017, The Astrophysical Journal, 836, 37, doi: 10.3847/1538-4357/836/1/37
Hill, G. 2016, ccRepo. http: //www.grant-hill.group.shef.ac.uk/ccrepo/index.html
Holbrook, K. A., Pilling, M. J., Robertson, S. H., & Robinson, P. J. 1996, Unimolecular reactions, Wiley
Hudgins, D. M., & Allamandola, L. J. 1995, The Journal of Physical Chemistry, 99, 3033, doi: 10.1021/j100010a011
Hyodo, K., Togashi, K., Oishi, N., Hasegawa, G., & Uchida, K. 2017, Organic Letters, 19, 3005, doi: 10.1021/acs.orglett.7b01263
Ishida, K., Morokuma, K., & Komornicki, A. 1977, The Journal of Chemical Physics, 66, 2153, doi: 10.1063/1.434152
Joblin, C., Boissel, P., Léger, A., D’Hendecourt, L., & Defourneau, D. 1995, Astronomy & Astrophysics, 299, 835. http://adsabs.harvard.edu/abs/1995A%26A…299..835J
Joblin, C., Wenzel, G., Castillo, S. R., et al. 2020, Journal of Physics: Conference Series, 1412, 062002, doi: 10.1088/1742-6596/1412/6/062002
Johnson, R. I. 2022, NIST computational chemistry comparison and benchmark database. http://cccbdb.nist.gov/
Jurečka, P., Šponer, J., Černý, J., & Hobza, P. 2006, Physical Chemistry Chemical Physics, 8, 1985, doi: 10.1039/B600027D
Kendall, R. A., Dunning, Jr., T. H., & Harrison, R. J. 1992, The Journal of Chemical Physics, 96, 6796, doi: 10.1063/1.462569
Kesharwani, M. K., Brauer, B., & Martin, J. M. L. 2015, The Journal of Physical Chemistry A, 119, 1701, doi: 10.1021/jp508422u
Le Page, V., Snow, T. P., & Bierbaum, V. M. 2009, The Astrophysical Journal, 704, 274, doi: 10.1088/0004-637X/704/1/274
Lee, C., Yang, W., & Parr, R. G. 1988, Physical Review B, 37, 785, doi: 10.1103/PhysRevB.37.785
Lee, K. L. K., Changala, P. B., Loomis, R. A., et al. 2021, The Astrophysical Journal Letters, 910, L2, doi: 10.3847/2041-8213/abe764
Liakos, D. G., & Neese, F. 2012, The Journal of Physical Chemistry A, 116, 4801, doi: 10.1021/jp302096v
Linstrom, P., & Mallard, W. 2024, NIST chemistry WebBook, NIST standard reference database number 69. https://doi.org/10.18434/T4D303
Loomis, R. A., Burkhardt, A. M., Shingledecker, C. N., et al. 2021, Nature Astronomy, 5, 188, doi: 10.1038/s41550-020-01261-4
Loru, D., Cabezas, C., Cernicharo, J., Schnell, M., & Steber, A. L. 2023, Astronomy & Astrophysics, 677, A166, doi: 10.1051/0004-6361/202347023
Lourderaj, U., & Hase, W. L. 2009, The Journal of Physical Chemistry A, 113, 2236, doi: 10.1021/jp806659f
Léger, A., & Puget, J. L. 1984, Astronomy & Astrophysics, 500, 279. https: //ui.adsabs.harvard.edu/1984A&A…137L…5L/abstract
Malloci, G., Mulas, G., Cecchi-Pestellini, C., & Joblin, C. 2008, Astronomy & Astrophysics, 489, 1183, doi: 10.1051/0004-6361:200810177
McCarthy, M. C., Lee, K. L. K., Loomis, R. A., et al. 2021, Nature Astronomy, 5, 176, doi: 10.1038/s41550-020-01213-y
McGuire, B. A., Xue, C., Lee, K. L. K., El-Abd, S., & Loomis, R. A. 2024, molsim, v0.5.0, Zenodo, doi: 10.5281/zenodo. 12697227
McGuire, B. A., Burkhardt, A. M., Loomis, R. A., et al. 2020, The Astrophysical Journal, 900, L10, doi: 10.3847/2041-8213/aba632
McGuire, B. A., Loomis, R. A., Burkhardt, A. M., et al. 2021, Science, 371, 1265, doi: 10.1126/science.abb7535
McNaughton, D., Jahn, M. K., Travers, M. J., et al. 2018, Monthly Notices of the Royal Astronomical Society, 476, 5268, doi: 10.1093/mnras/sty557
Mennella, V., Hornekær, L., Thrower, J., & Accolla, M. 2012, The Astrophysical Journal Letters, 745, L2, doi: 10.1088/2041-8205/745/1/L2
Miller, W. H. 1979, Journal of the American Chemical Society, 101, 6810, doi: 10.1021/ja00517a004
Neeman, E. M., Lesarri, A., & Bermúdez, C. 2025, ChemPhysChem, in press, e202401012, doi: 10.1002/cphc. 202401012
Neese, F. 2022, WIREs Computational Molecular Science, 12, e1606, doi: 10.1002/wcms. 1606
Oomens, J., Sartakov, B. G., Tielens, A. G. G. M., Meijer, G., & Helden, G. v. 2001, The Astrophysical Journal, 560, L99, doi: 10.1086/324170
Pathak, A., & Sarre, P. J. 2008, Monthly Notices of the Royal Astronomical Society: Letters, 391, L10, doi: 10.1111/j.1745-3933.2008.00544.x
Perdew, J. P. 1986, Physical Review B, 33, 8822, doi: 10.1103/PhysRevB. 33.8822
Pickett, H. M. 1991, Journal of Molecular Spectroscopy, 148, 371, doi: 10.1016/0022-2852(91)90393-O
Pinski, P., Riplinger, C., Valeev, E. F., & Neese, F. 2015, The Journal of Chemical Physics, 143, 034108, doi: 10.1063/1.4926879
Rauls, E., & Hornekær, L. 2008, The Astrophysical Journal, 679, 531, doi: 10.1086/587614
Reizer, E., Viskolcz, B., & Fiser, B. 2022, Chemosphere, 291, 132793, doi: 10.1016/j.chemosphere.2021.132793
Riplinger, C., Pinski, P., Becker, U., Valeev, E. F., & Neese, F. 2016, The Journal of Chemical Physics, 144, 024109, doi: 10.1063/1.4939030
Sabbah, H., Bonnamy, A., Papanastasiou, D., et al. 2017, The Astrophysical Journal, 843, 34, doi: 10.3847/1538-4357/aa73dd
Sabbah, H., Quitté, G., Demyk, K., & Joblin, C. 2024, Natural Sciences, 4, e20240010, doi: 10.1002/ntls. 20240010
Sephton, M. A., Love, G. D., Watson, J. S., et al. 2004, Geochimica et Cosmochimica Acta, 68, 1385, doi: 10.1016/j.gca.2003.08.019
Siebert, M. A., Lee, K. L. K., Remijan, A. J., et al. 2022, The Astrophysical Journal, 924, 21, doi: 10.3847/1538-4357/ac3238
Sita, M. L., Changala, P. B., Xue, C., et al. 2022, The Astrophysical Journal, 938, L12, doi: 10.3847/2041-8213/ac92f4
Stein, S. 1978, The Journal of Physical Chemistry, 82, 566, doi: 10.1021/j100494a600
Stockett, M. H., Subramani, A., Liu, C., et al. 2025, Dissociation and radiative stabilization of the indene cation: The nature of the C-H bond and astrochemical implications. https://arxiv.org/abs/2503.20686
Thrower, J. D., Jørgensen, B., Friis, E. E., et al. 2012, The Astrophysical Journal, 752, 3, doi: 10.1088/0004-637X/752/1/3
Tielens, A. G. G. M. 2008, Annual Review of Astronomy and Astrophysics, 46, 289, doi: 10.1146/annurev.astro.46.060407.145211
Useli-Bacchitta, F., Bonnamy, A., Mulas, G., et al. 2010, Chemical Physics, 371, 16, doi: 10.1016/j.chemphys.2010.03.012
Weigend, F., & Ahlrichs, R. 2005, Physical Chemistry Chemical Physics, 7, 3297, doi: 10.1039/B508541A
Wenzel, G., Cooke, I. R., Changala, P. B., et al. 2024, Science, 386, 810, doi: 10.1126/science.adq6391
Wenzel, G., Speak, T. H., Changala, P. B., et al. 2025, Nature Astronomy, 9, 262, doi: 10.1038/s41550-024-02410-9
West, N. A., Millar, T. J., Van de Sande, M., et al. 2019, The Astrophysical Journal, 885, 134, doi: 10.3847/1538-4357/ab480e
Xue, C. 2024, GBT Spectral Line Reduction Pipeline. https://github.com/cixue/gotham-spectral-pipeline
Zeichner, S. S., Aponte, J. C., Bhattacharjee, S., et al. 2023, Science, 382, 1411, doi: 10.1126/science.adg6304
Zhao, L., Kaiser, R. I., Xu, B., et al. 2018, Nature Astronomy, 2, 413, doi: 10.1038/s41550-018-0399-y
Zhen, J., Rodriguez Castillo, S., Joblin, C., et al. 2016, The Astrophysical Journal, 822, 113, doi: 10.3847/0004-637X/822/2/113
APPENDIX
A. FULL SYNTHESIS ROUTE TO CYANOCORONENE

A.1. Synthesis of Formylcoronene
- The reaction will release HCl gas during heating. Caution is advised.
- The reaction did not show improvement in yield after doubling the equivalence of
and . However, most of the starting material is recoverable. - The product and unreacted starting material are both poorly soluble in a wide range of organic solvents. As such, copious amounts (potentially exceeding 6 L ) of DCM are required to perform chromatography at the scale


A.2. Synthesis of Formylcoronene-Oxime
- The reaction mixture is heterogeneous and can stick on the walls of the vessel if stirred too violently, thus leading to incomplete reaction. Slow stirring is preferred.
A.3. Synthesis of Cyanocoronene

- Direct conversion of formylcoronene to cyanocoronene according to literature protocol (Hyodo et al. 2017) is difficult due to the limited reactivity of formylcoronene at room temperature. Noticeable conversion is only reliably achieved in refluxing toluene, chlorobenzene, or mesitylene. However, the acidic reaction conditions combined with high temperatures frequently resulted in significant degradation of the starting material and severely decreased yields.
- The O-sulfonyl oxime intermediate is sensitive to hydrolysis. Its isolation is not recommended.
- The reaction mixture is heterogeneous and can stick on the walls of the vessel if stirred too violently, thus leading to incomplete reaction. Slow stirring is preferred.
- Copious amounts (
of DCM) were required to complete the chromatography due to the low solubility of the product. Precipitation-induced clogging can be mitigated by gently disturbing the top of the column.
B. BENCHMARK OF LEVEL OF THEORY
| Parameter | 1-cyanopyrene | ||
| Theoretical | Experimental
|
Theoretical+Experimental
|
|
|
|
850.141 | 843.140191(128) | 843.141827(128) |
|
|
372.931 | 372.500175(56) | 372.500183(56) |
|
|
259.219 | 258.4249175(164) | 258.4248913(164) |
|
|
1.977 | 2.240(80) | 2.153(80)) |
|
|
-5.556 | -5.52(101) | -5.88(101) |
|
|
20.310 | [0] | [20.310] |
|
|
0.724 | 0.826(40) | 0.795(40) |
|
|
3.059 | 5.26(74) | 4.20(74) |
| Parameter | 2-cyanopyrene | ||
| Theoretical | Experimental
|
Theoretical+Experimental
|
|
|
|
1015.239 | 1009.19382(60) | 1009.19356(39) |
|
|
314.479 | 313.1345299(202) | 313.1345270(195) |
|
|
240.105 | 239.0427225(184) | 239.0427270(167) |
|
|
0.706 | 0.7008(109) | 0.7023(106) |
|
|
5.375 | 5.814(94) | 5.818(94) |
|
|
8.785 | 15.3(114) | [8.785] |
|
|
0.184 | 0.1759(60) | 0.1766(59) |
|
|
4.510 | 4.22(39) | 4.12(35) |
| Parameter | 4-cyanopyrene | ||
| Theoretical | Experimental
|
Theoretical+Experimental
|
|
|
|
652.155 | 651.383034(69) | 651.382955(64) |
|
|
456.670 | 453.731352(45) | 453.731444(41) |
|
|
268.590 | 267.5078168(224) | 267.5078004(221) |
|
|
1.893 | 1.780(98) | 2.026(69) |
|
|
-1.553 | 0.43(58) | [-1.553] |
|
|
14.821 | 10.89(73) | 12.61(53) |
|
|
0.756 | 0.677(49) | 0.803(35) |
|
|
1.971 | 2.56(33) | 2.40(33) |
C. MEASURED LINES OF CYANOCORONENE
| Transition (
|
Frequency
|
|
|
6788.4098 |
|
|
6788.4098 |
|
|
6788.4443 |
|
|
6788.4443 |
|
|
6788.7145 |
|
|
6788.7145 |
|
|
6789.9187 |
|
|
6789.9187 |
|
|
6815.8858 |
|
|
7005.2518 |
|
|
7054.6106 |
|
|
7054.6106 |
|
|
7054.6617 |
|
|
7054.6617 |
|
|
7054.8759 |
|
|
7054.8759 |
|
|
7055.9209 |
|
|
7055.9209 |
|
|
7058.7857 |
|
|
7058.7857 |
|
|
7073.0418 |
|
|
7080.6353 |
|
|
7088.6004 |
|
|
7291.4710 |
|
|
7320.8179 |
|
|
7320.8179 |
|
|
7320.8780 |
|
|
7320.8780 |
|
|
7321.0420 |
|
|
7321.0420 |
|
|
7321.9574 |
|
|
7321.9574 |
|
|
7324.4393 |
|
|
7324.4393 |
| Transition (
|
Frequency
|
|
|
7587.0283 |
|
|
7587.0283 |
|
|
7587.0875 |
|
|
7587.0875 |
|
|
8377.6038 |
|
|
8385.6505 |
|
|
8385.6505 |
|
|
8385.7347 |
|
|
8385.7347 |
|
|
8385.7636 |
|
|
8385.7636 |
|
|
8391.1806 |
|
|
8391.1806 |
|
|
8651.8594 |
|
|
8651.8594 |
|
|
8651.9466 |
|
|
8651.9466 |
|
|
8651.9537 |
|
|
8651.9537 |
|
|
8652.4539 |
|
|
8652.4539 |
|
|
8653.7843 |
|
|
8653.7843 |
|
|
8656.7527 |
|
|
8656.7527 |
|
|
10515.3437 |
|
|
10515.3437 |
|
|
10515.3437 |
|
|
10515.3437 |
|
|
10515.4529 |
|
|
10515.4529 |
|
|
10516.2356 |
|
|
10516.2356 |
|
|
10517.6703 |
|
|
10517.6703 |
|
|
10520.4313 |
|
|
10520.4313 |

D. PARTITION FUNCTION FOR CYANOCORONENE
| Temperature [K] | Partition function |
| 1.0 | 1703.7230 |
| 2.0 | 4813.7245 |
| 3.0 | 8840.2413 |
| 4.0 | 13608.0333 |
| 5.0 | 19015.7897 |
| 6.0 | 24995.1437 |
| 7.0 | 31495.9011 |
| 8.0 | 38479.1687 |
| 9.375 | 48812.4929 |
| 18.75 | 138047.6140 |
| 37.5 | 390439.4924 |
| 75.0 | 1104317.3292 |
| 150.0 | 3120078.8657 |
| 225.0 | 5686759.1241 |
| 300.0 | 8589526.6725 |
| 400.0 | 12678742.2060 |
| 500.0 | 16744897.1786 |
E. MCMC ANALYSIS OF CYANOCORONENE IN TMC-1
| Component No. |
|
Size (“) |
|
|
|
| 1 |
|
||||
| 2 |
|
|
|
|
|
| 3 |
|
||||
| 4 |
|
||||
| Min | 0.0 | 1 | 10.0 | 3.0 | 0.1 |
| Max | 10.0 | 100 | 13.0 | 15.0 | 0.3 |
| Component No. |
|
Size (“) |
|
|
|
| 1 |
|
50 |
|
|
|
| 2 |
|
50 |
|
||
| 3 |
|
50 |
|
||
| 4 |
|
49 |
|
||
|
|
|||||

F. COLUMN DENSITIES OF CYCLIC HYDROCARBONS IN TMC-1
| Molecule |
|
Column Density (
|
Reference |
|
|
5 |
|
Cernicharo et al. (2021a) |
|
|
6 |
|
Cernicharo et al. (2021b) |
|
|
6 |
|
Lee et al. (2021) |
|
|
6 |
|
Lee et al. (2021) |
|
|
7 |
|
Cernicharo et al. (2021c) |
|
|
7 |
|
Cernicharo et al. (2021c) |
|
|
7 |
|
Cernicharo et al. (2022) |
|
|
7 |
|
McGuire et al. (2021) |
|
|
8 |
|
Loru et al. (2023) |
|
|
9 |
|
Sita et al. (2022) |
|
|
10 |
|
Sita et al. (2022) |
|
|
11 |
|
McGuire et al. (2021) |
|
|
11 |
|
McGuire et al. (2021) |
|
|
13 |
|
Cernicharo et al. (2024) |
|
|
13 |
|
Cernicharo et al. (2024) |
|
|
17 |
|
Wenzel et al. (2024) |
|
|
17 |
|
Wenzel et al. (2025) |
|
|
17 |
|
Wenzel et al. (2025) |
|
|
16 |
|
Wenzel et al. (2025) |
|
|
25 |
|
This work |
|
|
24 |
|
This work |
G. AB-INITIO QUANTUM CHEMICAL CALCULATIONS
G.1. Computational Methodology
bonds. In these scans, all coordinates except the bond being scanned were allowed to relax while the scanned coordinate was varied. The resultant maxima were used as input geometries for transition state optimizations and the long-range minima prior to CN addition were optimized to a loose bound complex on the entrance channel.

G.2. Master equation kinetic predictions
| 1-1 | 1-2 | 1-3 | 1-4 | 1-5 | 2-1 | 2-2 | 2-3 | 2-4 | 2-5 | |
| CN + Coronene | 0.0 | 0.00 | 0.0 | 0.0 | 0.0 | 0.0 | 0.00 | 0.0 | 0.0 | 0.0 |
| VdW | -20.57 | -20.26 | -25.82 | * | * | * | ||||
| TS 1 (CN addition) | 9.87 | 14.42 | 3.83 | 21.48 | 25.03 | 13.18 | ||||
| N-Adduct 1 | -98.48 | -90.90 | -98.57 | -99.08 | -91.60 | -101.41 | ||||
| TS 3 H elimination | 36.35 | 42.57 | 33.38 | 38.55 | 45.37 | 34.23 | ||||
| H + Isocyanocoronene | 1.06 | 0.14 | 1.72 | 1.12 | -16.20 | 0.33 | -0.68 | 0.20 | 0.94 | -14.17 |
| TS 2 (NC addition) | -18.57 | -18.27 | -23.82 | -20.09 | -18.52 | -25.05 | ||||
| Adduct 1 | -186.80 | -179.23 | -184.50 | -186.68 | -179.22 | -186.00 | ||||
| TS 4 H elimination | -56.87 | -50.57 | -57.91 | -53.20 | -46.27 | -54.98 | ||||
| H + Cyanocoronene | -89.15 | -89.97 | -86.33 | -89.88 | -106.47 | -89.39 | -90.31 | -86.53 | -88.90 | -103.67 |

https://greenbankobservatory.org/portal/gbt/ gbt-legacy-archive/gotham-data/ Experimental uncertainties are 2 kHz . - *Estimated using the cyanopyrene and cyanocoronene column densities, calculated rate coefficients for CN addition, and an CN/H ratio of 0.15 (see Appendix G and Wenzel et al. 2025).
