DOI: https://doi.org/10.1038/s41590-024-02062-x
PMID: https://pubmed.ncbi.nlm.nih.gov/39806065
تاريخ النشر: 2025-01-13
الأدوار التفاضلية لخلايا T التنظيمية البشرية CD4+ و CD8+ في التحكم في الاستجابات المناعية الذاتية التفاعلية
تم القبول: 10 ديسمبر 2024
نُشر على الإنترنت: 13 يناير 2025
تحقق من التحديثات
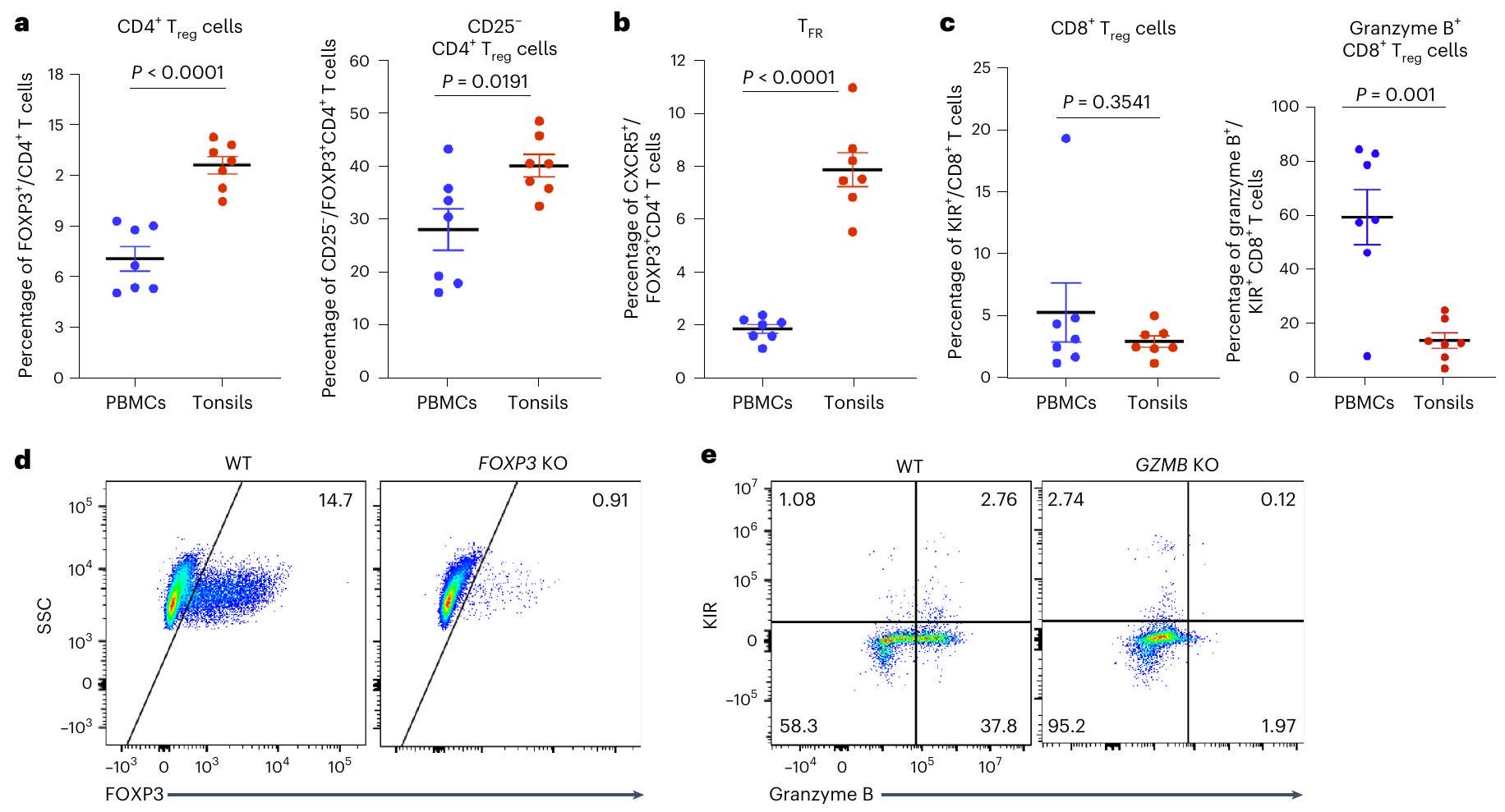
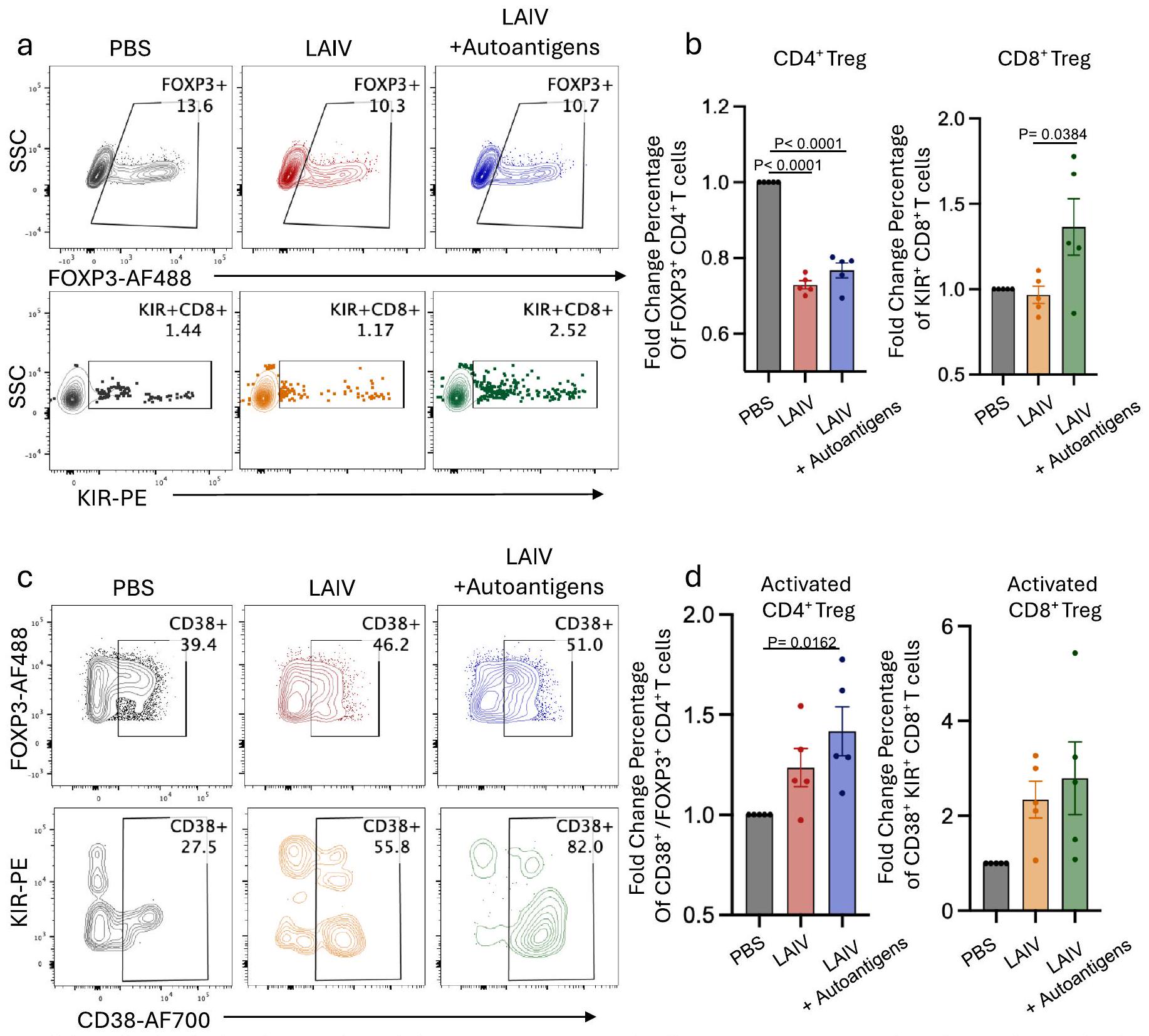
مخططات FACS التمثيلية لتعبير FOXP3 في خلايا CD4+ T (د) وتعبير KIR وجرانزيم B في CD8
وظائفهم وقاموا بقياس تأثيراتهم على التفاعلات الذاتية
كما تُظهر أيضًا أننا يمكننا نمذجة الميزات الرئيسية لكيفية التحكم في خلايا B و T الذاتية التفاعل، وبشكل أوسع، اختبار الفرضيات بسرعة وتحديد الآليات في نظام إنساني بحت.
النتائج
إزالة الجينات بكفاءة باستخدام Cas9-RNPs
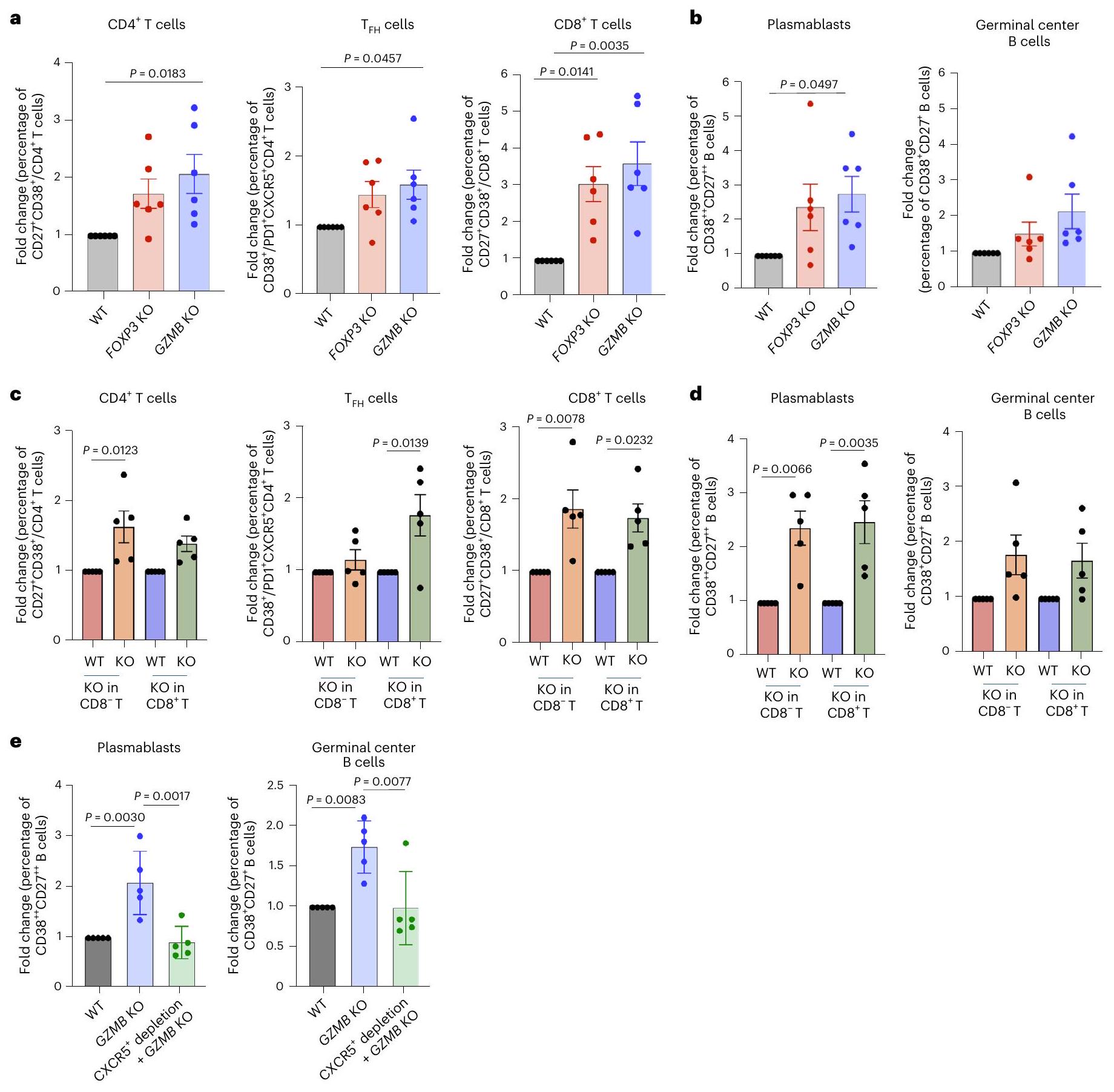
وظيفة كبح CD4
تم استخدامها كعنصر تحكم لتوليد خلايا T من النوع البري (WT). لتجنب احتمال تأثير الخرزات المرفقة على وظيفة خلايا تقديم المستضد (على سبيل المثال، خلايا B والخلايا النخاعية)، قمنا بتنقية الخلايا السلبية عن CD3 بشكل منفصل من قنينة جديدة من خلايا اللوزتين. تم عد الخلايا السلبية عن CD3 والخلايا الإيجابية عن CD3 التي تم إدخالها كهربائيًا، ودمجها وزرعها في الأطباق المتداخلة بكثافة

القدرة على البقاء وكفاءة KO من خلال قياس مستويات البروتين داخل الخلايا عبر تحليل تدفق الخلايا. حافظت خلايا T من ثقافات WT و KO على قدرة جيدة على البقاء (
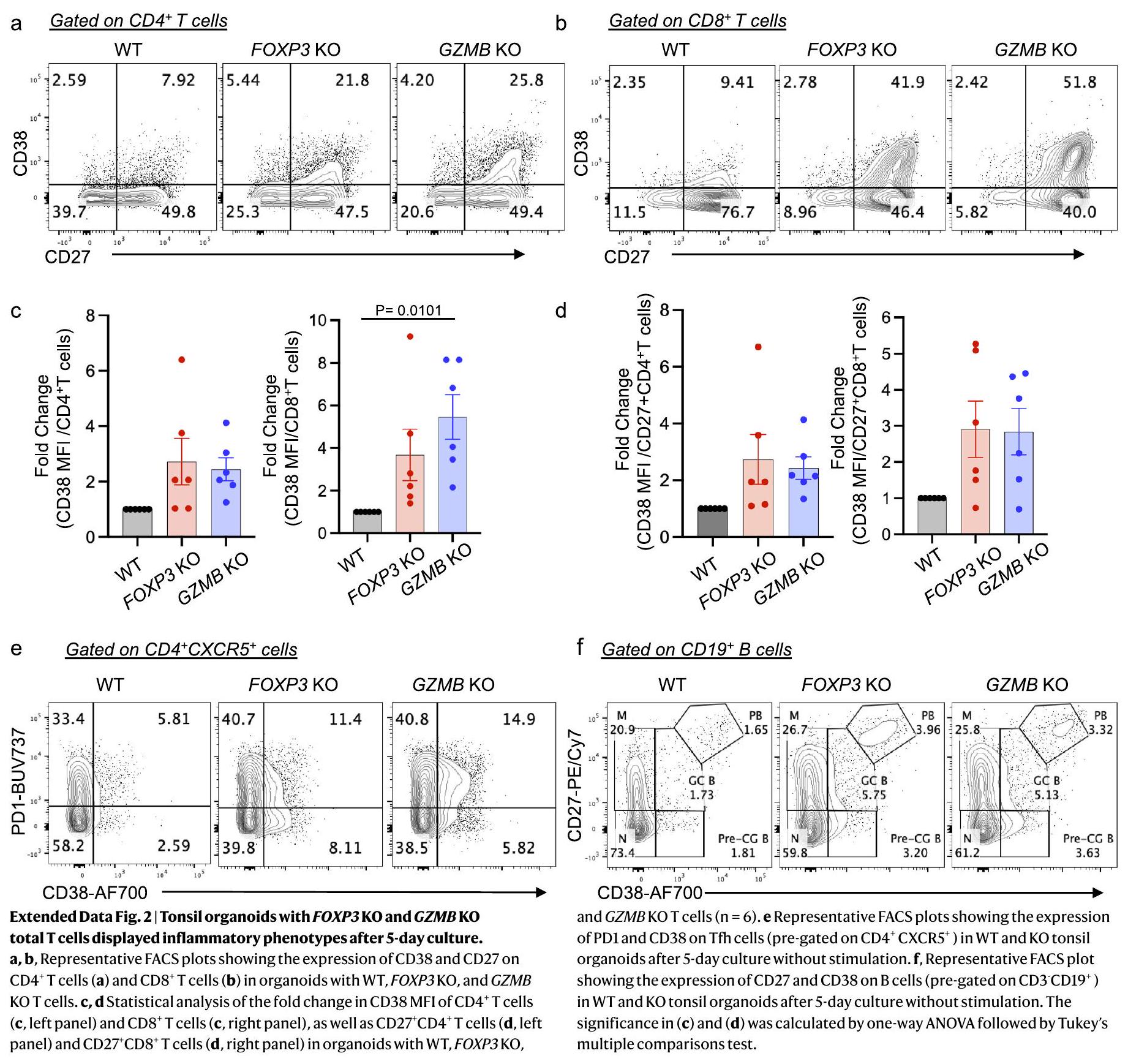
أعضاء اللوزتين العضوية KO تظهر أنماط التهابية
عبر إنزيم غرانزيم ب على خلايا T الذاتية التفاعل
إنتاج الأجسام المضادة الذاتية التفاضلية في عضيات اللوزتين KO
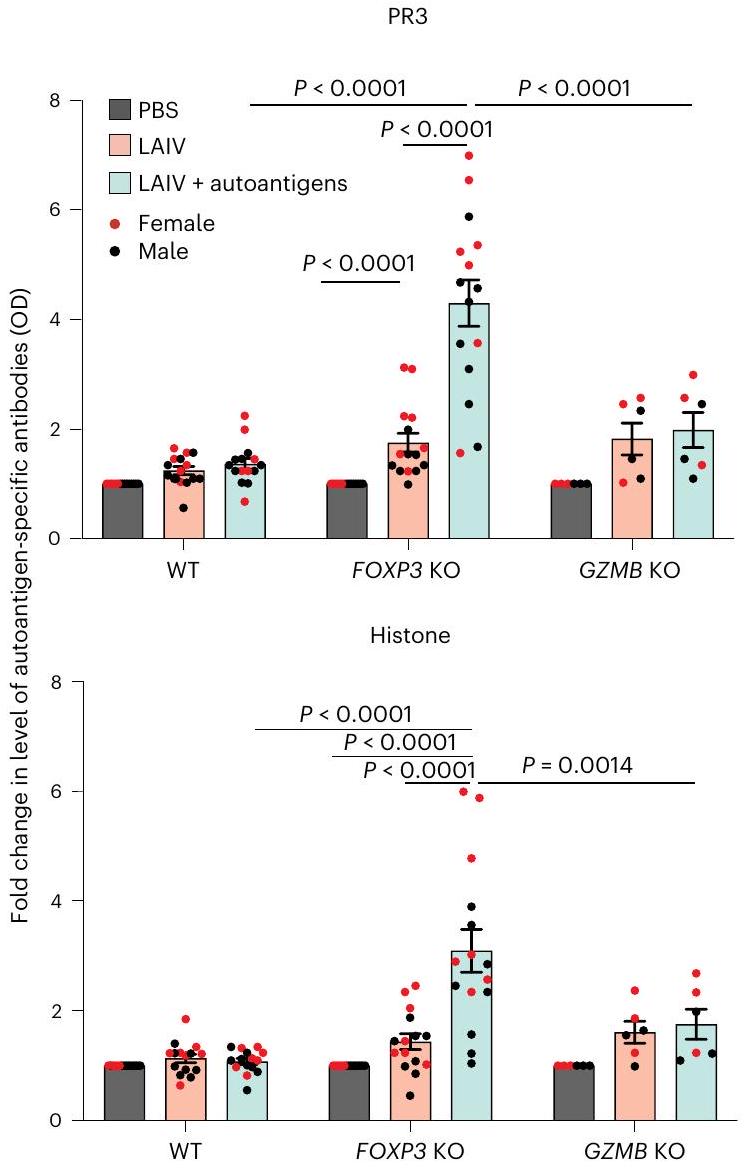
بين ظروف التحفيز و PBS في اللوزتين مع خلايا T من النوع البري، FOXP3 KO و GZMB KO بعد 7 أيام من التحفيز
إنتاج مقارنة مع الأعضاء العضلية اللوزية WT، حتى مع إضافة الأوتوأنجين إلى الثقافة (الشكل البياني الممتد 5). الدراسات السابقة اقترحت أن العدوى الفيروسية قد تكون عاملاً رئيسياً في بدء الأمراض المناعية الذاتية.
توسعت خلايا B الذاتية التفاعل في الأعضاء العضوية KO FOXP3 بعد التحفيز
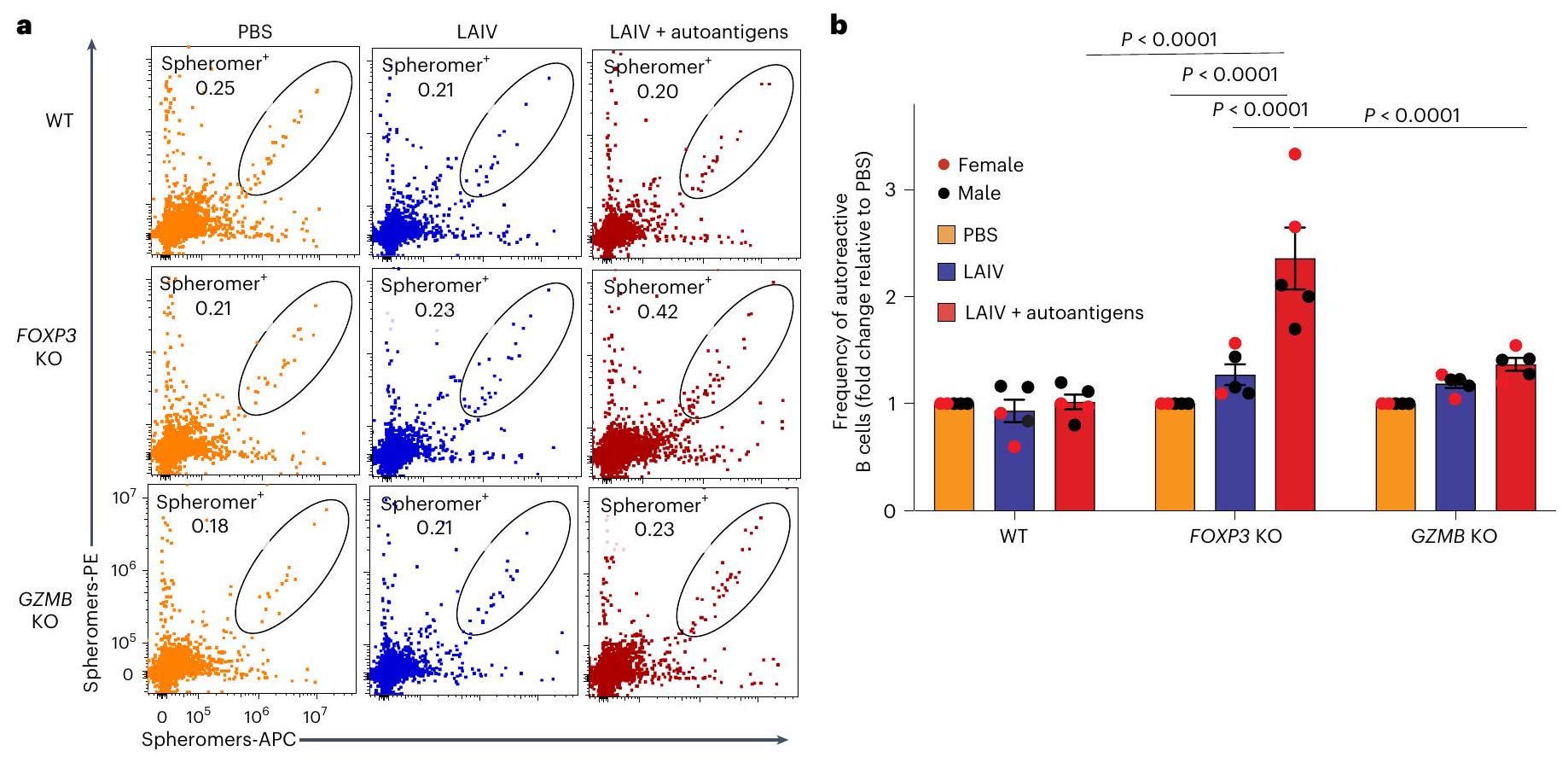
استهداف الأوتوأنجين PR3 و snRNP-C و core histone. في وجود LAIV، حفز كوكتيل الأوتوأنجين بشكل عميق توسيع خلايا B المحددة للأنتيجين الذاتي في عضيات اللوزتين FOXP3 KO (الشكل 4a، b)، بما يتماشى مع مستويات الأجسام المضادة الذاتية الملحوظة. ومن الجدير بالذكر أن أعلى اثنين من عضيات اللوزتين FOXP3KO التي أنتجت تكرارًا أعلى من خلايا B ذات النشاط الذاتي بعد تحفيز LAIV بالإضافة إلى الأوتوأنجين كانت أيضًا مستمدة من متبرعات إناث (الشكل 4b). بالمقابل، كان لإزالة GZMB في خلايا T اللوزية تأثير طفيف فقط على تكرارات خلايا B ذات النشاط الذاتي (الشكل 4a، b)، مما يؤكد أن CD4
استجابة خلايا T التلقائية التفاضلية في الأعضاء العضوية KO
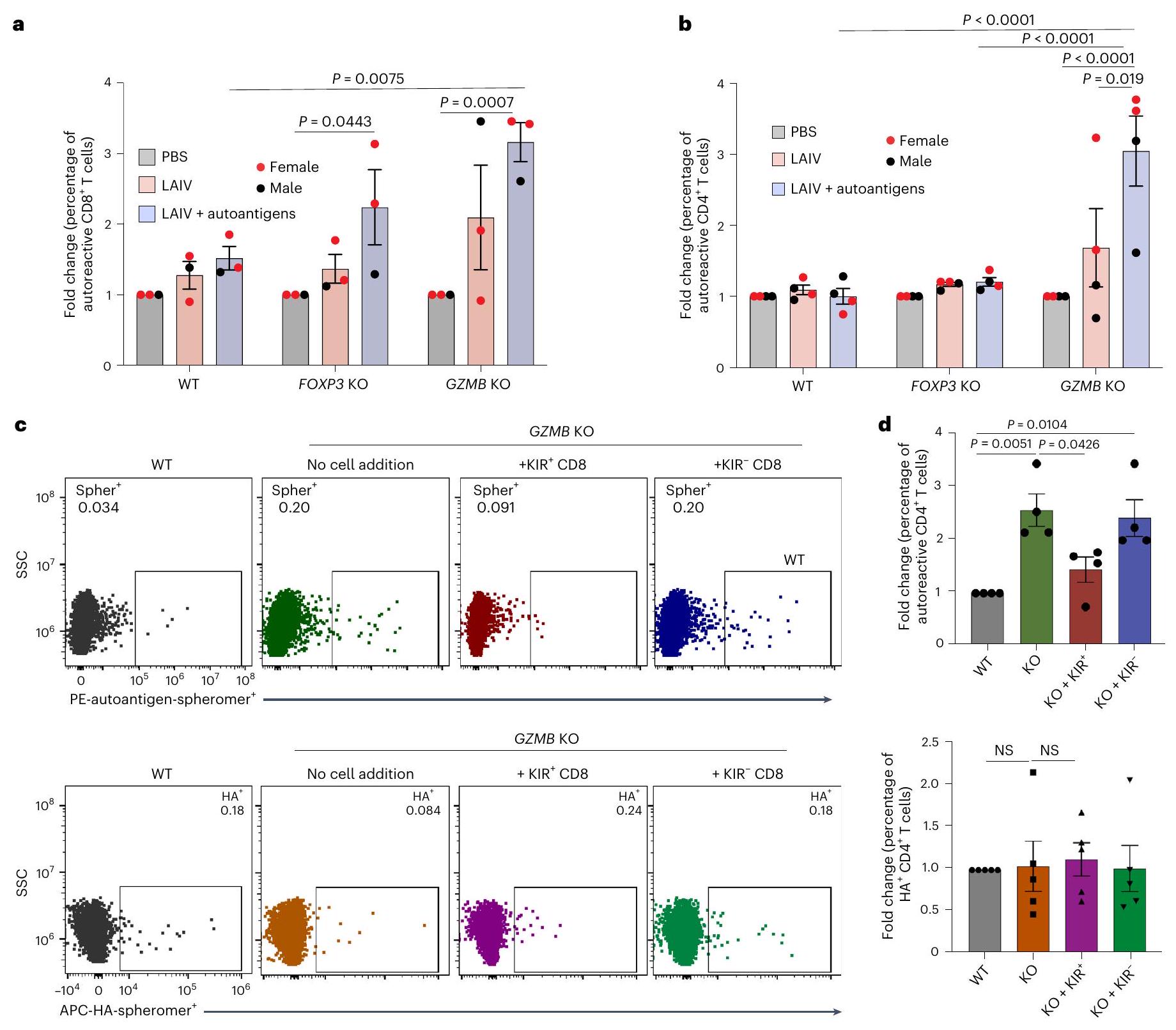
تم حساب الشرط.
لوحظت زيادة ذات دلالة إحصائية في
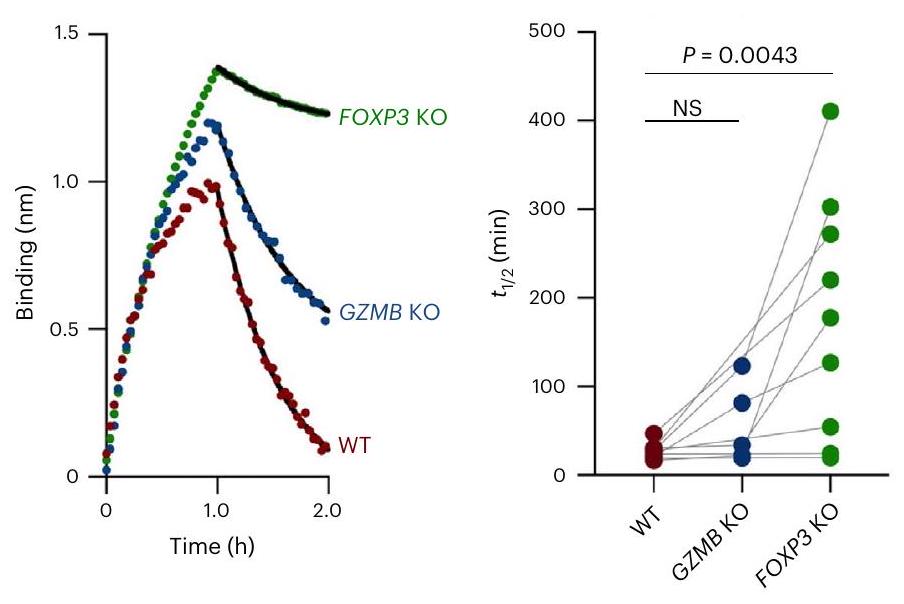
إزالة FOXP3 تعزز من قوة ارتباط الأجسام المضادة
زيادة النشاط الذاتي في الأعضاء العضوية من النساء مقارنة بالرجال
نقاش
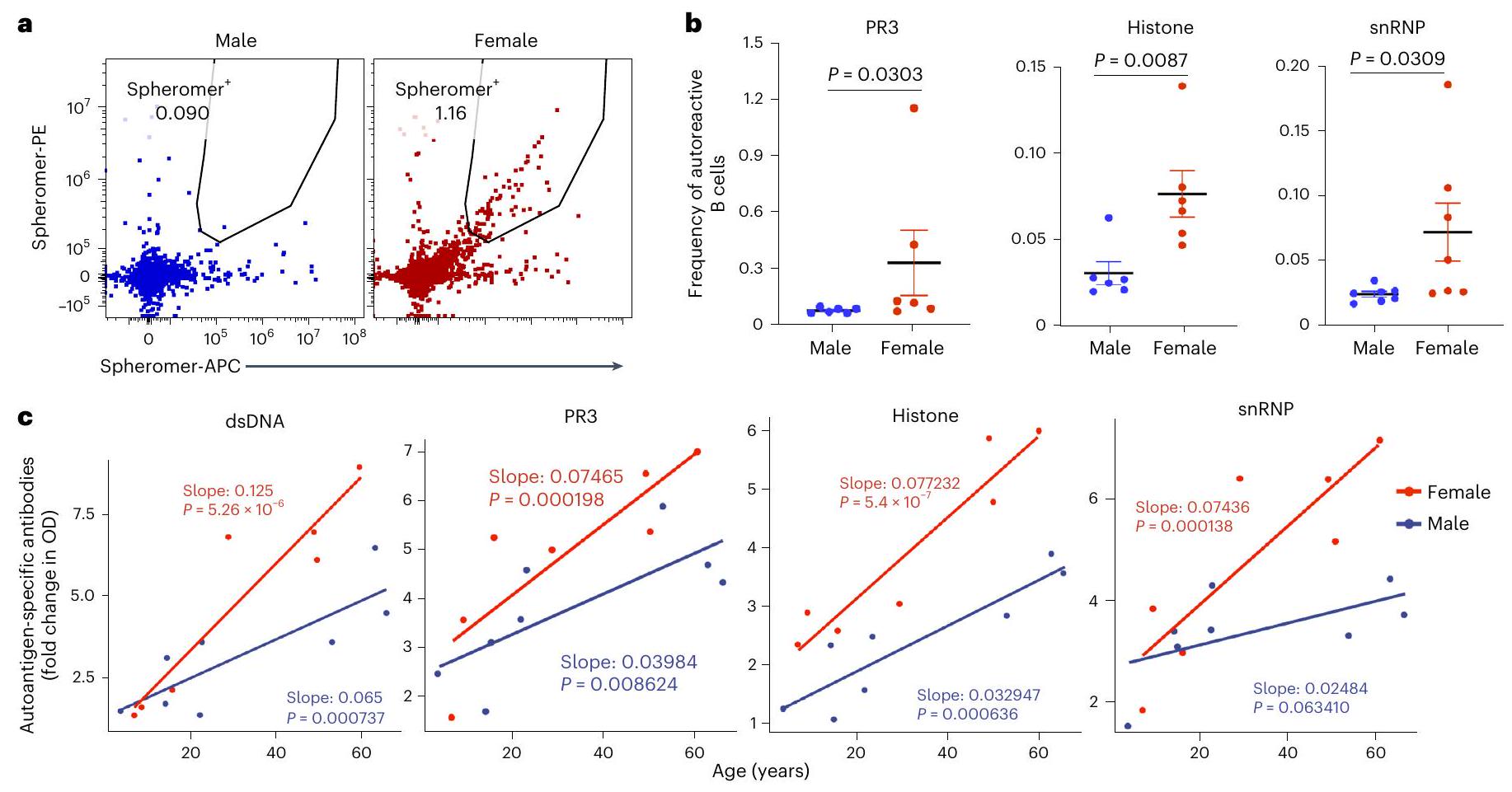
نموذج للتنبؤ بالعلاقات بين مستويات الأجسام المضادة الذاتية، والعمر، والجنس. تمثل معاملات نموذج الانحدار (الميل) تأثير العمر على المتغير التابع لكل جنس، مع
المحتوى عبر الإنترنت
References
- Valent, P. et al. Paul Ehrlich (1854-1915) and his contributions to the foundation and birth of translational medicine. J. Innate Immun. 8, 111-120 (2016).
- Goodnow, C. C. et al. Altered immunoglobulin expression and functional silencing of self-reactive B lymphocytes in transgenic mice. Nature 334, 676-682 (1988).
- Asano, M., Toda, M., Sakaguchi, N. & Sakaguchi, S. Autoimmune disease as a consequence of developmental abnormality of a T cell subpopulation. J. Exp. Med. 184, 387-396 (1996).
- Baecher-Allan, C. & Hafler, D. A. Human regulatory T cells and their role in autoimmune disease. Immunol. Rev. 212, 203-216 (2006).
- Jiang, H., Zhang, S. I. & Pernis, B. Role of CD8+ T cells in murine experimental allergic encephalomyelitis. Science 256, 1213-1215 (1992).
- Kim, H. J. et al. Stable inhibitory activity of regulatory T cells requires the transcription factor Helios. Science 350, 334-339 (2015).
- Kim, H. J., Verbinnen, B., Tang, X., Lu, L. & Cantor, H. Inhibition of follicular T-helper cells by CD8
regulatory T cells is essential for self tolerance. Nature 467, 328-332 (2010). - Li , J. et al.
cells suppress pathogenic T cells and are active in autoimmune diseases and COVID-19. Science 376, eabi9591 (2022). - Saligrama, N. et al. Opposing T cell responses in experimental autoimmune encephalomyelitis. Nature 572, 481-487 (2019).
- Wagar, L. E. et al. Modeling human adaptive immune responses with tonsil organoids. Nat. Med. 27, 125-135 (2021).
- Kastenschmidt, J. M. et al. Influenza vaccine format mediates distinct cellular and antibody responses in human immune organoids. Immunity 56, 1910-1926.e7 (2023).
- Hadaschik, E. N. et al. Regulatory T cell-deficient scurfy mice develop systemic autoimmune features resembling lupus-like disease. Arthritis Res. Ther. 17, 35 (2015).
- Tsuda, M. et al. The spectrum of autoantibodies in IPEX syndrome is broad and includes anti-mitochondrial autoantibodies. J. Autoimmun. 35, 265-268 (2010).
- Chang, S. E. et al. New-onset IgG autoantibodies in hospitalized patients with COVID-19. Nat. Commun. 12, 5417 (2021).
- Poulsen, T. R., Jensen, A., Haurum, J. S. & Andersen, P. S. Limits for antibody affinity maturation and repertoire diversification in hypervaccinated humans. J. Immunol. 187, 4229-4235 (2011).
- Choi, S. J. et al.
and NKG2A cells are distinct innate-like populations in humans. Cell Rep. 42, 112236 (2023). - Rubtsova, K., Marrack, P. & Rubtsov, A. V. Sexual dimorphism in autoimmunity. J. Clin. Invest. 125, 2187-2193 (2015).
- Dieckmann, D., Plottner, H., Berchtold, S., Berger, T. & Schuler, G. Ex vivo isolation and characterization of
cells with regulatory properties from human blood. J. Exp. Med. 193, 1303-1310 (2001). - Baecher-Allan, C. M. & Hafler, D. A. The purification and functional analysis of human CD4
regulatory T cells. Curr. Protoc. Immunol. 72, 7.4B.1-7.4B. 12 (2006). - Hori, S., Nomura, T. & Sakaguchi, S. Control of regulatory T cell development by the transcription factor Foxp3. Science https://doi.org/10.1126/science. 1079490 (2003).
- Salti, S. M. et al. Granzyme B regulates antiviral CD8+ T cell responses. J. Immunol. 187, 6301-6309 (2011).
- Li , J. et al.
cells suppress pathogenic T cells and are active in autoimmune diseases and COVID-19. Science https://doi. org/10.1126/science.abi9591 (2022). - Loebbermann, J. et al. Regulatory T cells expressing granzyme B play a critical role in controlling lung inflammation during acute viral infection. Mucosal Immunol. 5, 161-172 (2012).
- Ise, W. et al. T follicular helper cell-germinal center B cell interaction strength regulates entry into plasma cell or recycling germinal center cell fate. Immunity 48, 702-715.e4 (2018).
- Mintz, M. A. & Cyster, J. G. T follicular helper cells in germinal center B cell selection and lymphomagenesis. Immunol. Rev. 296, 48-61(2020).
- Shulman, Z. et al. T follicular helper cell dynamics in germinal centers. Science 341, 673-677 (2013).
- Getts, D. R., Chastain, E. M., Terry, R. L. & Miller, S. D. Virus infection, antiviral immunity, and autoimmunity. Immunol. Rev. 255, 197-209 (2013).
- Dieker, J. et al. Autoantibodies against modified histone peptides in SLE patients are associated with disease activity and lupus nephritis. PLoS ONE 11, e0165373 (2016).
- Kattah, N. H., Kattah, M. G. & Utz, P. J. The U1-snRNP complex: structural properties relating to autoimmune pathogenesis in rheumatic diseases. Immunol. Rev. 233, 126-145 (2010).
- Primo, V. C. et al. Anti-PR3 immune responses induce segmental and necrotizing glomerulonephritis. Clin. Exp. Immunol. 159, 327-337 (2010).
- Mallajosyula, V. et al. CD8
T cells specific for conserved coronavirus epitopes correlate with milder disease in patients with COVID-19. Sci. Immunol. https://doi.org/10.1126/sciimmunol.abg5669 (2021). - Yu, W. et al. Clonal deletion prunes but does not eliminate self-specific
CD8 T lymphocytes. Immunity 42, 929-941 (2015). - Nielen, M. M. et al. Antibodies to citrullinated human fibrinogen (ACF) have diagnostic and prognostic value in early arthritis. Ann. Rheum. Dis. 64, 1199-1204 (2005).
- Su, L. F., Kidd, B. A., Han, A., Kotzin, J. J. & Davis, M. M. Virus-specific CD4
memory-phenotype T cells are abundant in unexposed adults. Immunity 38, 373-383 (2013). - Yuan, J. et al. Safety and immunogenicity of a human and mouse gp100 DNA vaccine in a phase I trial of patients with melanoma. Cancer Immun. 9, 5 (2009).
- Zhang, L., Nakayama, M. & Eisenbarth, G. S. Insulin as an autoantigen in NOD/human diabetes. Curr. Opin. Immunol. 20, 111-118 (2008).
- Goronzy, J. J. & Weyand, C. M. Immune aging and autoimmunity. Cell. Mol. Life Sci. 69, 1615-1623 (2012).
- Whitacre, C. C. Sex differences in autoimmune disease. Nat. Immunol. 2, 777-780 (2001).
- Wardemann, H. et al. Predominant autoantibody production by early human B cell precursors. Science https://doi.org/10.1126/ science. 1086907 (2003).
- Fontenot, J. D., Gavin, M. A. & Rudensky, A. Y. Foxp3 programs the development and function of CD4
CD25 regulatory T cells. Nat. Immunol. 4, 330-336 (2003). - Kim, J. M. & Rudensky, A. The role of the transcription factor Foxp3 in the development of regulatory T cells. Immunol. Rev. 212, 86-98 (2006).
- Sakaguchi, S. Naturally arising Foxp3-expressing CD25
regulatory T cells in immunological tolerance to self and non-self. Nat. Immunol. 6, 345-352 (2005). - Yang, S., Fujikado, N., Kolodin, D., Benoist, C. & Mathis, D. Immune tolerance. Regulatory T cells generated early in life play a distinct role in maintaining self-tolerance. Science 348, 589-594 (2015).
- Zheng, Y. & Rudensky, A. Y. Foxp3 in control of the regulatory T cell lineage. Nat. Immunol. 8, 457-462 (2007).
- Hoshino, A. et al. Identification of autoantibodies using human proteome microarrays in patients with IPEX syndrome. Clin. Immunol. 203, 9-13 (2019).
- Kinnunen, T. et al. Accumulation of peripheral autoreactive B cells in the absence of functional human regulatory T cells. Blood 121, 1595-1603 (2013).
- McCarron, M. J. & Marie, J. C. TGF-beta prevents T follicular helper cell accumulation and B cell autoreactivity. J. Clin. Invest. 124, 4375-4386 (2014).
- Lim, H. W., Hillsamer, P., Banham, A. H. & Kim, C. H. Cutting edge: direct suppression of B cells by
regulatory T cells. J. Immunol. https://doi.org/10.4049/jimmunol.175.7.4180 (2005). - likuni, N., Lourenço, E. V., Hahn, B. H. & La, C. Cutting edge: regulatory T cells directly suppress B cells in systemic lupus erythematosus. J. Immunol. https://doi.org/10.4049/ jimmunol. 0901163 (2009).
- Lam, A. J. et al. Optimized CRISPR-mediated gene knockin reveals FOXP3-independent maintenance of human Treg identity. Cell Rep. 36, 109494 (2021).
- Zhang, W. et al. FOXP3 recognizes microsatellites and bridges DNA through multimerization. Nature 624, 433-441 (2023).
- Le Coz, C. et al. Human T follicular helper clones seed the germinal center-resident regulatory pool. Sci. Immunol. 8, eade8162 (2023).
- Davis, M. M. In praise of descriptive science: a breath of fresh AIRE. Cell 166, 530-531 (2016).
- Meyer, S. et al. AIRE-deficient patients harbor unique high-affinity disease-ameliorating autoantibodies. Cell 166, 582-595 (2016).
- Rabia, L. A., Desai, A. A., Jhajj, H. S. & Tessier, P. M. Understanding and overcoming trade-offs between antibody affinity, specificity, stability and solubility. Biochem. Eng. J. 137, 365-374 (2018).
- Suurmond, J. & Diamond, B. Autoantibodies in systemic autoimmune diseases: specificity and pathogenicity. J. Clin. Invest. 125, 2194-2202 (2015).
- Sundaresan, B., Shirafkan, F., Ripperger, K. & Rattay, K. The role of viral infections in the onset of autoimmune diseases. Viruses https://doi.org/10.3390/v15030782 (2023).
- Arbuckle, M. R. et al. Development of anti-dsDNA autoantibodies prior to clinical diagnosis of systemic lupus erythematosus. Scand. J. Immunol. 54, 211-219 (2001).
- Arbuckle, M. R. et al. Development of autoantibodies before the clinical onset of systemic lupus erythematosus. N. Engl. J. Med. 349, 1526-1533 (2003).
- Leslie, D., Lipsky, P. & Notkins, A. L. Autoantibodies as predictors of disease. J. Clin. Invest. 108, 1417-1422 (2001).
- Olsen, N. J., Okuda, D. T., Holers, V. M. & Karp, D. R. Editorial: understanding the concept of pre-clinical autoimmunity. Front. Immunol. 13, 983310 (2022).
(c) The Author(s) 2025
طرق
عينات بشرية ومعالجة اللوزتين
معالجة الدم
تجميع كاس9-RNP والكهربة
فرز الخلايا وتجميع الأعضاء العضوية
زراعة الخلايا والتحفيز
تدفق الخلايا
تبع ذلك صبغ باستخدام صبغة Aqua Zombie الحية/الميتة (ثيرمو فيشر) والأجسام المضادة ضد علامات السطح (
كشف الأجسام المضادة بواسطة اختبار الامتزاز المناعي المرتبط بالإنزيم
تعبير البروتين، التنقية والبيوتينيل
تجميع معقد الببتيد-MHC-سفيرومر ومعقد الأوتوانتيجين-سفيرومر
تمت مزج أحادية pMHC-I (من مرفق نسيج NIH) أو الأوتوأنتيجينات (التي تم إنتاجها داخليًا) مع
قياس affinity الربط
التحليل الإحصائي
ملخص التقرير
توفر البيانات
توفر الشيفرة
شكر وتقدير
مساهمات المؤلفين
المصالح المتنافسة
معلومات إضافية
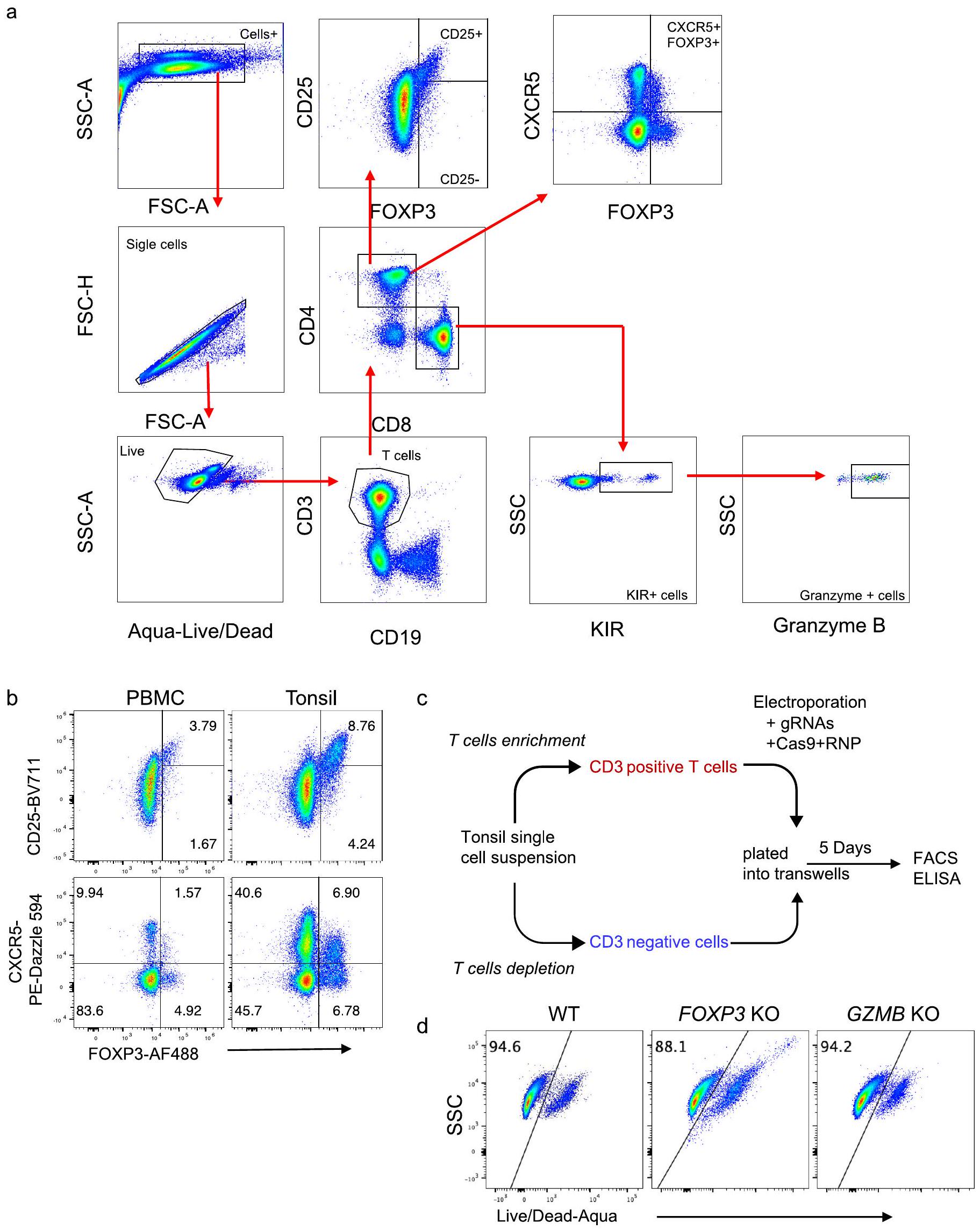
في عينات PBMC واللوزتين. ج، سير عمل لإنشاء عضيات لوزية معدلة وراثيًا باستخدام Cas9-RNPs. د، ملف FACS تمثيلي يظهر صبغة Live/Dead لخلايا T من عضيات اللوزتين WT وFOXP3 KO وGZMB KO.
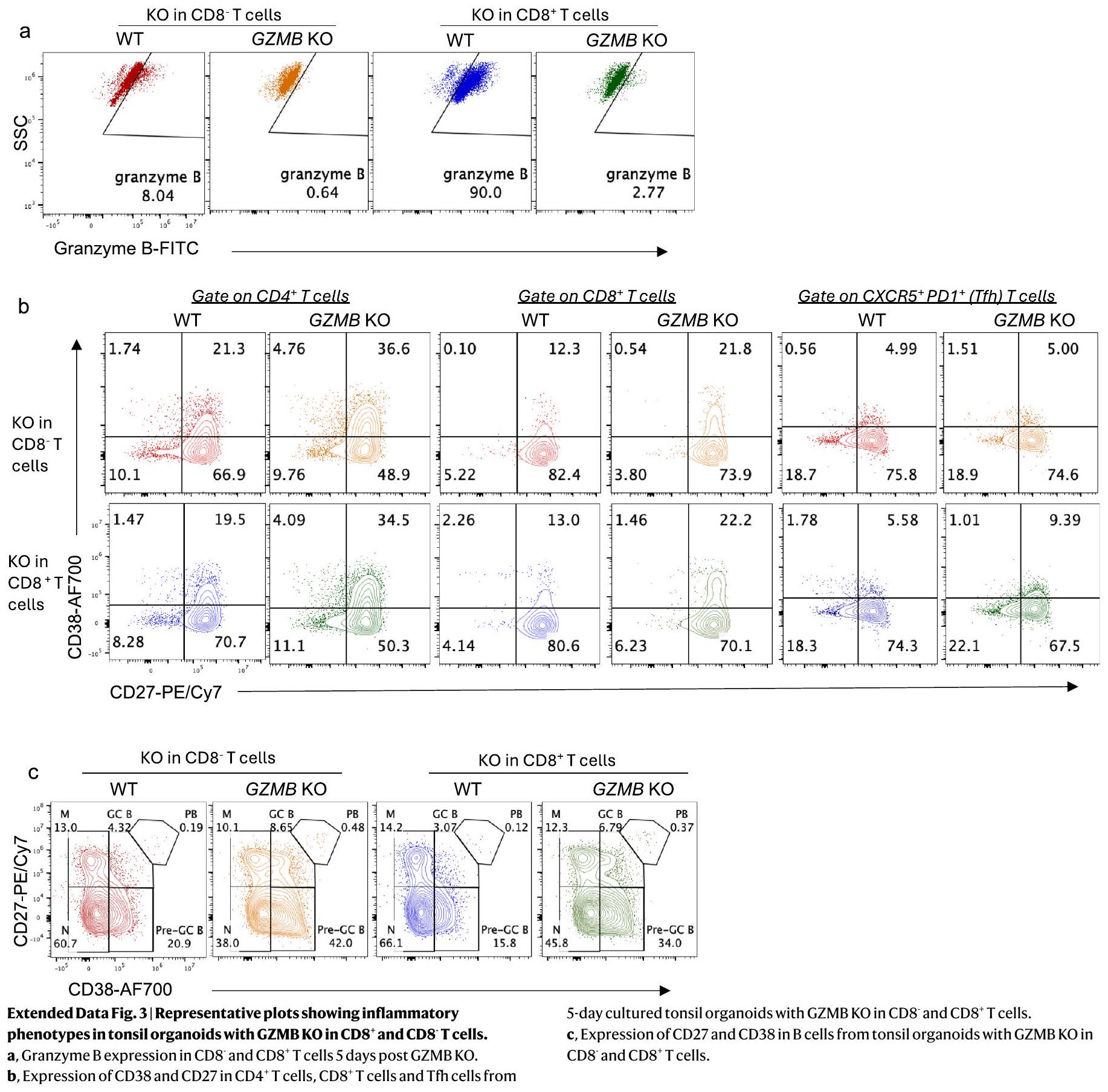
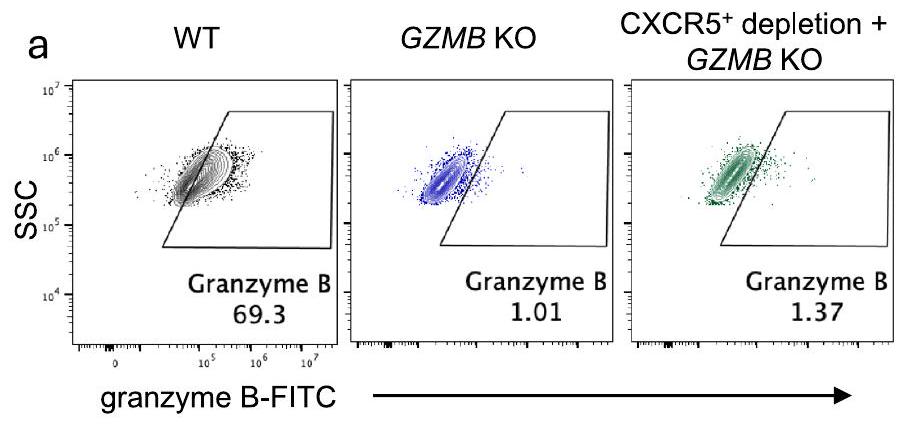


الشروط المشار إليها من الأعضاء العضلية لللوزتين. ج، تعبير CD27 و CD38 في خلايا B من الأعضاء العضلية لللوزتين مع WT و GZMB KO و GZMB KO المستنفد من CXCR5
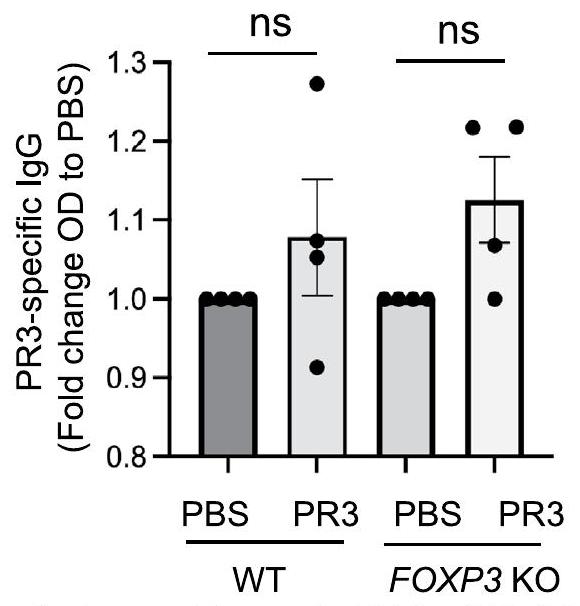
بواسطة إليسا (
الملخص
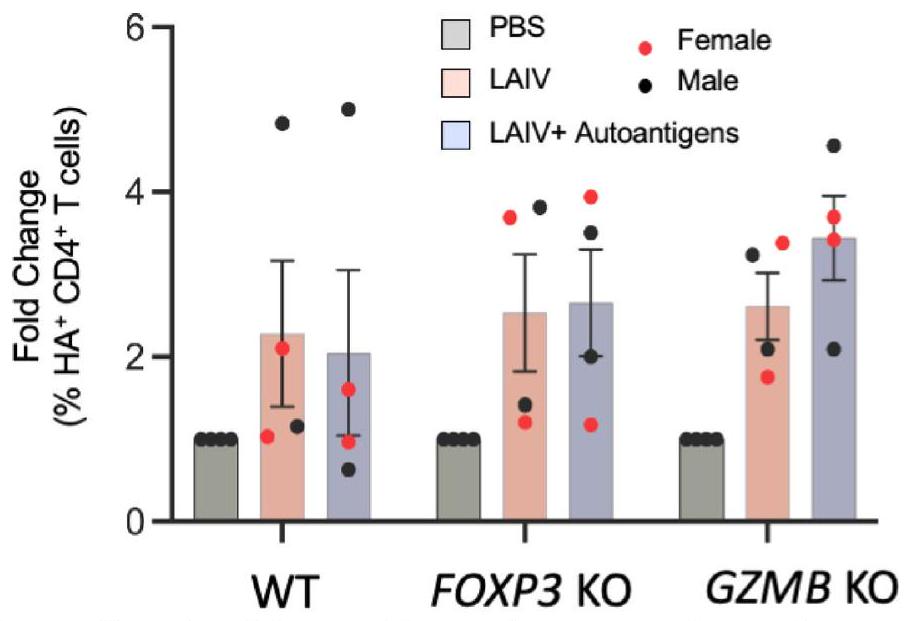
الشكل البياني الموسع 7 | نسبة الأجسام المضادة المحددة لـ HA
محفظة الطبيعة
| المؤلف(المؤلفون) المراسلون: | مارك م. ديفيس |
| آخر تحديث بواسطة المؤلفين: 2024/12/05 |
ملخص التقرير
الإحصائيات
غير متوفر
تم التأكيد
□ X
حجم العينة بالضبط
□
□ بيان حول ما إذا كانت القياسات قد أُخذت من عينات متميزة أو ما إذا كانت نفس العينة قد تم قياسها عدة مرات
□ X
اختبار(ات) الإحصاء المستخدمة وما إذا كانت أحادية الجانب أو ثنائية الجانب
يجب أن تُوصف الاختبارات الشائعة فقط بالاسم؛ واصفًا التقنيات الأكثر تعقيدًا في قسم الطرق.

□ وصف لجميع المتغيرات المرافقة التي تم اختبارها
□ X
وصف لأي افتراضات أو تصحيحات، مثل اختبارات الطبيعية والتعديل للمقارنات المتعددة
□

□ X
لاختبار الفرضية الصفرية، إحصائية الاختبار (على سبيل المثال،
□ لتحليل بايزي، معلومات حول اختيار القيم الأولية وإعدادات سلسلة ماركوف مونت كارلو
□ لتصميمات هرمية ومعقدة، تحديد المستوى المناسب للاختبارات والتقارير الكاملة عن النتائج
□ تقديرات أحجام التأثير (مثل حجم تأثير كوهين)
تحتوي مجموعتنا على الإنترنت حول الإحصائيات لعلماء الأحياء على مقالات تتناول العديد من النقاط المذكورة أعلاه.
البرمجيات والشيفرة
جمع البيانات
تم جمع بيانات تحليل تدفق الخلايا باستخدام برنامج BD FACSDiva (الإصدار 7). تم الحصول على بيانات FACS باستخدام أجهزة BD FACSymphony أو Agilent NovoVyte Penteon.
تم استخدام FlowJo 10.7.0 لتحليل بيانات تدفق الخلايا. وتم استخدام GraphPad Prism 10.1 و R studio 4.0.3 للرسم والتحليل الإحصائي.
بيانات
يجب أن تتضمن جميع المخطوطات بيانًا عن توفر البيانات. يجب أن يوفر هذا البيان المعلومات التالية، حيثما ينطبق:
- رموز الانضمام، معرفات فريدة، أو روابط ويب لمجموعات البيانات المتاحة للجمهور
- وصف لأي قيود على توفر البيانات
- بالنسبة لمجموعات البيانات السريرية أو بيانات الطرف الثالث، يرجى التأكد من أن البيان يتماشى مع سياستنا
محفظة الطبيعة | ملخص التقرير
أبريل 2023
البحث الذي يتضمن مشاركين بشريين، بياناتهم، أو مواد بيولوجية
| التقارير عن الجنس والنوع الاجتماعي | تم الإبلاغ عن كل من المرضى الذكور والإناث. تم الحصول على معلومات الجنس من السجلات الإلكترونية للمرضى، مع جمع الموافقة المستنيرة من جميع المشاركين. تتراوح أعمار المرضى بين 4 و 66 عامًا، مع
|
| التقارير عن العرق أو الإثنية أو غيرها من التجمعات الاجتماعية ذات الصلة | تُدرج بيانات العرق والإثنية في المعلومات التكميلية |
| خصائص السكان | تم تجنيد المرضى الذين يخضعون لعملية استئصال اللوزتين بموافقة لجنة الأخلاقيات للمساهمة بأنسجة في هذه الدراسة. تم استبعاد المرضى الذين يعانون من عدوى خطيرة أو الذين يتناولون أدوية مناعية نظامية من الدراسة. تتراوح أعمار المرضى من 4 إلى 66 عامًا، مع
|
| التوظيف | سيتم إحالة المرضى إلى الوحدات السريرية المناسبة لرعايتهم، مثل الإجراءات الجراحية. قبل إجراء عملية المريض، سيتواصل فريق البحث لدينا مع عائلة المريض الطفل أو البالغ للحصول على موافقة خطية مستنيرة. تم استبعاد المرضى الذين يعانون من عدوى خطيرة أو الذين كانوا يتناولون أدوية مناعية نظامية من الدراسة. الأفراد المسؤولون عن الحصول على موافقة المرضى وجمع الأنسجة لم يكونوا متورطين في الجوانب العلمية للدراسة. لا نتوقع أي انحياز منهجي في استراتيجيتنا لجمع البيانات. |
| رقابة الأخلاقيات | تمت تغطية جمع وعمل عينات اللوزتين من الأطفال والمتطوعين البالغين بواسطة بروتوكولات IRB 30837 و60741، المعتمدة من قبل مجلس المراجعة المؤسسية بجامعة ستانفورد (IRB). تم الحصول على موافقات مستنيرة من المشاركين و/أو من الآباء/الأوصياء القانونيين. لم يتم تقديم تعويض للمشاركين. تم طلب دم من متبرعين أصحاء من مركز دم ستانفورد بموجب بروتوكول IRB 40146. |
التقارير المتخصصة في المجال
علوم الحياة
العلوم السلوكية والاجتماعية
العلوم البيئية والتطورية والبيئية
لنسخة مرجعية من الوثيقة بجميع الأقسام، انظرnature.com/documents/nr-reporting-summary-flat.pdf
تصميم دراسة العلوم الحياتية
| حجم العينة | تفاوتت أحجام العينات من
|
| استثناءات البيانات | لم يتم استبعاد أي بيانات |
| التكرار | تم تقديم عدد المتبرعين الذين تم اختبارهم في أساطير الأشكال. توقعنا وجود تباين بين المتبرعين في الاستجابة للتحفيز والعلاج، وتم الإبلاغ عن الاستجابات للتحفيز في الأشكال أو في النص. تم استخدام متبرعين مختلفين لإظهار نطاق الاستجابات الممكنة. |
| العشوائية | كانت المجموعات التجريبية مرتبطة بالتحفيز، والجنس، والعمر، وبالتالي فإن العشوائية ليست ذات صلة. |
| عمى | التعمية غير ذات صلة بهذه الدراسة لأنها ليست تجربة سريرية. الهدف هو تقييم استجابات زراعة الخلايا لعلاجات مختلفة باستخدام اختبارات معتمدة. |
التقارير عن مواد وأنظمة وطرق محددة
| غير متوفر | مشارك في الدراسة | غير متوفر | مشارك في الدراسة |
| □ | – الأجسام المضادة | إكس | □ |
| □ | – خطوط خلايا حقيقية النواة | □ | – قياس التدفق الخلوي |
| – | □ | إكس | □ |
| – | □ | ||
| □ | |||
| إكس | □ | ||
| “め” translates to “م” in Arabic. | □ |
الأجسام المضادة
| الأجسام المضادة المستخدمة |
|
|||||||||||||||||
| التحقق |
|
خطوط خلايا حقيقية النواة
المصادقة
تلوث الميكوبلازما
النباتات
| مخزونات البذور | غير متوفر | ||
| أنماط جينية نباتية جديدة |
|
||
| المصادقة | غير متوفر |
تدفق الخلايا
المؤامرات
توضح تسميات المحاور العلامة والفلوركروم المستخدم (مثل CD4-FITC).
المقاييس على المحاور واضحة تمامًا. قم بتضمين الأرقام على المحاور فقط للرسم البياني في أسفل اليسار من المجموعة (المجموعة هي تحليل للعلامات المتطابقة).
جميع الرسوم البيانية هي رسوم بيانية متساوية الارتفاع مع نقاط شاذة أو رسوم بيانية بالألوان الزائفة.
تم توفير قيمة عددية لعدد الخلايا أو النسبة المئوية (مع الإحصائيات).
المنهجية
| تحضير العينة | تم إعادة تعليق الأعضاء الثقافية عن طريق شطف الغشاء بالوسط وجمعها من الترانسويلز. تم غسل الخلايا بمحلول FACS (PBS + 0.1% BSA، 0.05% نازيد الصوديوم و 2 مللي مول EDTA) ومعالجتها بحاجز مستقبلات Fc (Biolegend،
|
|||
| آلة | تم الحصول على بيانات FACS باستخدام أجهزة BD FACSymphony أو Agilent NovoVyte Penteon. تم استخدام BD FACSAria لفرز الخلايا. | |||
| برمجيات | تم جمع بيانات تحليل تدفق الخلايا باستخدام برنامج BD FACSDiva (الإصدار 7). | |||
| وفرة تجمع الخلايا | نقاء الخلايا المفروزة كان أكثر من
|
|||
| استراتيجية البوابة |
|
معهد المناعة وزرع الأعضاء والعدوى، جامعة ستانفورد، ستانفورد، كاليفورنيا، الولايات المتحدة الأمريكية. قسم المناعة والميكروبيولوجيا، جامعة كوبنهاغن، كوبنهاغن، الدنمارك. قسم جراحة النوم، قسم الأنف والأذن والحنجرة – جراحة الرأس والعنق، كلية الطب بجامعة ستانفورد، ستانفورد، كاليفورنيا، الولايات المتحدة الأمريكية. قسم علم الأحياء الدقيقة والمناعة، كلية الطب بجامعة ستانفورد، ستانفورد، كاليفورنيا، الولايات المتحدة الأمريكية. معهد هوارد هيوز الطبي، كلية الطب بجامعة ستانفورد، ستانفورد، كاليفورنيا، الولايات المتحدة الأمريكية. ساهم هؤلاء المؤلفون بالتساوي: شين تشين، مصطفى غانيزادا. -البريد الإلكتروني:mmdavis@stanford.edu
DOI: https://doi.org/10.1038/s41590-024-02062-x
PMID: https://pubmed.ncbi.nlm.nih.gov/39806065
Publication Date: 2025-01-13
Differential roles of human
Accepted: 10 December 2024
Published online: 13 January 2025
Check for updates

d,e, Representative FACS plots of FOXP3 expression in CD4+ T cells (d) and KIR and granzyme B expression in CD8
their functions and gauged their effects on self-reactive
also demonstrate that we can model key features of how autoreactive B and T cells are controlled and, more broadly, quickly test hypotheses and define mechanisms in a purely human system.
Results
Efficient gene KO using Cas9-RNPs

the suppressive function of CD4
were used as a control to generate wild-type (WT) T cells. To avoid the possibility of the attached beads interfering with the function of antigen-presenting cells (for example, B cells and myeloid cells), we purified the unlabeled CD3-negative cells separately from a new vial of tonsil cells. The CD3-negative cells and electroporated CD3-positive cells were enumerated, combined and plated into transwells at a density of


viability and the KO efficiency by measuring intracellular protein levels via flow cytometry. T cells from WT and KO cultures maintained good viability (
KO tonsil organoids show inflammatory phenotypes
via granzyme B on autoreactive T cells
Differential autoantibody production in KO tonsil organoids

between stimulation and PBS conditions in tonsils with WT, FOXP3 KO and GZMB KO T cells 7 days poststimulation (
production compared with WT tonsil organoids, even with addition of the autoantigen to the culture (Extended Data Fig. 5). Previous studies have suggested that viral infection could be a primary factor in initiation of autoimmune diseases
Autoreactive B cells in FOXP3 KO organoids expanded after stimulation
targeting the autoantigens PR3, snRNP-C and core histone. In the presence of LAIV, the autoantigen cocktail profoundly stimulated the expansion of self-antigen-specific B cells in FOXP3 KO tonsil organoids (Fig. 4a,b), consistent with the observed autoantibody levels. Notably, the top two FOXP3KO tonsil organoids that produced the higher frequency of autoreactive B cells after LAIV plus autoantigen stimulation were also derived from female donors (Fig. 4b). By contrast, knocking out GZMB in tonsillar T cells had only a minor impact on the frequencies of autoreactive B cells (Fig. 4a,b), confirming that CD4
Differential autoreactive T cell response in KO organoids

condition was calculated.
observed a statistically significant expansion of

FOXP3 KO enhances higher antibody affinity
Higher autoreactivity in organoids from women compared with men
Discussion

model to predict the correlations between autoantibody levels, age and sex. The regression model coefficients (slopes) represent the effect of age on the response variable for each sex, with
Online content
References
- Valent, P. et al. Paul Ehrlich (1854-1915) and his contributions to the foundation and birth of translational medicine. J. Innate Immun. 8, 111-120 (2016).
- Goodnow, C. C. et al. Altered immunoglobulin expression and functional silencing of self-reactive B lymphocytes in transgenic mice. Nature 334, 676-682 (1988).
- Asano, M., Toda, M., Sakaguchi, N. & Sakaguchi, S. Autoimmune disease as a consequence of developmental abnormality of a T cell subpopulation. J. Exp. Med. 184, 387-396 (1996).
- Baecher-Allan, C. & Hafler, D. A. Human regulatory T cells and their role in autoimmune disease. Immunol. Rev. 212, 203-216 (2006).
- Jiang, H., Zhang, S. I. & Pernis, B. Role of CD8+ T cells in murine experimental allergic encephalomyelitis. Science 256, 1213-1215 (1992).
- Kim, H. J. et al. Stable inhibitory activity of regulatory T cells requires the transcription factor Helios. Science 350, 334-339 (2015).
- Kim, H. J., Verbinnen, B., Tang, X., Lu, L. & Cantor, H. Inhibition of follicular T-helper cells by CD8
regulatory T cells is essential for self tolerance. Nature 467, 328-332 (2010). - Li , J. et al.
cells suppress pathogenic T cells and are active in autoimmune diseases and COVID-19. Science 376, eabi9591 (2022). - Saligrama, N. et al. Opposing T cell responses in experimental autoimmune encephalomyelitis. Nature 572, 481-487 (2019).
- Wagar, L. E. et al. Modeling human adaptive immune responses with tonsil organoids. Nat. Med. 27, 125-135 (2021).
- Kastenschmidt, J. M. et al. Influenza vaccine format mediates distinct cellular and antibody responses in human immune organoids. Immunity 56, 1910-1926.e7 (2023).
- Hadaschik, E. N. et al. Regulatory T cell-deficient scurfy mice develop systemic autoimmune features resembling lupus-like disease. Arthritis Res. Ther. 17, 35 (2015).
- Tsuda, M. et al. The spectrum of autoantibodies in IPEX syndrome is broad and includes anti-mitochondrial autoantibodies. J. Autoimmun. 35, 265-268 (2010).
- Chang, S. E. et al. New-onset IgG autoantibodies in hospitalized patients with COVID-19. Nat. Commun. 12, 5417 (2021).
- Poulsen, T. R., Jensen, A., Haurum, J. S. & Andersen, P. S. Limits for antibody affinity maturation and repertoire diversification in hypervaccinated humans. J. Immunol. 187, 4229-4235 (2011).
- Choi, S. J. et al.
and NKG2A cells are distinct innate-like populations in humans. Cell Rep. 42, 112236 (2023). - Rubtsova, K., Marrack, P. & Rubtsov, A. V. Sexual dimorphism in autoimmunity. J. Clin. Invest. 125, 2187-2193 (2015).
- Dieckmann, D., Plottner, H., Berchtold, S., Berger, T. & Schuler, G. Ex vivo isolation and characterization of
cells with regulatory properties from human blood. J. Exp. Med. 193, 1303-1310 (2001). - Baecher-Allan, C. M. & Hafler, D. A. The purification and functional analysis of human CD4
regulatory T cells. Curr. Protoc. Immunol. 72, 7.4B.1-7.4B. 12 (2006). - Hori, S., Nomura, T. & Sakaguchi, S. Control of regulatory T cell development by the transcription factor Foxp3. Science https://doi.org/10.1126/science. 1079490 (2003).
- Salti, S. M. et al. Granzyme B regulates antiviral CD8+ T cell responses. J. Immunol. 187, 6301-6309 (2011).
- Li , J. et al.
cells suppress pathogenic T cells and are active in autoimmune diseases and COVID-19. Science https://doi. org/10.1126/science.abi9591 (2022). - Loebbermann, J. et al. Regulatory T cells expressing granzyme B play a critical role in controlling lung inflammation during acute viral infection. Mucosal Immunol. 5, 161-172 (2012).
- Ise, W. et al. T follicular helper cell-germinal center B cell interaction strength regulates entry into plasma cell or recycling germinal center cell fate. Immunity 48, 702-715.e4 (2018).
- Mintz, M. A. & Cyster, J. G. T follicular helper cells in germinal center B cell selection and lymphomagenesis. Immunol. Rev. 296, 48-61(2020).
- Shulman, Z. et al. T follicular helper cell dynamics in germinal centers. Science 341, 673-677 (2013).
- Getts, D. R., Chastain, E. M., Terry, R. L. & Miller, S. D. Virus infection, antiviral immunity, and autoimmunity. Immunol. Rev. 255, 197-209 (2013).
- Dieker, J. et al. Autoantibodies against modified histone peptides in SLE patients are associated with disease activity and lupus nephritis. PLoS ONE 11, e0165373 (2016).
- Kattah, N. H., Kattah, M. G. & Utz, P. J. The U1-snRNP complex: structural properties relating to autoimmune pathogenesis in rheumatic diseases. Immunol. Rev. 233, 126-145 (2010).
- Primo, V. C. et al. Anti-PR3 immune responses induce segmental and necrotizing glomerulonephritis. Clin. Exp. Immunol. 159, 327-337 (2010).
- Mallajosyula, V. et al. CD8
T cells specific for conserved coronavirus epitopes correlate with milder disease in patients with COVID-19. Sci. Immunol. https://doi.org/10.1126/sciimmunol.abg5669 (2021). - Yu, W. et al. Clonal deletion prunes but does not eliminate self-specific
CD8 T lymphocytes. Immunity 42, 929-941 (2015). - Nielen, M. M. et al. Antibodies to citrullinated human fibrinogen (ACF) have diagnostic and prognostic value in early arthritis. Ann. Rheum. Dis. 64, 1199-1204 (2005).
- Su, L. F., Kidd, B. A., Han, A., Kotzin, J. J. & Davis, M. M. Virus-specific CD4
memory-phenotype T cells are abundant in unexposed adults. Immunity 38, 373-383 (2013). - Yuan, J. et al. Safety and immunogenicity of a human and mouse gp100 DNA vaccine in a phase I trial of patients with melanoma. Cancer Immun. 9, 5 (2009).
- Zhang, L., Nakayama, M. & Eisenbarth, G. S. Insulin as an autoantigen in NOD/human diabetes. Curr. Opin. Immunol. 20, 111-118 (2008).
- Goronzy, J. J. & Weyand, C. M. Immune aging and autoimmunity. Cell. Mol. Life Sci. 69, 1615-1623 (2012).
- Whitacre, C. C. Sex differences in autoimmune disease. Nat. Immunol. 2, 777-780 (2001).
- Wardemann, H. et al. Predominant autoantibody production by early human B cell precursors. Science https://doi.org/10.1126/ science. 1086907 (2003).
- Fontenot, J. D., Gavin, M. A. & Rudensky, A. Y. Foxp3 programs the development and function of CD4
CD25 regulatory T cells. Nat. Immunol. 4, 330-336 (2003). - Kim, J. M. & Rudensky, A. The role of the transcription factor Foxp3 in the development of regulatory T cells. Immunol. Rev. 212, 86-98 (2006).
- Sakaguchi, S. Naturally arising Foxp3-expressing CD25
regulatory T cells in immunological tolerance to self and non-self. Nat. Immunol. 6, 345-352 (2005). - Yang, S., Fujikado, N., Kolodin, D., Benoist, C. & Mathis, D. Immune tolerance. Regulatory T cells generated early in life play a distinct role in maintaining self-tolerance. Science 348, 589-594 (2015).
- Zheng, Y. & Rudensky, A. Y. Foxp3 in control of the regulatory T cell lineage. Nat. Immunol. 8, 457-462 (2007).
- Hoshino, A. et al. Identification of autoantibodies using human proteome microarrays in patients with IPEX syndrome. Clin. Immunol. 203, 9-13 (2019).
- Kinnunen, T. et al. Accumulation of peripheral autoreactive B cells in the absence of functional human regulatory T cells. Blood 121, 1595-1603 (2013).
- McCarron, M. J. & Marie, J. C. TGF-beta prevents T follicular helper cell accumulation and B cell autoreactivity. J. Clin. Invest. 124, 4375-4386 (2014).
- Lim, H. W., Hillsamer, P., Banham, A. H. & Kim, C. H. Cutting edge: direct suppression of B cells by
regulatory T cells. J. Immunol. https://doi.org/10.4049/jimmunol.175.7.4180 (2005). - likuni, N., Lourenço, E. V., Hahn, B. H. & La, C. Cutting edge: regulatory T cells directly suppress B cells in systemic lupus erythematosus. J. Immunol. https://doi.org/10.4049/ jimmunol. 0901163 (2009).
- Lam, A. J. et al. Optimized CRISPR-mediated gene knockin reveals FOXP3-independent maintenance of human Treg identity. Cell Rep. 36, 109494 (2021).
- Zhang, W. et al. FOXP3 recognizes microsatellites and bridges DNA through multimerization. Nature 624, 433-441 (2023).
- Le Coz, C. et al. Human T follicular helper clones seed the germinal center-resident regulatory pool. Sci. Immunol. 8, eade8162 (2023).
- Davis, M. M. In praise of descriptive science: a breath of fresh AIRE. Cell 166, 530-531 (2016).
- Meyer, S. et al. AIRE-deficient patients harbor unique high-affinity disease-ameliorating autoantibodies. Cell 166, 582-595 (2016).
- Rabia, L. A., Desai, A. A., Jhajj, H. S. & Tessier, P. M. Understanding and overcoming trade-offs between antibody affinity, specificity, stability and solubility. Biochem. Eng. J. 137, 365-374 (2018).
- Suurmond, J. & Diamond, B. Autoantibodies in systemic autoimmune diseases: specificity and pathogenicity. J. Clin. Invest. 125, 2194-2202 (2015).
- Sundaresan, B., Shirafkan, F., Ripperger, K. & Rattay, K. The role of viral infections in the onset of autoimmune diseases. Viruses https://doi.org/10.3390/v15030782 (2023).
- Arbuckle, M. R. et al. Development of anti-dsDNA autoantibodies prior to clinical diagnosis of systemic lupus erythematosus. Scand. J. Immunol. 54, 211-219 (2001).
- Arbuckle, M. R. et al. Development of autoantibodies before the clinical onset of systemic lupus erythematosus. N. Engl. J. Med. 349, 1526-1533 (2003).
- Leslie, D., Lipsky, P. & Notkins, A. L. Autoantibodies as predictors of disease. J. Clin. Invest. 108, 1417-1422 (2001).
- Olsen, N. J., Okuda, D. T., Holers, V. M. & Karp, D. R. Editorial: understanding the concept of pre-clinical autoimmunity. Front. Immunol. 13, 983310 (2022).
(c) The Author(s) 2025
Methods
Human samples and tonsil processing
Blood processing
Cas9-RNP assembly and electroporation
Cell sorting and organoid assembly
Cell culture and stimulation
Flow cytometry
followed by staining with live/dead Aqua Zombie stain (Thermo Fisher) and antibodies against surface markers (
Antibody detection by enzyme-linked immunosorbent assay
Protein expression, purification and biotinylation
Assembly of the peptide-MHC-spheromer complex and autoantigen-spheromer complex
core facility), pMHC-I monomers (NIH tetramer core facility) or autoantigens (generated in-house) were incubated with
Binding affinity measurement
Statistical analysis
Reporting summary
Data availability
Code availability
Acknowledgements
Author contributions
Competing interests
Additional information

in PBMC and tonsil samples. c, A workflow of generating genetically modified tonsil organoids using Cas9-RNPs. d, A representative FACS profile showing Live/Dead staining of T cells from the WT, FOXP3 KO, and GZMB KO tonsil organoids.





indicated conditions from tonsil organoids. c, Expression of CD27 and CD38 in B cells from tonsil organoids with WT, GZMB KO, and CXCR5-depleted GZMB KO

by ELISA (


Abstract
Extended Data Fig. 7 | The percentage of HA -specific
natureportfolio
| Corresponding author(s): | Mark M Davis |
| Last updated by author(s): 2024/12/05 |
Reporting Summary
Statistics
n/a
Confirmed
□ X
The exact sample size
□
□ A statement on whether measurements were taken from distinct samples or whether the same sample was measured repeatedly
□ X
The statistical test(s) used AND whether they are one- or two-sided
Only common tests should be described solely by name; describe more complex techniques in the Methods section.

□ A description of all covariates tested
□ X
A description of any assumptions or corrections, such as tests of normality and adjustment for multiple comparisons
□

□ X
For null hypothesis testing, the test statistic (e.g.
□ For Bayesian analysis, information on the choice of priors and Markov chain Monte Carlo settings
□ For hierarchical and complex designs, identification of the appropriate level for tests and full reporting of outcomes
□ Estimates of effect sizes (e.g. Cohen’s
Our web collection on statistics for biologists contains articles on many of the points above.
Software and code
Data collection
Flow cytometry date were collected using BD FACSDiva software (v7). FACS data were obtained using BD FACSymphony or Agilent NovoVyte Penteon instruments.
FlowJo 10.7.0 was used for the analysis of flow cytometry data. GraphPad Prism 10.1 and R studio 4.0.3 were used for plotting and statistical analysis.
Data
All manuscripts must include a data availability statement. This statement should provide the following information, where applicable:
- Accession codes, unique identifiers, or web links for publicly available datasets
- A description of any restrictions on data availability
- For clinical datasets or third party data, please ensure that the statement adheres to our policy
nature portfolio | reporting summary
April 2023
Research involving human participants, their data, or biological material
| Reporting on sex and gender | Both male and female patients are reported. Sex information was obtained from electronic patient records, with informed consent collected from all participants. The patients’ ages range from 4 to 66 years, with
|
| Reporting on race, ethnicity, or other socially relevant groupings | Race and ethnicity data are listed in the supplementary information |
| Population characteristics | Patients undergoing tonsillectomy were recruited with IRB approval for donating tissues to this study. Patients with serious infections or who were taking systemic immunomodulatory drugs were excluded from the study. The patients’ ages range from 4 to 66 years, with
|
| Recruitment | Patients will be referred to the appropriate clinical units for their respective care, such as surgical procedures. Prior to the patient’s surgery, our research team will contact the family of the child or adult patient to obtain written informed consent. Patients with serious infections or who were taking systemic immunomodulatory drugs were excluded from the study. Individiuals responsible for consenting patients and collecting tissues were not involved in the scientific aspects of the study. We do not expect any systematic bias in our collection strategy. |
| Ethics oversight | The collection and process of tonsil samples from children and adult volunteers were covered by IRB protocols 30837 and 60741, approved by the Stanford University Institutional Review Board (IRB). Informed consents were obtained from the participants and/or from parents/legal guardians. No participant compensation was provided for the participants. Blood from healthy donors was requested from the Stanford Blood Center under IRB protocol 40146. |
Field-specific reporting
Life sciences
Behavioural & social sciences
Ecological, evolutionary & environmental sciences
For a reference copy of the document with all sections, see nature.com/documents/nr-reporting-summary-flat.pdf
Life sciences study design
| Sample size | Sample sizes varied from
|
| Data exclusions | No data were excluded |
| Replication | The number of donors tested is provided in the figure legends. We anticipated inter-donor variation in response to the stimulation and treatment and responses to stimulation were reported in figures or in text. Different donors were used to demonstrate the range of possible responses. |
| Randomization | Experimental groups were stimulation-related, sex and age-related, thus randomization is not relevant. |
| Blinding | Blinding is irrelevant for this study as it is not a clinical trial. The objective is to assess cell culture responses to various treatments using established assays. |
Reporting for specific materials, systems and methods
| n/a | Involved in the study | n/a | Involved in the study |
| □ | – Antibodies | X | □ |
| □ | – Eukaryotic cell lines | □ | – Flow cytometry |
| – | □ | X | □ |
| – | □ | ||
| □ | |||
| X | □ | ||
| め | □ |
Antibodies
| Antibodies used |
|
|||||||||||||||||
| Validation |
|
Eukaryotic cell lines
Authentication
Mycoplasma contamination
Plants
| Seed stocks | N/A | ||
| Novel plant genotypes |
|
||
| Authentication | N/A |
Flow Cytometry
Plots
The axis labels state the marker and fluorochrome used (e.g. CD4-FITC).
The axis scales are clearly visible. Include numbers along axes only for bottom left plot of group (a ‘group’ is an analysis of identical markers).
All plots are contour plots with outliers or pseudocolor plots.
A numerical value for number of cells or percentage (with statistics) is provided.
Methodology
| Sample preparation | Culture organoids were resuspended by rinsing the membrane with media and collected from the transwells. Cells were washed with FACS buffer (PBS+0.1% BSA, 0.05% sodium azide and 2 mM EDTA) and treated with Fc receptor block (Biolegend,
|
|||
| Instrument | FACS data were obtained using BD FACSymphony or Agilent NovoVyte Penteon instruments. BD FACSAria was used for Cell sorting | |||
| Software | Flow cytometry date were collected using BD FACSDiva software (v7). | |||
| Cell population abundance | The purify of the sorted cells was more than
|
|||
| Gating strategy |
|
Institute for Immunity, Transplantation, and Infection, Stanford University, Stanford, CA, USA. Department of Immunology and Microbiology, University of Copenhagen, Copenhagen, Denmark. Division of Sleep Surgery, Department of Otolaryngology-Head and Neck Surgery, Stanford University School of Medicine, Stanford, CA, USA. Department of Microbiology and Immunology, Stanford University School of Medicine, Stanford, CA, USA. The Howard Hughes Medical Institute, Stanford University School of Medicine, Stanford, CA, USA. These authors contributed equally: Xin Chen, Mustafa Ghanizada. -e-mail: mmdavis@stanford.edu
