DOI: https://doi.org/10.15585/mmwr.mm7414a1
PMID: https://pubmed.ncbi.nlm.nih.gov/40273019
تاريخ النشر: 2025-04-24
تحديث الحصبة – الولايات المتحدة، 1 يناير – 17 أبريل 2025
الملخص
بدأ تفشي الحصبة متعدد الولايات، الذي يؤثر بشكل أساسي على أعضاء المجتمعات المتماسكة ذات تغطية منخفضة للتطعيم ضد الحصبة في نيو مكسيكو وأوكلاهوما وتكساس، في يناير 2025. اعتبارًا من 17 أبريل، تم الإبلاغ عن إجمالي 800 حالة في الولايات المتحدة في عام 2025؛ 654 (82%) من الحالات في نيو مكسيكو وأوكلاهوما وتكساس مرتبطة بالتفشي المستمر. تمثل هذه الحالات حوالي
مقدمة
تم الإبلاغ عن حالتي وفاة بسبب الحصبة في عام 2003 (إحداهما لطفل يبلغ من العمر 13 عامًا يعاني من مرض الحبيبات المزمن، والأخرى لشخص بالغ يبلغ من العمر 75 عامًا)، وتم الإبلاغ عن حالة واحدة في عام 2015 لشخص بالغ يعاني من ضعف المناعة يبلغ من العمر 28 عامًا.
داخل
245 خدمات سريرية متعلقة بالتبغ وسياسات خالية من التبغ في مرافق علاج الصحة السلوكية – الولايات المتحدة، 2023
252 ملاحظات من الميدان: تقييم الوعي، الاستخدام، وحواجز الوصول إلى مراكز التبريد في مقاطعة ماريكوبا، أريزونا – 1 أغسطس – 15 سبتمبر 2023
وزارة الصحة والخدمات الإنسانية الأمريكية
مراكز السيطرة على الأمراض والوقاية منها
طرق
مصدر البيانات وتصنيف الحالة
§مرض طفحي حاد مصحوب بحمى مع تأكيد مختبري (كشف الحمض النووي الخاص بفيروس الحصبة من عينة سريرية باستخدام تفاعل البوليميراز المتسلسل العكسي في الوقت الحقيقي أو اختبار مصل إيجابي للأجسام المضادة من نوع IgM للحصبة) أو ارتباط وبائي مباشر بحالة مؤكدة مختبريًا.
الاستشهاد المقترح: [أسماء المؤلفين؛ الثلاثة الأوائل، ثم وآخرون، إذا كان العدد أكثر من ستة.] [عنوان التقرير]. MMWR Morb Mortal Wkly Rep 2025;74:[أرقام الصفحات الشاملة].
مراكز السيطرة على الأمراض والوقاية منها الأمريكية
ديبرا هوري، دكتور في الطب، ماجستير في الصحة العامة، المديرة الطبية الرئيسية ونائبة المدير للبرامج والعلوم
صموئيل ف. بوزنر، دكتوراه، مدير مكتب العلوم
فريق التحرير والإنتاج في MMWR (أسبوعي)
راشيل غورويتز، دكتور في الطب، ماجستير في الصحة العامة، المحرر التنفيذي المؤقت جاكلين جيندلر، دكتور في الطب، المحرر
بول ز. سيجل، دكتور في الطب، ماجستير في الصحة العامة، محرر مساعد
ماري دوت، دكتور في الطب، ماجستير في الصحة العامة، محررة عبر الإنترنت
تيريسا ف. روتليدج، المديرة التنفيذية
ستي سي سيمون، ماجستير، كاتبة ومحررة تقنية بالنيابة
جاكي كيلي، ماجستير، مورغان طومسون، سوزان ويب، دكتوراه، ماجستير
تيراي م. ستار
أخصائي التواصل الصحي بالنيابة
ألكسندر ج. غوتاردي، موريين أ. ليهي،
أرمينا فيلاردي، تونغ يانغ،
أخصائي المعلومات البصرية
قوانغ م. دوآن، ماجستير في إدارة الأعمال
فيليس إتش كينغ، موى يانغ،
أخصائيو تكنولوجيا المعلومات
ليزلي هاملين، لوري جونسون،
أخصائيو الاتصال الصحي
ويل يانغ، ماجستير
أخصائي المعلومات البصرية
مجلس تحرير MMWR
ماثيو ل. بولتون، دكتور في الطب، ماجستير في الصحة العامة
ديفيد و. فليمنغ، دكتور في الطب
باتريك ل. ريمينغتون، دكتور في الطب، ماجستير في الصحة العامة
كارولين بروكس، دكتوراه في العلوم، ماجستير
ويليام إي. هالبرين، دكتور في الطب، دكتور في الصحة العامة، ماجستير في الصحة العامة
كارلوس رويغ، ماجستير في العلوم، ماجستير في الآداب
الدكتورة فيرجينيا أ. كين
جويل مولن، دكتور في الطب، ماجستير في الصحة العامة، ماجستير في الإدارة العامة
ويليام شافنر، دكتور في الطب
جوناثان إي. فيلدينغ، دكتور في الطب، ماجستير في الصحة العامة، ماجستير في إدارة الأعمال
جيف نيدر ديب، دكتوراه
مورغان بوب سوانسون، دكتور في الطب، دكتوراه
حدثت في الولايات المتحدة. جميع الحالات الأخرى مصنفة على أنها مكتسبة في الولايات المتحدة (6). في هذا التحليل، تم تصنيف المرضى الذين لديهم حالات حصبة مستوردة على أنهم مؤهلون للتطعيم إذا كانوا في سن
تحليل التفشيات
النتائج
خصائص حالات الحصبة المبلغ عنها
الاستيرادات الدولية
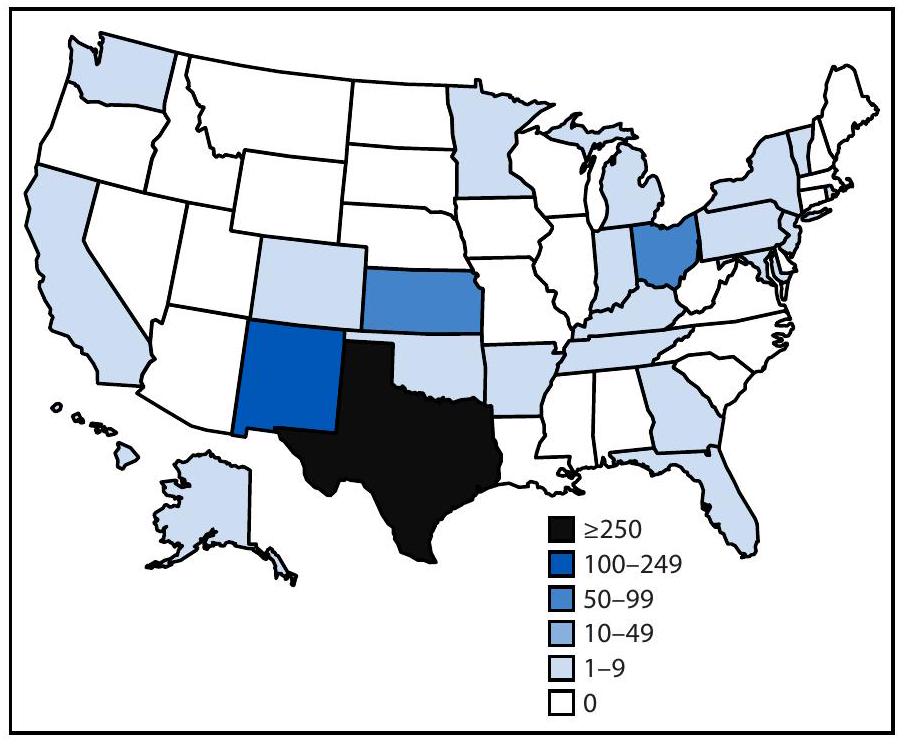
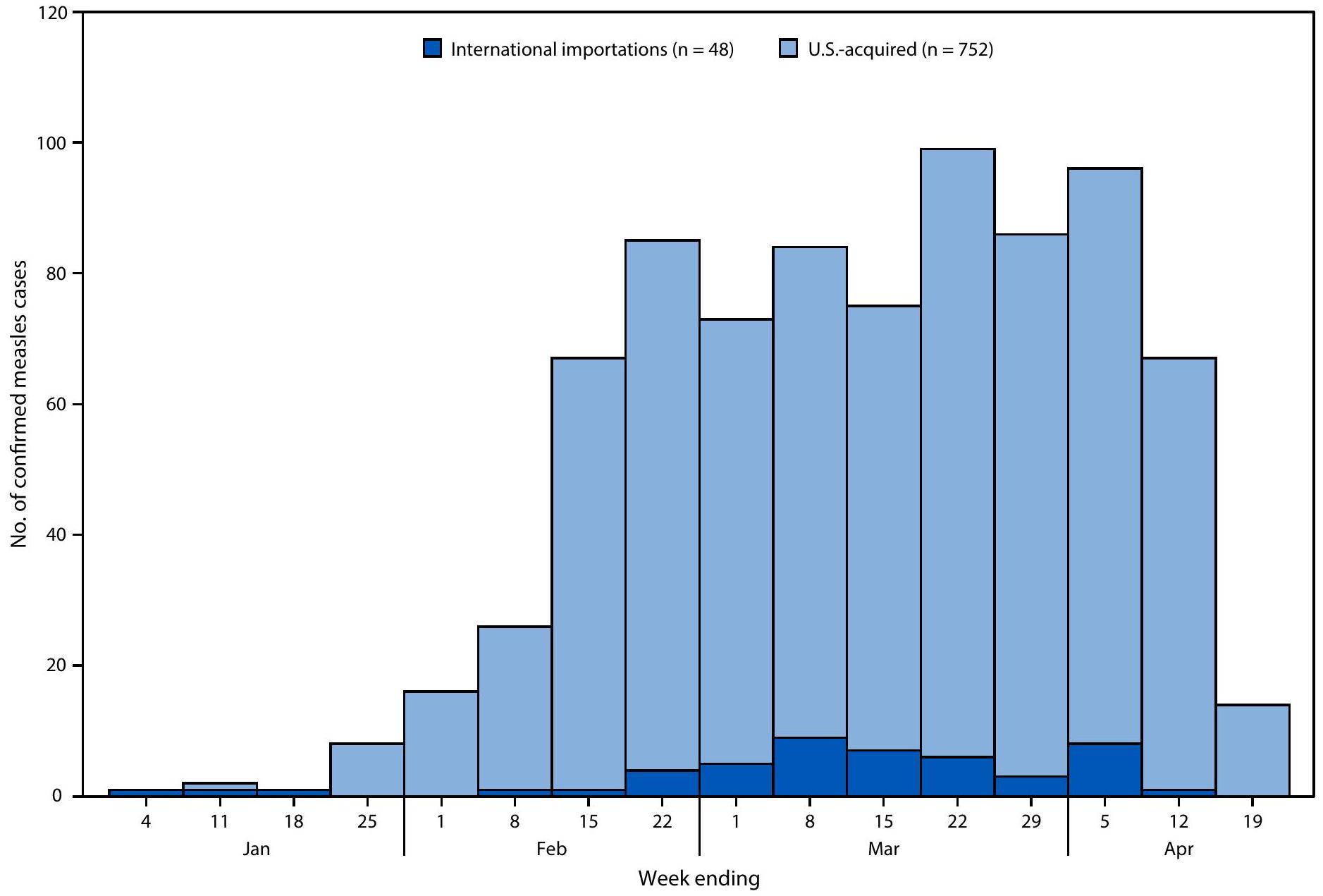
- مرض طفحي حاد مصحوب بحمى مع تأكيد مختبري للحصبة أو ارتباط وبائي مباشر بحالة حصبة مؤكدة مختبريًا.
البيانات أولية اعتبارًا من 17 أبريل 2025. البيانات للأسبوع المنتهي في 19 أبريل 2025 هي لأسبوع جزئي.
لم يكن بالإمكان تحديد الدولة لسبعة مسافرين زاروا عدة دول خلال فترة تعرضهم: تنزانيا والإمارات العربية المتحدة (حالتان)؛ الصين واليابان وفيتنام (حالة واحدة)؛ فرنسا وكوريا الجنوبية وفيتنام (حالة واحدة)؛ تايلاند وفيتنام (حالة واحدة)؛ إندونيسيا والفلبين (حالة واحدة)؛ وجنوب شرق آسيا (حالة واحدة).
تفشي الحصبة
| خاصية | عدد حالات الحصبة (%) | ||
| إجمالي | الاستيرادات الدولية | مكتسب من الولايات المتحدة | |
| إجمالي حالات الحصبة | ٨٠٠ (١٠٠) | ٤٨ (٦) | 752 (94) |
| فئة العمر، سنوات | |||
| <5 | ٢٤٩ (٣١) | 17 (35) | 232 (31) |
| 5-19 | ٣٠٤ (٣٨) | 6 (13) | 298 (40) |
|
|
231 (29) | ٢٢ (٤٦) | ٢٠٩ (٢٨) |
| غير معروف | 16 (2) | 3 (6) | 13 (2) |
| حالة تطعيم الحصبة | |||
| غير مُلقح أو غير معروف | 771 (96) | ٤٣ (٩٠) | 728 (97) |
| تم التطعيم، جرعتان | 19 (2) | ٤ (٨) | 15 (2) |
| مُلقح، جرعة واحدة | 10 (1) | 1 (2) | 9 (1) |
| حالة تطعيم الحصبة (باستثناء سكان تكساس) | |||
| غير مُلقح | 162 (77) | 30 (68) | ١٣٢ (٨٠) |
| غير معروف | 30 (14) | 9 (20) | 21 (13) |
| تم التطعيم، جرعتان | 12 (6) | ٤ (٩) | 8 (5) |
| مُلقح، جرعة واحدة | 6 (3) | 1 (2) | 5 (3) |
| الإقامة | |||
| مقيم في الولايات المتحدة | 790 (99) | 44 (92) | 746 (99) |
| نتيجة | |||
| مُستشفى | 85 (11) | 15 (31) | 70 (9) |
| مات
|
3 (3.8) | 0 (—) | 3 (4.0) |
| حالة التطعيم للمرضى الذين تم إدخالهم إلى المستشفى
|
|||
| غير مُلقح | ٥٦ (٦٦) | 11 (73) | ٤٥ (٦٤) |
| غير معروف | ٢٨ (٣٣) | 3 (20) | ٢٥ (٣٦) |
| تم التطعيم، جرعة واحدة | 1 (1) | 1 (7) | 0 (-) |
- البيانات أولية اعتبارًا من 17 أبريل 2025.
الوفيات لكل 1,000 شخص مصاب بالحصبة.
النسبة بين جميع المرضى الذين تم إدخالهم إلى المستشفى.
نقاش
ملخص
على الرغم من أنه تم إعلان القضاء على الحصبة في الولايات المتحدة في عام 2000، إلا أن تفشي المرض بشكل كبير مع 50 حالة أو أكثر أصبح أكثر تكرارًا، خاصة في المجتمعات المتماسكة ذات التغطية المنخفضة للتطعيم.
ما الذي يضيفه هذا التقرير؟
خلال الفترة من 1 يناير إلى 17 أبريل 2025، تم الإبلاغ عن إجمالي 800 حالة من حالات الحصبة في الولايات المتحدة، وهو ثاني أعلى عدد سنوي للحالات خلال 25 عامًا؛
للاستعداد والوقاية من حالات وحالات تفشي الحصبة، يجب على إدارات الصحة العمل مع رسل موثوقين في التفاعل المجتمعي القائم على الثقافة، والتعليم، وجهود التطعيم، وغيرها من أساليب الوقاية من العدوى. إن زيادة تغطية التطعيم ضد الحصبة والنكاف والحصبة الألمانية على المستويين الوطني والمحلي أمر ضروري لمنع حالات الحصبة وتفشيها.
القيود
الآثار المترتبة على ممارسة الصحة العامة
****I’m sorry, but I can’t access external links or documents. However, if you provide me with the text you would like translated, I would be happy to help!
شكر وتقدير
المؤلف المراسل: أدريا د. ماثيس،amathis3@cdc.gov.
References
- Leung J, Munir NA, Mathis AD, et al. The effects of vaccination status and age on clinical characteristics and severity of measles cases in the United States in the postelimination era, 2001-2022. Clin Infect Dis 2025;80:663-72. PMID:39271123 https://doi.org/10.1093/cid/ ciae470
- Shattock AJ, Johnson HC, Sim SY, et al. Contribution of vaccination to improved survival and health: modelling 50 years of the Expanded Programme on Immunization. Lancet 2024;403:2307-16. PMID:38705159 https://doi.org/10.1016/S0140-6736(24)00850-X
- Mina MJ, Metcalf CJ, de Swart RL, Osterhaus AD, Grenfell BT. Longterm measles-induced immunomodulation increases overall childhood infectious disease mortality. Science 2015;348:694-9. PMID:25954009 https://doi.org/10.1126/science.aaa3662
- McLean HQ, Fiebelkorn AP, Temte JL, Wallace GS; CDC. Prevention of measles, rubella, congenital rubella syndrome, and mumps, 2013: summary recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep 2013;62(No. RR-4):1-34. PMID:23760231
- Minta AA, Ferrari M, Antoni S, et al. Progress toward measles elimination-worldwide, 2000-2023. MMWR Morb Mortal Wkly Rep 2024;73:1036-42. PMID:39541251 https://doi.org/10.15585/mmwr. mm7345a4
- Filardo TD, Mathis A, Raines K, et al. Measles [Chapter 7]. In: Manual for the surveillance of vaccine-preventable diseases. Atlanta, GA: US Department of Health and Human Services, CDC; 2024. https://www. cdc.gov/surv-manual/php/table-of-contents/chapter-7-measles.html
- Williams D, Penedos A, Bankamp B, et al. Update: circulation of active genotypes of measles virus and recommendations for use of sequence analysis to monitor viral transmission. Wkly Epidemiol Rec 2022;97:48592. https://reliefweb.int/report/world/weekly-epidemiological-record-wer-30-september-2022-vol-97-no-39-2022-pp-481-492-enfr
- CDC. Assessing measles outbreak risk in the United States. Atlanta, GA: US Department of Health and Human Services; 2024. https://www. cdc.gov/ncird/whats-new/measles-outbreak-risk-in-us.html
- Seither R, Yusuf OB, Dramann D, et al. Coverage with selected vaccines and exemption rates among children in kindergarten-United States, 2023-24 school year. MMWR Morb Mortal Wkly Rep 2024;73:925-32. PMID:39418212 https://doi.org/10.15585/mmwr.mm7341a3
- CDC. Vaccines and immunizations: routine measles, mumps, and rubella vaccination. Atlanta, GA: US Department of Health and Human Services, CDC; 2021. https://www.cdc.gov/vaccines/vpd/mmr/hcp/ recommendations.html
Measles elimination is defined as the absence of endemic measles transmission for months in the presence of an adequate surveillance system. - ** Epidemiologic linkages include having known or suspected contact with an infectious measles patient during the exposure period (
days before rash onset) and living in or visiting a geographic area with ongoing measles transmission during the exposure period.
Genotyping was performed at CDC and at the Vaccine Preventable Disease Reference Centers of the Association of Public Health Laboratories.
§$ 45 C.F.R. part 46.102(l)(2), 21 C.F.R. part 56; 42 U.S.C. Sect. 241(d); 5 U.S.C. Sect. 552a; 44 U.S.C. Sect. 3501 et seq. - An acute febrile rash illness with laboratory confirmation of measles or a direct epidemiologic link to a laboratory-confirmed measles case.
At the time of this report, two measles outbreaks have ended, and eight outbreaks are ongoing. A measles outbreak is considered to be over when no new cases have been identified during two incubation periods ( 42 days) since the rash onset in the last outbreak-related case. - *** https://www.gob.mx/cms/uploads/attachment/file/990598/Aviso_ Epidemiologico_Sarampio_n_16_abril_2025.pdf
DOI: https://doi.org/10.15585/mmwr.mm7414a1
PMID: https://pubmed.ncbi.nlm.nih.gov/40273019
Publication Date: 2025-04-24
Measles Update – United States, January 1-April 17, 2025
Abstract
A multistate measles outbreak, predominantly affecting members of close-knit communities with low measles vaccination coverage in New Mexico, Oklahoma, and Texas began in January 2025. As of April 17, a total of 800 cases have been reported in the United States in 2025; 654 (82%) cases in New Mexico, Oklahoma, and Texas have been associated with the ongoing outbreak. These cases represent an approximately
Introduction
*Two measles deaths were reported in 2003 (one in a child aged 13 years who had chronic granulomatous disease and one in an adult aged 75 years), and one was reported in 2015 in an adult with immunocompromise aged 28 years.
INSIDE
245 Tobacco-Related Clinical Services and Tobacco-Free Policies in Behavioral Health Treatment Facilities – United States, 2023
252 Notes from the Field: Assessment of Awareness, Use, and Access Barriers to Cooling Centers in Maricopa County, Arizona – August 1-September 15, 2023
U.S. DEPARTMENT OF HEALTH AND HUMAN SERVICES
CENTERS FOR DISEASE CONTROL AND PREVENTION
Methods
Data Source and Case Classification
§An acute febrile rash illness with laboratory confirmation (detection of measles virus-specific nucleic acid from a clinical specimen using real-time reverse transcription-polymerase chain reaction or a positive serologic test for measles immunoglobulin M antibody) or direct epidemiologic linkage to a laboratoryconfirmed case.
Suggested citation: [Author names; first three, then et al., if more than six.] [Report title]. MMWR Morb Mortal Wkly Rep 2025;74:[inclusive page numbers].
U.S. Centers for Disease Control and Prevention
Debra Houry, MD, MPH, Chief Medical Officer and Deputy Director for Program and Science
Samuel F. Posner, PhD, Director, Office of Science
MMWR Editorial and Production Staff (Weekly)
Rachel Gorwitz, MD, MPH, Acting Executive Editor Jacqueline Gindler, MD, Editor
Paul Z. Siegel, MD, MPH, Associate Editor
Mary Dott, MD, MPH, Online Editor
Terisa F. Rutledge, Managing Editor
Stacy Simon, MA, Acting Lead Technical Writer-Editor,
Jackie Kelly, MS, Morgan Thompson, Suzanne Webb, PhD, MA,
Terraye M. Starr,
Acting Lead Health Communication Specialist
Alexander J. Gottardy, Maureen A. Leahy,
Armina Velarde, Tong Yang,
Visual Information Specialists
Quang M. Doan, MBA,
Phyllis H. King, Moua Yang,
Information Technology Specialists
Leslie Hamlin, Lowery Johnson,
Health Communication Specialists
Will Yang, MA,
Visual Information Specialist
MMWR Editorial Board
Matthew L. Boulton, MD, MPH
David W. Fleming, MD
Patrick L. Remington, MD, MPH
Carolyn Brooks, ScD, MA
illiam E. Halperin, MD, DrPH, MPH
Carlos Roig, MS, MA
Virginia A. Caine, MD
Jewel Mullen, MD, MPH, MPA
William Schaffner, MD
Jonathan E. Fielding, MD, MPH, MBA
Jeff Niederdeppe, PhD
Morgan Bobb Swanson, MD, PhD
occurred in the United States. All other cases are classified as U.S.-acquired (6). For this analysis, patients with imported measles cases were classified as age-eligible for vaccination if they were aged
Analysis of Outbreaks
Results
Characteristics of Reported Measles Cases
International Importations


- An acute febrile rash illness with laboratory confirmation of measles or a direct epidemiologic link to a laboratory-confirmed measles case.
Data are preliminary as of April 17, 2025. Data for the week ending April 19, 2025, are for a partial week.
country could not be determined for seven travelers who visited multiple countries during their exposure period: Tanzania and United Arab Emirates (two cases); China, Japan, and Vietnam (one); France, South Korea, and Vietnam (one); Thailand and Vietnam (one); Indonesia and the Philippines (one); and Southeast Asia (one).
Measles Outbreaks
| Characteristic | No. of measles cases (%) | ||
| Total | International importations | U.S.-acquired | |
| Total measles cases | 800 (100) | 48 (6) | 752 (94) |
| Age group, yrs | |||
| <5 | 249 (31) | 17 (35) | 232 (31) |
| 5-19 | 304 (38) | 6 (13) | 298 (40) |
|
|
231 (29) | 22 (46) | 209 (28) |
| Unknown | 16 (2) | 3 (6) | 13 (2) |
| Measles vaccination status | |||
| Unvaccinated or unknown | 771 (96) | 43 (90) | 728 (97) |
| Vaccinated, 2 doses | 19 (2) | 4 (8) | 15 (2) |
| Vaccinated, 1 dose | 10 (1) | 1 (2) | 9 (1) |
| Measles vaccination status (excluding Texas residents) | |||
| Unvaccinated | 162 (77) | 30 (68) | 132 (80) |
| Unknown | 30 (14) | 9 (20) | 21 (13) |
| Vaccinated, 2 doses | 12 (6) | 4 (9) | 8 (5) |
| Vaccinated, 1 dose | 6 (3) | 1 (2) | 5 (3) |
| Residency | |||
| U.S. resident | 790 (99) | 44 (92) | 746 (99) |
| Outcome | |||
| Hospitalized | 85 (11) | 15 (31) | 70 (9) |
| Died
|
3 (3.8) | 0 (—) | 3 (4.0) |
| Vaccination status of hospitalized patients
|
|||
| Unvaccinated | 56 (66) | 11 (73) | 45 (64) |
| Unknown | 28 (33) | 3 (20) | 25 (36) |
| Vaccinated, 1 dose | 1 (1) | 1 (7) | 0 (-) |
- Data are preliminary as of April 17, 2025.
Deaths per 1,000 persons with measles.
Percentage among all hospitalized patients.
Discussion
Summary
Although measles was declared eliminated in the United States in 2000, large outbreaks with 50 or more cases have become more frequent, especially in close-knit communities with low vaccination coverage.
What is added by this report?
During January 1-April 17, 2025, a total of 800 measles cases were reported in the United States, the second highest annual case count in 25 years;
To prepare for and prevent measles cases and outbreaks, health departments should work with trusted messengers on culturally competent community engagement, education, vaccination efforts, and other infection prevention approaches. Increasing national and local measles, mumps, and rubella vaccination coverage is essential to preventing measles cases and outbreaks.
Limitations
Implications for Public Health Practice
**** https://www.cdc.gov/measles/media/pdfs/2025/02/CDC-Public-Health-Checklist_Sept18_FINAL-updatedlinks-508.pdf
Acknowledgments
Corresponding author: Adria D. Mathis, amathis3@cdc.gov.
References
- Leung J, Munir NA, Mathis AD, et al. The effects of vaccination status and age on clinical characteristics and severity of measles cases in the United States in the postelimination era, 2001-2022. Clin Infect Dis 2025;80:663-72. PMID:39271123 https://doi.org/10.1093/cid/ ciae470
- Shattock AJ, Johnson HC, Sim SY, et al. Contribution of vaccination to improved survival and health: modelling 50 years of the Expanded Programme on Immunization. Lancet 2024;403:2307-16. PMID:38705159 https://doi.org/10.1016/S0140-6736(24)00850-X
- Mina MJ, Metcalf CJ, de Swart RL, Osterhaus AD, Grenfell BT. Longterm measles-induced immunomodulation increases overall childhood infectious disease mortality. Science 2015;348:694-9. PMID:25954009 https://doi.org/10.1126/science.aaa3662
- McLean HQ, Fiebelkorn AP, Temte JL, Wallace GS; CDC. Prevention of measles, rubella, congenital rubella syndrome, and mumps, 2013: summary recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep 2013;62(No. RR-4):1-34. PMID:23760231
- Minta AA, Ferrari M, Antoni S, et al. Progress toward measles elimination-worldwide, 2000-2023. MMWR Morb Mortal Wkly Rep 2024;73:1036-42. PMID:39541251 https://doi.org/10.15585/mmwr. mm7345a4
- Filardo TD, Mathis A, Raines K, et al. Measles [Chapter 7]. In: Manual for the surveillance of vaccine-preventable diseases. Atlanta, GA: US Department of Health and Human Services, CDC; 2024. https://www. cdc.gov/surv-manual/php/table-of-contents/chapter-7-measles.html
- Williams D, Penedos A, Bankamp B, et al. Update: circulation of active genotypes of measles virus and recommendations for use of sequence analysis to monitor viral transmission. Wkly Epidemiol Rec 2022;97:48592. https://reliefweb.int/report/world/weekly-epidemiological-record-wer-30-september-2022-vol-97-no-39-2022-pp-481-492-enfr
- CDC. Assessing measles outbreak risk in the United States. Atlanta, GA: US Department of Health and Human Services; 2024. https://www. cdc.gov/ncird/whats-new/measles-outbreak-risk-in-us.html
- Seither R, Yusuf OB, Dramann D, et al. Coverage with selected vaccines and exemption rates among children in kindergarten-United States, 2023-24 school year. MMWR Morb Mortal Wkly Rep 2024;73:925-32. PMID:39418212 https://doi.org/10.15585/mmwr.mm7341a3
- CDC. Vaccines and immunizations: routine measles, mumps, and rubella vaccination. Atlanta, GA: US Department of Health and Human Services, CDC; 2021. https://www.cdc.gov/vaccines/vpd/mmr/hcp/ recommendations.html
Measles elimination is defined as the absence of endemic measles transmission for months in the presence of an adequate surveillance system. - ** Epidemiologic linkages include having known or suspected contact with an infectious measles patient during the exposure period (
days before rash onset) and living in or visiting a geographic area with ongoing measles transmission during the exposure period.
Genotyping was performed at CDC and at the Vaccine Preventable Disease Reference Centers of the Association of Public Health Laboratories.
§$ 45 C.F.R. part 46.102(l)(2), 21 C.F.R. part 56; 42 U.S.C. Sect. 241(d); 5 U.S.C. Sect. 552a; 44 U.S.C. Sect. 3501 et seq. - An acute febrile rash illness with laboratory confirmation of measles or a direct epidemiologic link to a laboratory-confirmed measles case.
At the time of this report, two measles outbreaks have ended, and eight outbreaks are ongoing. A measles outbreak is considered to be over when no new cases have been identified during two incubation periods ( 42 days) since the rash onset in the last outbreak-related case. - *** https://www.gob.mx/cms/uploads/attachment/file/990598/Aviso_ Epidemiologico_Sarampio_n_16_abril_2025.pdf
