DOI: https://doi.org/10.1038/s41467-024-47022-z
PMID: https://pubmed.ncbi.nlm.nih.gov/38521830
تاريخ النشر: 2024-03-23
تسهيل لحظات ثنائية القطب المستحثة في محفزات ZnCdS غير المتبلورة لتطور الهيدروجين الضوئي
تم القبول: 18 مارس 2024
نُشر على الإنترنت: 23 مارس 2024
(أ) التحقق من التحديثات
الملخص
تعتبر أشباه الموصلات غير المتبلورة التي تفتقر إلى هياكل الشبكة البلورية المثالية غير ملائمة عادةً للتصوير الضوئي بسبب وجود حالات الفخ الغنية والعيوب. هنا نوضح أن كسر النظام الذري بعيد المدى في محفز ZnCdS غير المتبلور يمكن أن يحفز لحظات ثنائية القطب ويولد مجالات كهربائية قوية داخل الجسيمات مما يسهل فصل الشحنات ونقلها. التحميل
يمكن تحسين أزواج الإلكترونات والثقوب الناتجة عن الضوء بشكل كبير، حيث يمكن استهلاك الإلكترونات والثقوب الناتجة عن الضوء في التفاعلات الضوئية الحفازة على السطح، وبالتالي يمكن القضاء على التفاعلات الجانبية بين حوامل الشحنة الناتجة عن الضوء والحفاز الضوئي نفسه. خلال عملية التحفيز الضوئي، يتم نقل الإلكترونات والثقوب الناتجة عن الضوء بشكل عشوائي داخل الحفاز الضوئي الجزيئي بسبب عدم وجود مجال كهربائي موجه.
النتائج
آلية حقول ثنائية القطب الناتجة عن الهيكل غير المتبلور
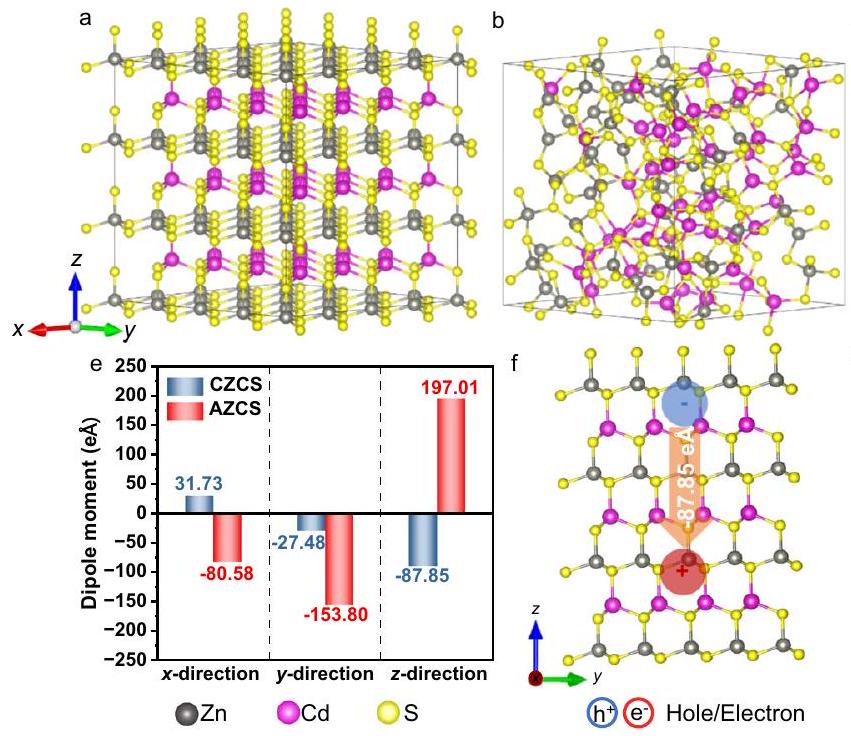


0.30 e


الاتجاهات البلورية. مخططات (ف) CZCS و (ج) AZCS مع مراكز الشحنة الموجبة والسالبة.
صغير جدًا لتحفيز الفصل الاتجاهي للإلكترونات والثقوب الناتجة عن الضوء، ويحدث إعادة تركيب شحنة شديدة. ومع ذلك، عندما يتم تعطيل ترتيب جميع خلايا الوحدة المرتبة جيدًا في بلورة ZnCdS، فإنه سيسبب توزيع غير متساوٍ للشحنة في الفضاء، مما يولد لحظات ثنائية القطب التي تحفز حقول ثنائية القطب قوية في كامل المحفز الضوئي. سيؤدي حقل ثنائي القطب الاتجاهي القوي إلى انحناء كبير في نطاق الطاقة في AZCS لتعزيز فصل الشحنة، مما يمكن أن يعزز النشاط التحفيزي الضوئي والاستقرار.
خصائص المحفزات الضوئية التي تم تصنيعها
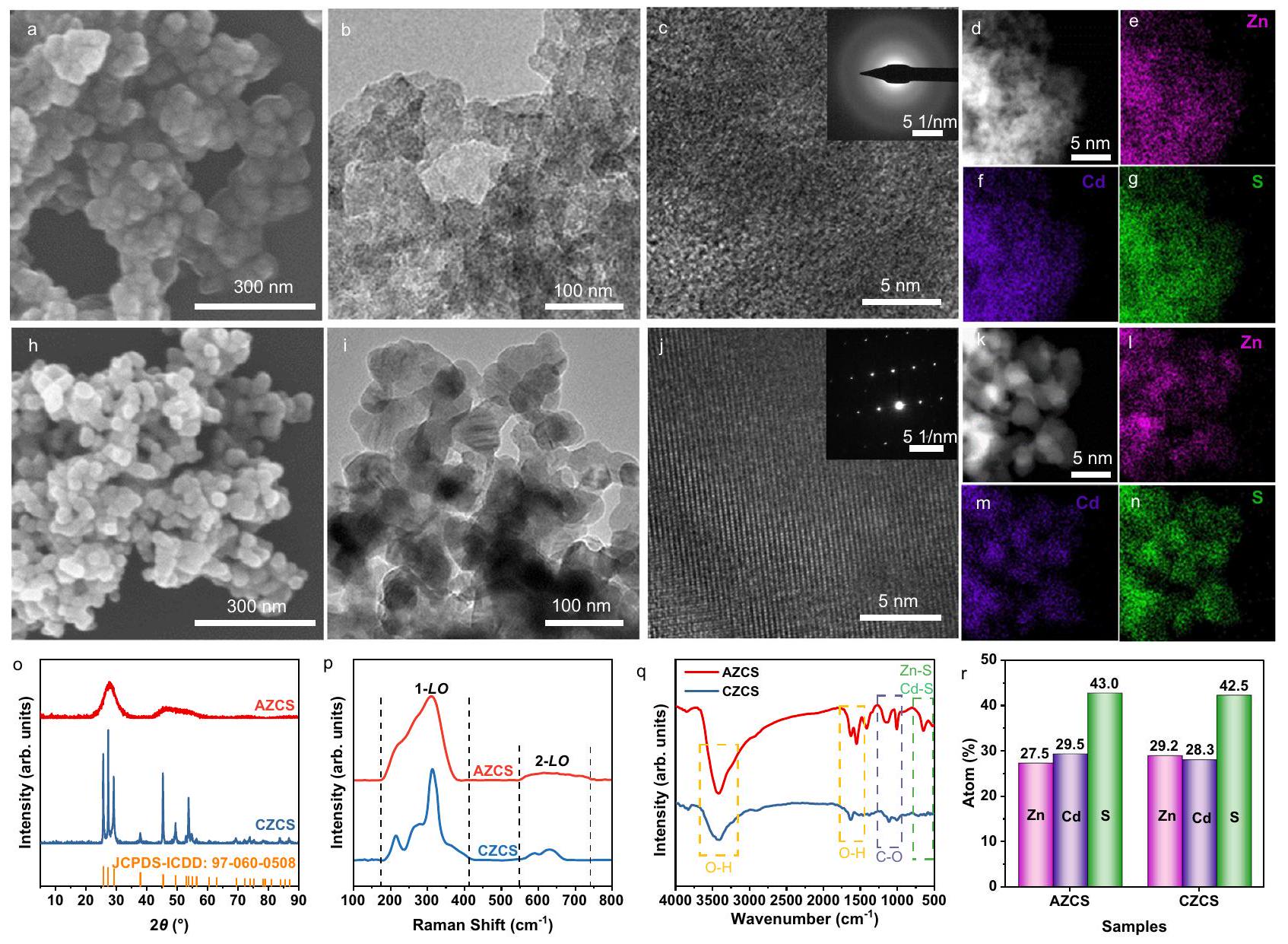
(HRTEM). كما هو موضح في الشكل 2أ، يتكون AZCS من جزيئات نانوية متصلة بحجم يقارب 42.4 نانومتر. لا يمكن ملاحظة حدود حبيبية حادة في صورة TEM (الشكل 2ب)، مما يشير إلى الخصائص غير البلورية. تُظهر صورة HRTEM لـ AZCS ترتيبًا ذريًا غير منظم بدون حواف شبكية واضحة (الشكل 2ج)، ونمط حيود الإلكترون في المنطقة المختارة (SAED) يظهر حلقات هالة مستمرة وسميكة بدون أي نقاط حيود مميزة (الإدراج في الشكل 2ج)، مما يشير إلى السمة غير البلورية لـ AZCS. يُظهر تخطيط طيف الأشعة السينية المشتتة للطاقة (EDS) لـ AZCS توزيعًا متجانسًا لعناصر
المعروضة في صورة TEM. لذلك، قد تكون قيم حجم الجسيمات التي تم قياسها بواسطة هاتين الطريقتين المختلفتين مختلفة، بينما يمكن مقارنة القيم التي تم قياسها بنفس الطريقة بشكل معقول. يتم عكس ترتيب الذرات المنظم من خلال الحواف الشبكية الواضحة في صورة HRTEM (الشكل 2ي)، وتظهر النقاط الأساسية في نمط SAED (الإدراج في الشكل 2ي) أن CZCS بلوري للغاية. يؤكد تخطيط EDS توزيعًا متجانسًا لـ
تحفيز ضوئي
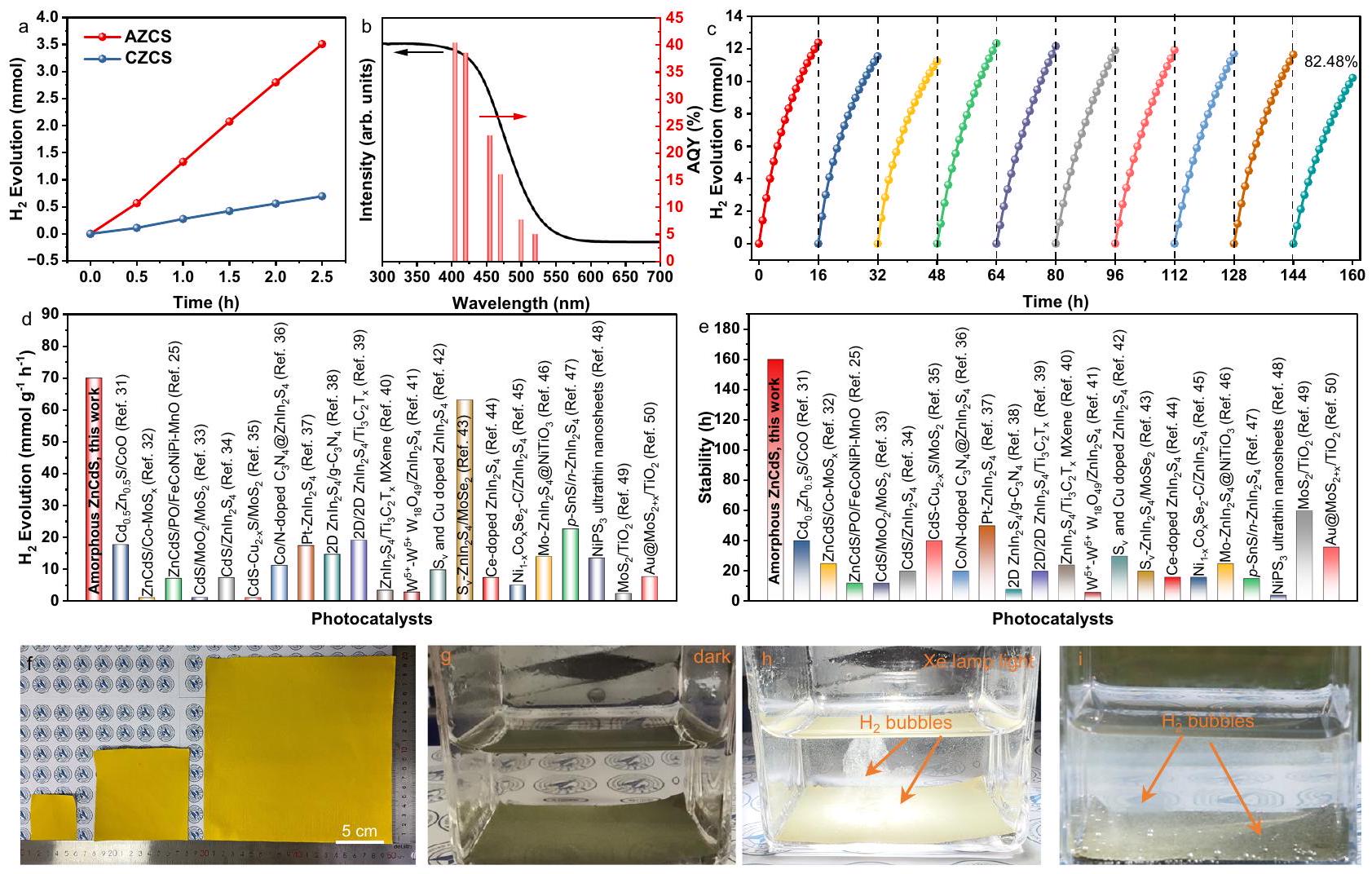
مختلف محفزات الكبريتيد الضوئية التي تم الإبلاغ عنها حتى الآن، (ف) أفلام محفز ضوئي مرنة بأحجام مختلفة
تقترح نفس آلية التحفيز الضوئي. على وجه التحديد، فإن قيم AQY لـ AZCS هي
محفزات ضوئية مختلفة من الكبريتيدات
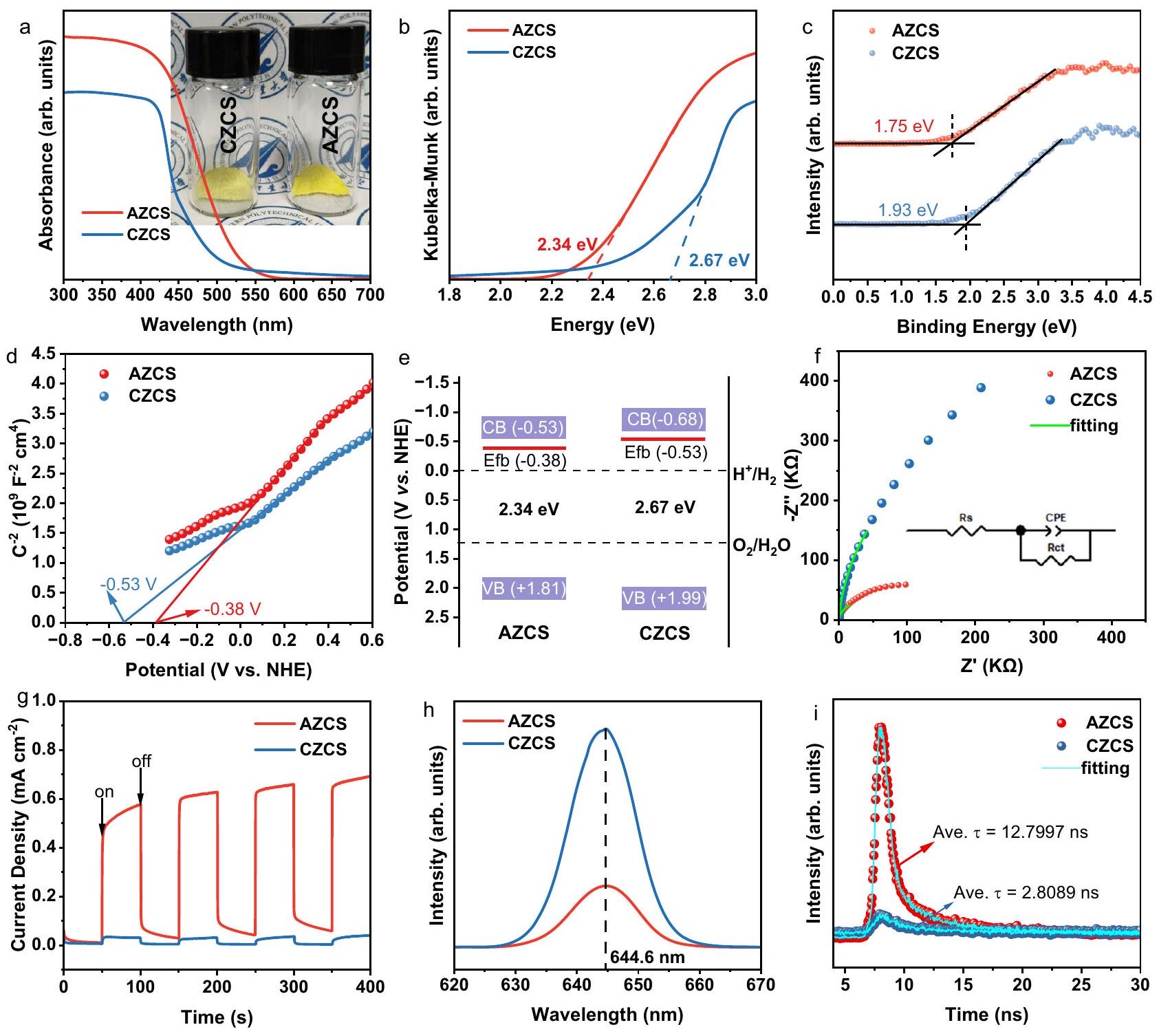
استكشاف آلية التحفيز الضوئي
ذروة انبعاث أضعف بين النطاقين عند 644 نانومتر مقارنة بنظيرها CZCS. يمكن تفسير نتيجة تلاشي PL من خلال تثبيط إعادة تركيب الشحنات الناتجة عن الترتيبات الذرية غير المنتظمة.
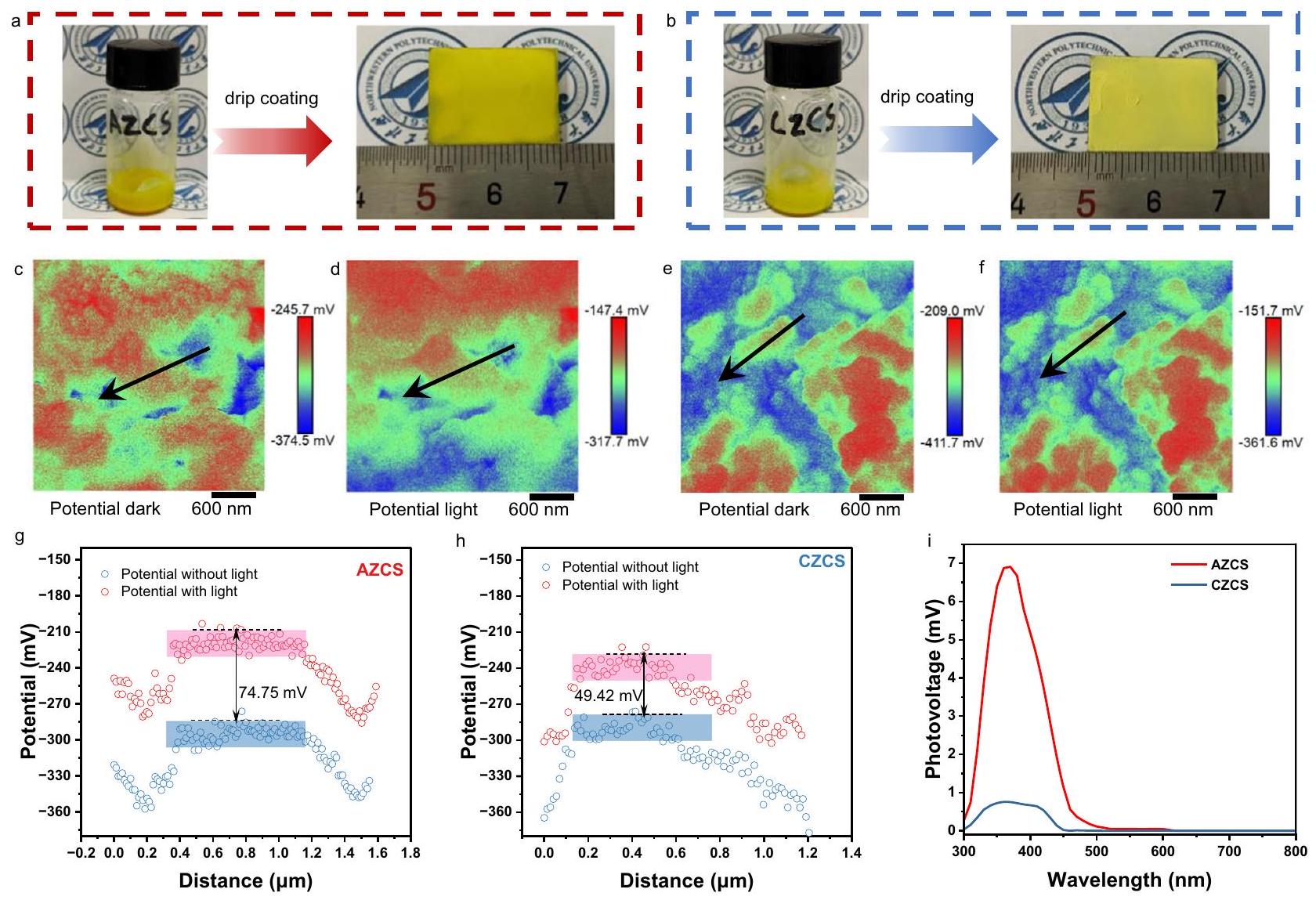
خصائص المجال ثنائي القطب
مع تغيير الموضع. علاوة على ذلك، يظهر AZCS مع الإضاءة الخفيفة زيادة في متوسط الجهد السطحي لـ
نقاش
طرق
تحضير المواد
إنوشيم،
توصيف
اختبارات التحفيز الضوئي
و
القياسات الكهروضوئية الكيميائية
حسابات DFT
of Zn و
توفر البيانات
References
- Mora Rollo, A., Rollo, A. & Mora, C. The tree-lined path to carbon neutrality. Nat. Rev. Earth Environ. 1, 332 (2020).
- Wang, Z., Li, C. & Domen, K. Recent developments in heterogeneous photocatalysts for solar-driven overall water splitting. Chem. Soc. Rev. 48, 2109-2125 (2019).
- Zhou, C., Wu, J., Li, Y. & Cao, H. Highly efficient UV-visible-infrared light-driven photothermocatalytic steam biomass reforming to
on Ni nanoparticles loaded on mesoporous silica. Energy Environ. Sci. 15, 3041-3050 (2022). - Wang, Q. et al. Scalable water splitting on particulate photocatalyst sheets with a solar-to-hydrogen energy conversion efficiency exceeding 1%. Nat. Mater. 15, 611-615 (2016).
- Wang, X. et al. Development of
-type photoanodes for photoelectrochemical water splitting. EcoEnergy 1, 108-153 (2023). - Hisatomi, T. & Domen, K. Reaction systems for solar hydrogen production via water splitting with particulate semiconductor photocatalysts. Nat. Catal. 2, 387-399 (2019).
- Yang, L. et al. Beyond
п-conjugated metal-free polymeric semiconductors for photocatalytic chemical transformations. Chem. Soc. Rev. 50, 2147-2172 (2021). - Guo, Y. et al. Concentrating electron and activating H-OH bond of absorbed water on metallic
boosting photocatalytic hydrogen evolution. Nano Energy 95, 107028 (2022). - Hu, Y. et al. Lattice distortion induced internal electric field in
photoelectrode for efficient charge separation and transfer. Nat. Commun. 11, 2129 (2020). - Si, Y. et al. The effect of directed photogenerated carrier separation on photocatalytic hydrogen production. Nano Energy 41, 488-493 (2017).
- Zhang, C. et al. Piezo-photocatalysis over metal-organic frameworks: promoting photocatalytic activity by Piezoelectric effect. Adv. Mater. 33, 2106308 (2021).
- Xu, Q., Zhang, L., Cheng, B., Fan, J. & Yu, J. S-scheme heterojunction photocatalyst. Chem 6, 1543-1559 (2020).
- Cui, Y. et al. Fluid-induced piezoelectric field enhancing photocatalytic hydrogen evolution reaction on
membrane. Nano Energy 99, 107429 (2022). - Li, H. et al. Enhanced ferroelectric-nanocrystal-based hybrid photocatalysis by ultrasonic-wave-generated Piezophototronic effect. Nano Lett. 15, 2372-2379 (2015).
- Zhang, J. et al. Boosting photocatalytic water splitting by tuning built-in electric field at phase junction. J. Mater. Chem. A 7, 10264-10272 (2019).
- Wang, Q. et al. Particulate photocatalyst sheets based on carbon conductor layer for efficient Z-scheme pure-water splitting at ambient pressure. J. Am. Chem. Soc. 139, 1675-1683 (2017).
-
. et al. Unique S -scheme heterojunctions in self-assembled hybrids for photoreduction. Nat. Commun. 11, 4613 (2020). - Wu, H. et al. Low-bias photoelectrochemical water splitting via mediating trap states and small polaron hopping. Nat. Commun. 13, 6231 (2022).
- Mu, L. et al. Enhancing charge separation on high symmetry
exposed with anisotropic facets for photocatalytic water splitting. Energy Environ. Sci. 9, 2463-2469 (2016). - Ma, Z. et al. Electrostatic potential of the incorporated asymmetry molecules induced high charge separation efficiency of the modified carbon nitride copolymers. Appl. Catal. B 319, 121922 (2022).
- Heckel, S. et al. Beyond Janus geometry: characterization of flow fields around nonspherical photocatalytic microswimmers. Adv. Sci. 9, 19-21 (2022).
- Zhang, Y. et al. Visualizing coherent intermolecular dipole-dipole coupling in real space. Nature 531, 623-627 (2016).
- Li, Z. et al. Dipole field in nitrogen-enriched carbon nitride with external forces to boost the artificial photosynthesis of hydrogen peroxide. Nat. Commun. 14, 5742 (2023).
- Wang, W. et al. Band-gap modulation for enhancing NO photocatalytic oxidation over hollow ZnCdS: a combined experimental and theoretical investigation. J. Phys. Chem. C 126, 3967-3979 (2022).
- Song, J. et al. Photochemical construction of the
FeCoNiPi-MnO composite for efficient tandem application of photocatalytic partial water splitting and overall water splitting. J. Mater. Chem. A 10, 16029-16036 (2022). - Wang, X. et al. Two-dimensional amorphous
nanosheets enabling high-efficiency photoinduced charge transfer for excellent SERS activity. J. Am. Chem. Soc. 141, 5856-5862 (2019). - Song, J., Zhao, H., Sun, R., Li, X. & Sun, D. An efficient hydrogen evolution catalyst composed of palladium phosphorous sulphide (
) and twin nanocrystal solid solution with both homo- and hetero-junctions. Energy Environ. Sci. 10, 225-235 (2017). - Liu, S. et al. Facilitating nitrogen accessibility to boron-rich covalent organic frameworks via electrochemical excitation for efficient nitrogen fixation. Nat. Commun. 10, 3898 (2019).
- Chen, Y. C. et al. Photocatalytic enhancement of hydrogen production in water splitting under simulated solar light by band gap engineering and localized surface plasmon resonance of
nanowires decorated by Au nanoparticles. Nano Energy 67, 104225 (2020). - Hsu, Y. Y. et al. Heterojunction of Zinc Blende/Wurtzite in
solid solution for efficient solar hydrogen generation: x-ray absorption/diffraction approaches. ACS Appl. Mater. Interfaces 7, 22558-22569 (2015). - Zhao, H., Guo, L., Xing, C., Liu, H. & Li, X. A homojunction-heterojunction-homojunction scaffold boosts photocatalytic
evolution over hybrids. J. Mater. Chem. A 8, 1955-1965 (2020). - Lei, Y. et al. Molybdenum sulfide cocatalyst activation upon photodeposition of cobalt for improved photocatalytic hydrogen production activity of ZnCdS. Chem. Eng. J. 425, 131478 (2021).
- Bie, C. et al. A bifunctional
catalyst enhances photocatalytic evolution and pyruvic acid synthesis. Angew. Chem. Int. Ed. 61, e202212045 (2022). - Li, C. Q. et al. Constructing direct Z-scheme heterostructure by enwrapping
on CdS hollow cube for efficient photocatalytic generation. Adv. Sci. 9, 2201773 (2022). - Liu, G. et al. MoS
-stratified core-shell nanorods for highly efficient photocatalytic hydrogen production. ACS Nano 14, 5468-5479 (2020). - Wang, S., Wang, Y., Zhang, S. L., Zang, S. Q. & Lou, X. W. Supporting ultrathin
nanosheets on -Doped graphitic carbon nanocages for efficient photocatalytic generation. Adv. Mater. 31, 1903404 (2019). - Shi, X . et al. Protruding Pt single-sites on hexagonal
to accelerate photocatalytic hydrogen evolution. Nat. Commun. 13, 1287 (2022). - Tan, M. et al. Boosting photocatalytic hydrogen production via interfacial engineering on 2D ultrathin Z-scheme ZnIn
heterojunction. Adv. Funct. Mater. 32, 2111740 (2022). - Su, T. et al. Sulfur vacancy and
cocatalyst synergistically boosting interfacial charge transfer in 2D/2D heterostructure for enhanced photocatalytic hydrogen evolution. Adv. Sci. 9, 2103715 (2022). - Zuo, G. et al. Ultrathin
nanosheets anchored on MXene for photocatalytic evolution. Angew. Chem. Int. Ed. 132, 11383-11388 (2020). - Lu, Y. et al.
pair induced LSPR of to sensitize for full-spectrum solar-light-driven photocatalytic hydrogen evolution. Adv. Funct. Mater. 32, 2203638 (2022). - Zhang, S. et al. Gradient hydrogen migration modulated with selfadapting S vacancy in copper-doped
nanosheet for photocatalytic hydrogen evolution. ACS Nano 15, 15238-15248 (2021). - Wang, X. et al. Interfacial chemical bond and internal electric field modulated Z-scheme Sv-ZnIn
photocatalyst for efficient hydrogen evolution. Nat. Commun. 12, 4112 (2021). - Fan, H., Jin, Y., Liu, K. & Liu, W. One-step MOF-templated strategy to fabrication of Ce-Doped
tetrakaidecahedron hollow nanocages as an efficient photocatalyst for hydrogen evolution. Adv. Sci. 9, 2104579 (2022). - Chao, Y. et al.
hybrid nanocages with strong 2D/2D hetero-interface interaction enable efficient -releasing photocatalysis. Adv. Funct. Mater. 31, 2100923 (2021). - Zhu, J. et al. Mo-modified
-scheme heterojunction with enhanced interfacial electric field for efficient visible-lightdriven hydrogen evolution. Adv. Funct. Mater. 33, 2213131 (2023). - Jia, X. et al. Interfacial mediation by Sn and S vacancies of p-SnS/n
for enhancing photocatalytic hydrogen evolution with new scheme of Type-I Heterojunction. Adv. Funct. Mater. 33, 2304072 (2023). - Ran, J. et al.
ultrathin nanosheets as versatile platform advancing highly active photocatalytic production. Nat. Commun. 13, 4600 (2022). - Wang, W. et al. Edge-enriched ultrathin
embedded yolk-shell with boosted charge transfer for superior photocatalytic evolution. Adv. Funct. Mater. 29, 1901958 (2019). - Gao, D. et al. Reversing free-electron transfer of
cocatalyst for optimizing antibonding-orbital occupancy enables high photocatalytic evolution. Angew. Chem. Int. Ed. 62, e202304559 (2023). - Sharma, K. et al. Sulphur vacancy defects engineered metal sulfides for amended photo(electro)catalytic water splitting: a review. J. Mater. Sci. Technol. 152, 50-64 (2023).
- Xiao, J. et al. Simultaneously tuning the defects and surface properties of
nanoparticles by codoping for significantly accelerated photocatalytic evolution. J. Am. Chem. Soc. 143, 10059-10064 (2021). - Wang, X., Liu, B., Xiao, X., Wang, S. & Huang, W. Boron dopant simultaneously achieving nanostructure control and electronic structure tuning of graphitic carbon nitride with enhanced photocatalytic activity. J. Mater. Chem. C 9, 14876-14884 (2021).
- Wang, S. et al. Boosting the photocatalytic hydrogen production performance of graphitic carbon nitride nanosheets by tailoring the cyano groups. J. Colloid Interface Sci. 610, 495-503 (2022).
- Lin, Z., Du, C., Yan, B., Wang, C. & Yang, G. Two-dimensional amorphous NiO as a plasmonic photocatalyst for solar
evolution. Nat. Commun. 9, 4036 (2018). - Kang, Y. et al. An amorphous carbon nitride photocatalyst with greatly extended visible-light-responsive range for photocatalytic hydrogen generation. Adv. Mater. 27, 4572-4577 (2015).
- Zhang, L. J., Li, S., Liu, B. K., Wang, D. J. & Xie, T. F. Highly efficient
photocatalysts: Z-scheme photocatalytic mechanism for
their enhanced photocatalyticevolution under visible light. ACS Catal 4, 3724-3729 (2014). - Sheng, Y., Li, W., Xu, L. & Zhu, Y. High photocatalytic oxygen evolution via strong built-in electric field induced by high crystallinity of perylene imide supramolecule. Adv. Mater. 34, 2102354 (2022).
- Wang, S. et al. One-step supramolecular preorganization constructed crinkly graphitic carbon nitride nanosheets with enhanced photocatalytic activity. J. Mater. Sci. Technol. 104, 155-162 (2022).
- Kresse, G. & Hafner, J. Ab initio molecular dynamics for liquid metals. Phys. Rev. B 47, 558-561 (1993).
- Kresse, G. & Furthmüller, J. Efficient iterative schemes for ab initio total-energy calculations using a plane-wave basis set. Phys. Rev. B Condens. Matter Mater. Phys. 54, 11169-11186 (1996).
- Perdew, J. P., Burke, K. & Ernzerhof, M. Generalized gradient approximation made simple. Phys. Rev. Lett. 77, 3865-3868 (1996).
- Blöchl, P. E. Projector augmented-wave method. Phys. Rev. B 50, 17953-17979 (1994).
- Biswas, A., Meher, S. R. & Kaushik, D. K. Electronic and band structure calculation of Wurtzite CdS using GGA and GGA+U functionals. J. Phys. Conf. Ser. 2267, 012155 (2022).
- Jiang, H., Gomez-Abal, R. I., Rinke, P. & Scheffler, M. First-principles modeling of localized d states with the GW@LDA+U approach. Phys. Rev. B Condens. Matter Mater. Phys. 82, 045108 (2010).
شكر وتقدير
مساهمات المؤلفين
التوصيف. قام X.W. و S.W. و L.W. و G.Z. و W.H. بتحليل البيانات وإعداد المخطوطة. علق جميع المؤلفين ووافقوا على الورقة.
المصالح المتنافسة
معلومات إضافية
المواد التكميلية متاحة على
https://doi.org/10.1038/s41467-024-47022-z.
يجب توجيه المراسلات والطلبات للحصول على المواد إلى ليانزهو وانغ، غانغكيانغ تشو، وي هاي، أو سونغكان وانغ.
http://www.nature.com/reprints
ملاحظة الناشر: تظل شركة سبرينجر ناتشر محايدة فيما يتعلق بالمطالبات القضائية في الخرائط المنشورة والانتماءات المؤسسية.
© المؤلف(ون) 2024
مركز العلوم الحدودية للإلكترونيات المرنة، معهد الإلكترونيات المرنة في شيان (IFE)، جامعة شمال غرب بوليتكنيك، 127 طريق يويي الغربي، شيان 710072، الصين. مركز المواد النانوية، المعهد الأسترالي للهندسة الحيوية والتكنولوجيا النانوية ومدرسة الهندسة الكيميائية، جامعة كوينزلاند، بريسبان، كوينزلاند 4072، أستراليا. كلية الفيزياء وتكنولوجيا المعلومات، جامعة شاندونغ العادية، شيآن 710062، الصين.
البريد الإلكتروني: l.wang@uq.edu.au; zgq2006@snnu.edu.cn; iamwhuang@nwpu.edu.cn; iamscwang@nwpu.edu.cn
DOI: https://doi.org/10.1038/s41467-024-47022-z
PMID: https://pubmed.ncbi.nlm.nih.gov/38521830
Publication Date: 2024-03-23
Induced dipole moments in amorphous ZnCdS catalysts facilitate photocatalytic
Accepted: 18 March 2024
Published online: 23 March 2024
(A) Check for updates
Abstract
Amorphous semiconductors without perfect crystalline lattice structures are usually considered to be unfavorable for photocatalysis due to the presence of enriched trap states and defects. Here we demonstrate that breaking longrange atomic order in an amorphous ZnCdS photocatalyst can induce dipole moments and generate strong electric fields within the particles which facilitates charge separation and transfer. Loading
photogenerated electron-hole pairs can be significantly improved, the photogenerated electrons and holes can be consumed in the surface photocatalytic reactions, and thus side-reactions between the photogenerated charge carriers and the photocatalyst itself can be eliminated. During a photocatalytic process, the photogenerated electrons and holes are transported randomly within a particulate photocatalyst due to the lack of directed electric field
Results
Mechanism of amorphous structure induced dipole fields



0.30 e


crystallographic directions. Schematics of (f) CZCS and (g) AZCS structures with positive and negative charge centers.

small to drive the directional separation of the photogenerated electrons and holes, and severe charge recombination occurs. However, when the order of all well-arranged unit cells in the ZnCdS crystal are disrupted, it will cause uneven charge distribution in space, thereby generating dipole moments that induce strong dipole fields in the entire photocatalyst. The strong directional dipole field will cause a large energy band bending in AZCS to promote charge separation, which can enhance the photocatalytic activity and stability.
Characterizations of the as-synthesized photocatalysts
(HRTEM). As shown in Fig. 2a, AZCS is composed of connected nanoparticles with a size of approximately 42.4 nm . No sharp grain boundaries can be observed in the TEM image (Fig. 2b), indicating the amorphous characteristics. The HRTEM image of AZCS shows disordered atomic arrangement without obvious lattice fringes (Fig. 2c), and the selected area electron diffraction (SAED) pattern exhibits diffused continuous and thick halo rings without any distinguishable diffraction spots (inset in Fig. 2c), indicating the amorphous feature of AZCS. Energy dispersive X-ray spectrometry (EDS) mapping of AZCS demonstrates the homogeneous distribution of
particles shown in the TEM image. Therefore, the particle size values measured by these two different methods may be different, while the values measured by the same method can be reasonably compared. The ordered atomic arrangement is reflected by the clear lattice fringes in the HRTEM image (Fig. 2j), and the matrix spots in the SAED pattern (inset in Fig. 2j) demonstrate that CZCS is highly crystalline. EDS mapping confirms the homogeneous distribution of
Photocatalytic

different sulfide photocatalysts reported so far, (f) Flexible photocatalyst films of different sizes
suggesting the same photocatalytic mechanism. Specifically, the AQY values of AZCS are
various sulfide photocatalysts

Photocatalytic mechanism exploration

weaker band-to-band emission peak at 644 nm than its CZCS counterpart. The PL quenching result could be explained by the inhibition of charge recombination from the disorder atomic arrangements
Dipole field characterizations
with the change of position. Furthermore, AZCS with light illumination exhibits an increase average surface potential of
Discussion
Methods
Materials preparation
(Innochem,
Characterization
Photocatalytic tests
and
Photoelectrochemical measurements
DFT calculations
of Zn and
Data availability
References
- Mora Rollo, A., Rollo, A. & Mora, C. The tree-lined path to carbon neutrality. Nat. Rev. Earth Environ. 1, 332 (2020).
- Wang, Z., Li, C. & Domen, K. Recent developments in heterogeneous photocatalysts for solar-driven overall water splitting. Chem. Soc. Rev. 48, 2109-2125 (2019).
- Zhou, C., Wu, J., Li, Y. & Cao, H. Highly efficient UV-visible-infrared light-driven photothermocatalytic steam biomass reforming to
on Ni nanoparticles loaded on mesoporous silica. Energy Environ. Sci. 15, 3041-3050 (2022). - Wang, Q. et al. Scalable water splitting on particulate photocatalyst sheets with a solar-to-hydrogen energy conversion efficiency exceeding 1%. Nat. Mater. 15, 611-615 (2016).
- Wang, X. et al. Development of
-type photoanodes for photoelectrochemical water splitting. EcoEnergy 1, 108-153 (2023). - Hisatomi, T. & Domen, K. Reaction systems for solar hydrogen production via water splitting with particulate semiconductor photocatalysts. Nat. Catal. 2, 387-399 (2019).
- Yang, L. et al. Beyond
п-conjugated metal-free polymeric semiconductors for photocatalytic chemical transformations. Chem. Soc. Rev. 50, 2147-2172 (2021). - Guo, Y. et al. Concentrating electron and activating H-OH bond of absorbed water on metallic
boosting photocatalytic hydrogen evolution. Nano Energy 95, 107028 (2022). - Hu, Y. et al. Lattice distortion induced internal electric field in
photoelectrode for efficient charge separation and transfer. Nat. Commun. 11, 2129 (2020). - Si, Y. et al. The effect of directed photogenerated carrier separation on photocatalytic hydrogen production. Nano Energy 41, 488-493 (2017).
- Zhang, C. et al. Piezo-photocatalysis over metal-organic frameworks: promoting photocatalytic activity by Piezoelectric effect. Adv. Mater. 33, 2106308 (2021).
- Xu, Q., Zhang, L., Cheng, B., Fan, J. & Yu, J. S-scheme heterojunction photocatalyst. Chem 6, 1543-1559 (2020).
- Cui, Y. et al. Fluid-induced piezoelectric field enhancing photocatalytic hydrogen evolution reaction on
membrane. Nano Energy 99, 107429 (2022). - Li, H. et al. Enhanced ferroelectric-nanocrystal-based hybrid photocatalysis by ultrasonic-wave-generated Piezophototronic effect. Nano Lett. 15, 2372-2379 (2015).
- Zhang, J. et al. Boosting photocatalytic water splitting by tuning built-in electric field at phase junction. J. Mater. Chem. A 7, 10264-10272 (2019).
- Wang, Q. et al. Particulate photocatalyst sheets based on carbon conductor layer for efficient Z-scheme pure-water splitting at ambient pressure. J. Am. Chem. Soc. 139, 1675-1683 (2017).
-
. et al. Unique S -scheme heterojunctions in self-assembled hybrids for photoreduction. Nat. Commun. 11, 4613 (2020). - Wu, H. et al. Low-bias photoelectrochemical water splitting via mediating trap states and small polaron hopping. Nat. Commun. 13, 6231 (2022).
- Mu, L. et al. Enhancing charge separation on high symmetry
exposed with anisotropic facets for photocatalytic water splitting. Energy Environ. Sci. 9, 2463-2469 (2016). - Ma, Z. et al. Electrostatic potential of the incorporated asymmetry molecules induced high charge separation efficiency of the modified carbon nitride copolymers. Appl. Catal. B 319, 121922 (2022).
- Heckel, S. et al. Beyond Janus geometry: characterization of flow fields around nonspherical photocatalytic microswimmers. Adv. Sci. 9, 19-21 (2022).
- Zhang, Y. et al. Visualizing coherent intermolecular dipole-dipole coupling in real space. Nature 531, 623-627 (2016).
- Li, Z. et al. Dipole field in nitrogen-enriched carbon nitride with external forces to boost the artificial photosynthesis of hydrogen peroxide. Nat. Commun. 14, 5742 (2023).
- Wang, W. et al. Band-gap modulation for enhancing NO photocatalytic oxidation over hollow ZnCdS: a combined experimental and theoretical investigation. J. Phys. Chem. C 126, 3967-3979 (2022).
- Song, J. et al. Photochemical construction of the
FeCoNiPi-MnO composite for efficient tandem application of photocatalytic partial water splitting and overall water splitting. J. Mater. Chem. A 10, 16029-16036 (2022). - Wang, X. et al. Two-dimensional amorphous
nanosheets enabling high-efficiency photoinduced charge transfer for excellent SERS activity. J. Am. Chem. Soc. 141, 5856-5862 (2019). - Song, J., Zhao, H., Sun, R., Li, X. & Sun, D. An efficient hydrogen evolution catalyst composed of palladium phosphorous sulphide (
) and twin nanocrystal solid solution with both homo- and hetero-junctions. Energy Environ. Sci. 10, 225-235 (2017). - Liu, S. et al. Facilitating nitrogen accessibility to boron-rich covalent organic frameworks via electrochemical excitation for efficient nitrogen fixation. Nat. Commun. 10, 3898 (2019).
- Chen, Y. C. et al. Photocatalytic enhancement of hydrogen production in water splitting under simulated solar light by band gap engineering and localized surface plasmon resonance of
nanowires decorated by Au nanoparticles. Nano Energy 67, 104225 (2020). - Hsu, Y. Y. et al. Heterojunction of Zinc Blende/Wurtzite in
solid solution for efficient solar hydrogen generation: x-ray absorption/diffraction approaches. ACS Appl. Mater. Interfaces 7, 22558-22569 (2015). - Zhao, H., Guo, L., Xing, C., Liu, H. & Li, X. A homojunction-heterojunction-homojunction scaffold boosts photocatalytic
evolution over hybrids. J. Mater. Chem. A 8, 1955-1965 (2020). - Lei, Y. et al. Molybdenum sulfide cocatalyst activation upon photodeposition of cobalt for improved photocatalytic hydrogen production activity of ZnCdS. Chem. Eng. J. 425, 131478 (2021).
- Bie, C. et al. A bifunctional
catalyst enhances photocatalytic evolution and pyruvic acid synthesis. Angew. Chem. Int. Ed. 61, e202212045 (2022). - Li, C. Q. et al. Constructing direct Z-scheme heterostructure by enwrapping
on CdS hollow cube for efficient photocatalytic generation. Adv. Sci. 9, 2201773 (2022). - Liu, G. et al. MoS
-stratified core-shell nanorods for highly efficient photocatalytic hydrogen production. ACS Nano 14, 5468-5479 (2020). - Wang, S., Wang, Y., Zhang, S. L., Zang, S. Q. & Lou, X. W. Supporting ultrathin
nanosheets on -Doped graphitic carbon nanocages for efficient photocatalytic generation. Adv. Mater. 31, 1903404 (2019). - Shi, X . et al. Protruding Pt single-sites on hexagonal
to accelerate photocatalytic hydrogen evolution. Nat. Commun. 13, 1287 (2022). - Tan, M. et al. Boosting photocatalytic hydrogen production via interfacial engineering on 2D ultrathin Z-scheme ZnIn
heterojunction. Adv. Funct. Mater. 32, 2111740 (2022). - Su, T. et al. Sulfur vacancy and
cocatalyst synergistically boosting interfacial charge transfer in 2D/2D heterostructure for enhanced photocatalytic hydrogen evolution. Adv. Sci. 9, 2103715 (2022). - Zuo, G. et al. Ultrathin
nanosheets anchored on MXene for photocatalytic evolution. Angew. Chem. Int. Ed. 132, 11383-11388 (2020). - Lu, Y. et al.
pair induced LSPR of to sensitize for full-spectrum solar-light-driven photocatalytic hydrogen evolution. Adv. Funct. Mater. 32, 2203638 (2022). - Zhang, S. et al. Gradient hydrogen migration modulated with selfadapting S vacancy in copper-doped
nanosheet for photocatalytic hydrogen evolution. ACS Nano 15, 15238-15248 (2021). - Wang, X. et al. Interfacial chemical bond and internal electric field modulated Z-scheme Sv-ZnIn
photocatalyst for efficient hydrogen evolution. Nat. Commun. 12, 4112 (2021). - Fan, H., Jin, Y., Liu, K. & Liu, W. One-step MOF-templated strategy to fabrication of Ce-Doped
tetrakaidecahedron hollow nanocages as an efficient photocatalyst for hydrogen evolution. Adv. Sci. 9, 2104579 (2022). - Chao, Y. et al.
hybrid nanocages with strong 2D/2D hetero-interface interaction enable efficient -releasing photocatalysis. Adv. Funct. Mater. 31, 2100923 (2021). - Zhu, J. et al. Mo-modified
-scheme heterojunction with enhanced interfacial electric field for efficient visible-lightdriven hydrogen evolution. Adv. Funct. Mater. 33, 2213131 (2023). - Jia, X. et al. Interfacial mediation by Sn and S vacancies of p-SnS/n
for enhancing photocatalytic hydrogen evolution with new scheme of Type-I Heterojunction. Adv. Funct. Mater. 33, 2304072 (2023). - Ran, J. et al.
ultrathin nanosheets as versatile platform advancing highly active photocatalytic production. Nat. Commun. 13, 4600 (2022). - Wang, W. et al. Edge-enriched ultrathin
embedded yolk-shell with boosted charge transfer for superior photocatalytic evolution. Adv. Funct. Mater. 29, 1901958 (2019). - Gao, D. et al. Reversing free-electron transfer of
cocatalyst for optimizing antibonding-orbital occupancy enables high photocatalytic evolution. Angew. Chem. Int. Ed. 62, e202304559 (2023). - Sharma, K. et al. Sulphur vacancy defects engineered metal sulfides for amended photo(electro)catalytic water splitting: a review. J. Mater. Sci. Technol. 152, 50-64 (2023).
- Xiao, J. et al. Simultaneously tuning the defects and surface properties of
nanoparticles by codoping for significantly accelerated photocatalytic evolution. J. Am. Chem. Soc. 143, 10059-10064 (2021). - Wang, X., Liu, B., Xiao, X., Wang, S. & Huang, W. Boron dopant simultaneously achieving nanostructure control and electronic structure tuning of graphitic carbon nitride with enhanced photocatalytic activity. J. Mater. Chem. C 9, 14876-14884 (2021).
- Wang, S. et al. Boosting the photocatalytic hydrogen production performance of graphitic carbon nitride nanosheets by tailoring the cyano groups. J. Colloid Interface Sci. 610, 495-503 (2022).
- Lin, Z., Du, C., Yan, B., Wang, C. & Yang, G. Two-dimensional amorphous NiO as a plasmonic photocatalyst for solar
evolution. Nat. Commun. 9, 4036 (2018). - Kang, Y. et al. An amorphous carbon nitride photocatalyst with greatly extended visible-light-responsive range for photocatalytic hydrogen generation. Adv. Mater. 27, 4572-4577 (2015).
- Zhang, L. J., Li, S., Liu, B. K., Wang, D. J. & Xie, T. F. Highly efficient
photocatalysts: Z-scheme photocatalytic mechanism for
their enhanced photocatalyticevolution under visible light. ACS Catal 4, 3724-3729 (2014). - Sheng, Y., Li, W., Xu, L. & Zhu, Y. High photocatalytic oxygen evolution via strong built-in electric field induced by high crystallinity of perylene imide supramolecule. Adv. Mater. 34, 2102354 (2022).
- Wang, S. et al. One-step supramolecular preorganization constructed crinkly graphitic carbon nitride nanosheets with enhanced photocatalytic activity. J. Mater. Sci. Technol. 104, 155-162 (2022).
- Kresse, G. & Hafner, J. Ab initio molecular dynamics for liquid metals. Phys. Rev. B 47, 558-561 (1993).
- Kresse, G. & Furthmüller, J. Efficient iterative schemes for ab initio total-energy calculations using a plane-wave basis set. Phys. Rev. B Condens. Matter Mater. Phys. 54, 11169-11186 (1996).
- Perdew, J. P., Burke, K. & Ernzerhof, M. Generalized gradient approximation made simple. Phys. Rev. Lett. 77, 3865-3868 (1996).
- Blöchl, P. E. Projector augmented-wave method. Phys. Rev. B 50, 17953-17979 (1994).
- Biswas, A., Meher, S. R. & Kaushik, D. K. Electronic and band structure calculation of Wurtzite CdS using GGA and GGA+U functionals. J. Phys. Conf. Ser. 2267, 012155 (2022).
- Jiang, H., Gomez-Abal, R. I., Rinke, P. & Scheffler, M. First-principles modeling of localized d states with the GW@LDA+U approach. Phys. Rev. B Condens. Matter Mater. Phys. 82, 045108 (2010).
Acknowledgements
Author contributions
characterization. X.W., S.W., L.W., G.Z., and W.H. analyzed the data and prepared the manuscript. All the authors commented and approved the paper.
Competing interests
Additional information
supplementary material available at
https://doi.org/10.1038/s41467-024-47022-z.
Correspondence and requests for materials should be addressed to Lianzhou Wang, Gangqiang Zhu, Wei Huang or Songcan Wang.
http://www.nature.com/reprints
Publisher’s note Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.
© The Author(s) 2024
Frontiers Science Center for Flexible Electronics, Xi’an Institute of Flexible Electronics (IFE), Northwestern Polytechnical University, 127 West Youyi Road, Xi’an 710072, China. Nanomaterials Centre, Australian Institute for Bioengineering and Nanotechnology and School of Chemical Engineering, The University of Queensland, Brisbane, QLD 4072, Australia. School of Physics and Information Technology, Shaanxi Normal University, Xi’an 710062, China.
-e-mail: l.wang@uq.edu.au; zgq2006@snnu.edu.cn; iamwhuang@nwpu.edu.cn; iamscwang@nwpu.edu.cn
