DOI: https://doi.org/10.1038/s41586-024-08426-5
PMID: https://pubmed.ncbi.nlm.nih.gov/39814891
تاريخ النشر: 2025-01-15
تفعيل IL-33 للخلايا اللمفاوية التائية المساعدة من النوع 2 يحفز تشكيل الهياكل اللمفاوية الثلاثية في سرطان البنكرياس
تاريخ الاستلام: 25 أكتوبر 2021
تم القبول: 19 نوفمبر 2024
نُشر على الإنترنت: 15 يناير 2025
الوصول المفتوح
تحقق من التحديثات
الملخص
الهياكل اللمفاوية الثانوية (TLSs) هي تجمعات لمفاوية خارجية تتشكل من جديد وتنظم المناعة في الأنسجة الملتهبة بشكل مزمن، بما في ذلك الأورام. على الرغم من أن TLSs تتشكل نتيجة لتنشيط مسار مستقبلات اللمفوتوكسين (LT)-LTβ بسبب الالتهاب.
الأعضاء اللمفاوية خارج الموقع، المعروفة باسم TLSs، هي هياكل شائعة تنظم المناعة في الأنسجة الملتهبة بشكل مزمن.
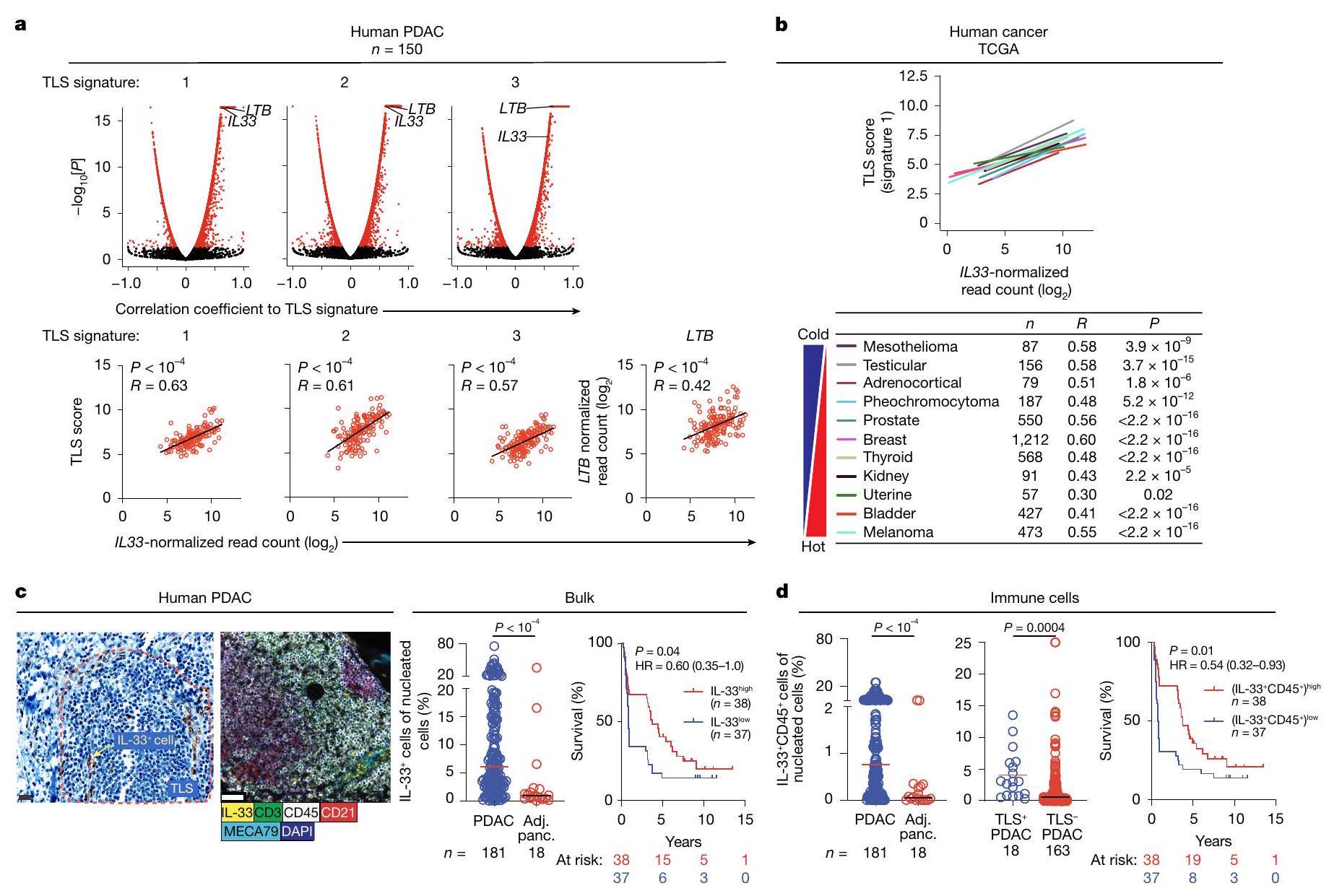
البقاء
التي يتم تشكيلها، تتجمع TLSs من جديد في الأنسجة الملتهبة بشكل مزمن. وبالتالي، فإن المحركات والخلايا المستحثة بواسطة الالتهاب التي تحفز TLSs لا تزال غير محددة بشكل كامل.
IL-33 يتوسط تكوين الأوعية اللمفاوية
(الشكل 1c (يسار)، الشكل البياني الممتد 1c، d والجدول التكميلي 2) التي كانت أكثر وفرة في الأورام مقارنة بالأنسجة البنكرياسية المجاورة (الشكل 1c (وسط) و1d (يسار))، وكانت غنية في الأورام التي تحتوي على TLSs مقارنة بتلك التي لا تحتوي عليها (الشكل 1d (وسط)). علاوة على ذلك، كانت مستويات IL- داخل الورم أعلى…
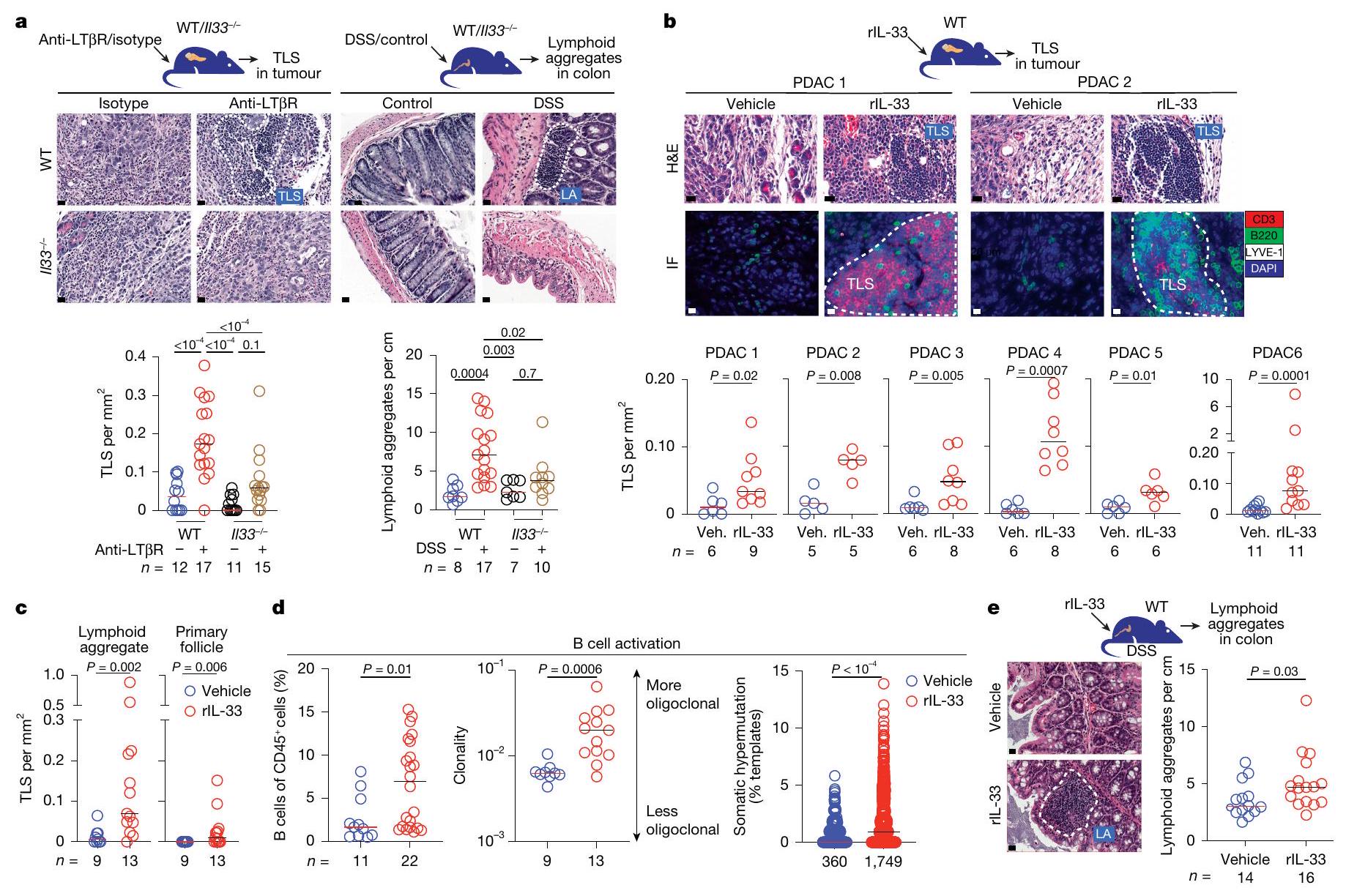
في الفئران المصابة بالتهاب القولون الناتج عن DSS والمعالجة بالسيارة والمعالجة بـ rIL-33. تم جمع البيانات بعد أسبوعين (
فقدان الوزن وزيادة بقاء الفئران (الشكل 2g من البيانات الموسعة). وبالتالي، فإن الألارمين IL-33 يحفز تكوين الأوعية اللمفاوية في السرطان والالتهاب.
IL-33 يوسع ILC2s اللمفاوية
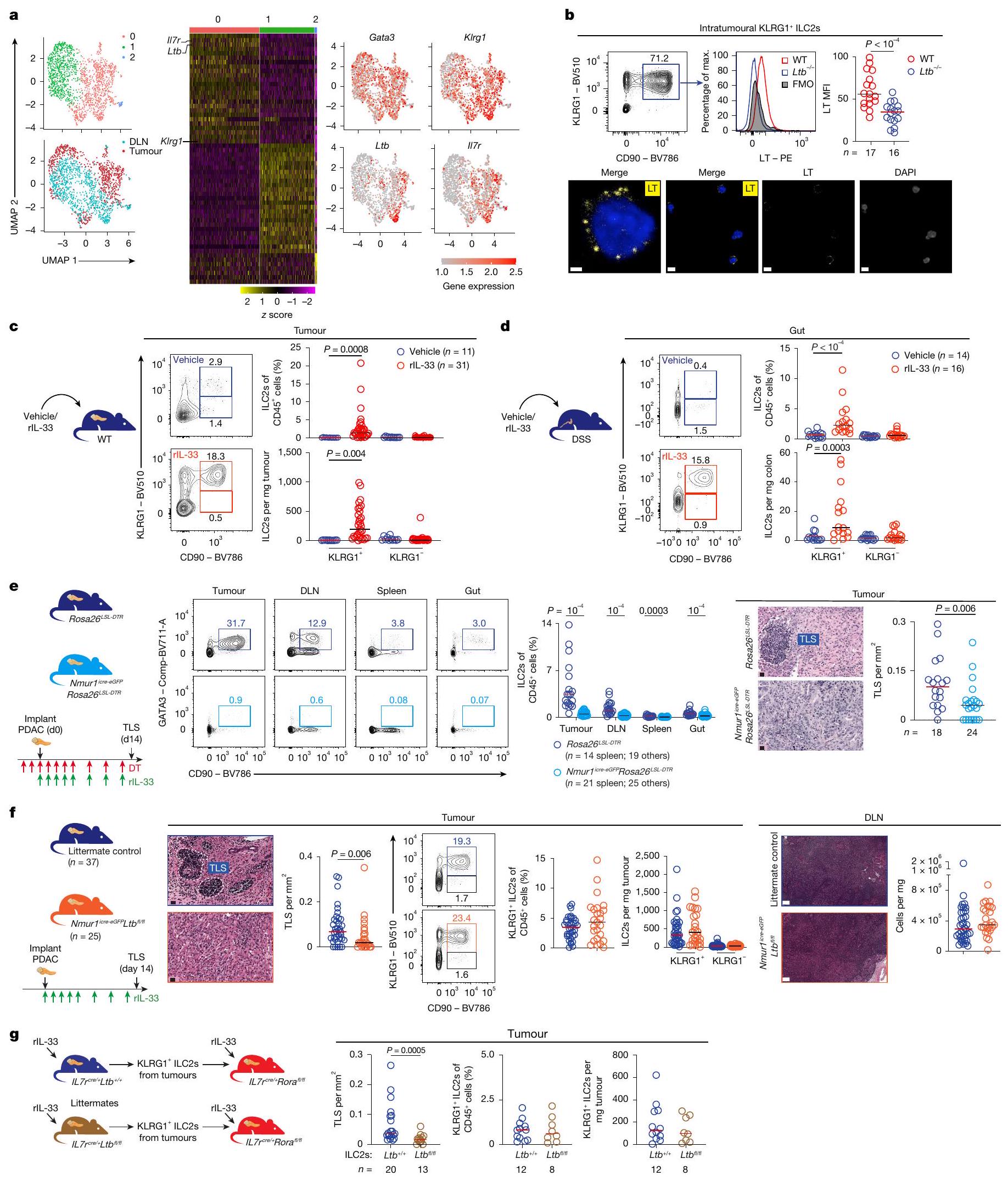
وعدد خلايا المناعة DLN (يمين) في Nmur1 المعالجة بـ rlL-33
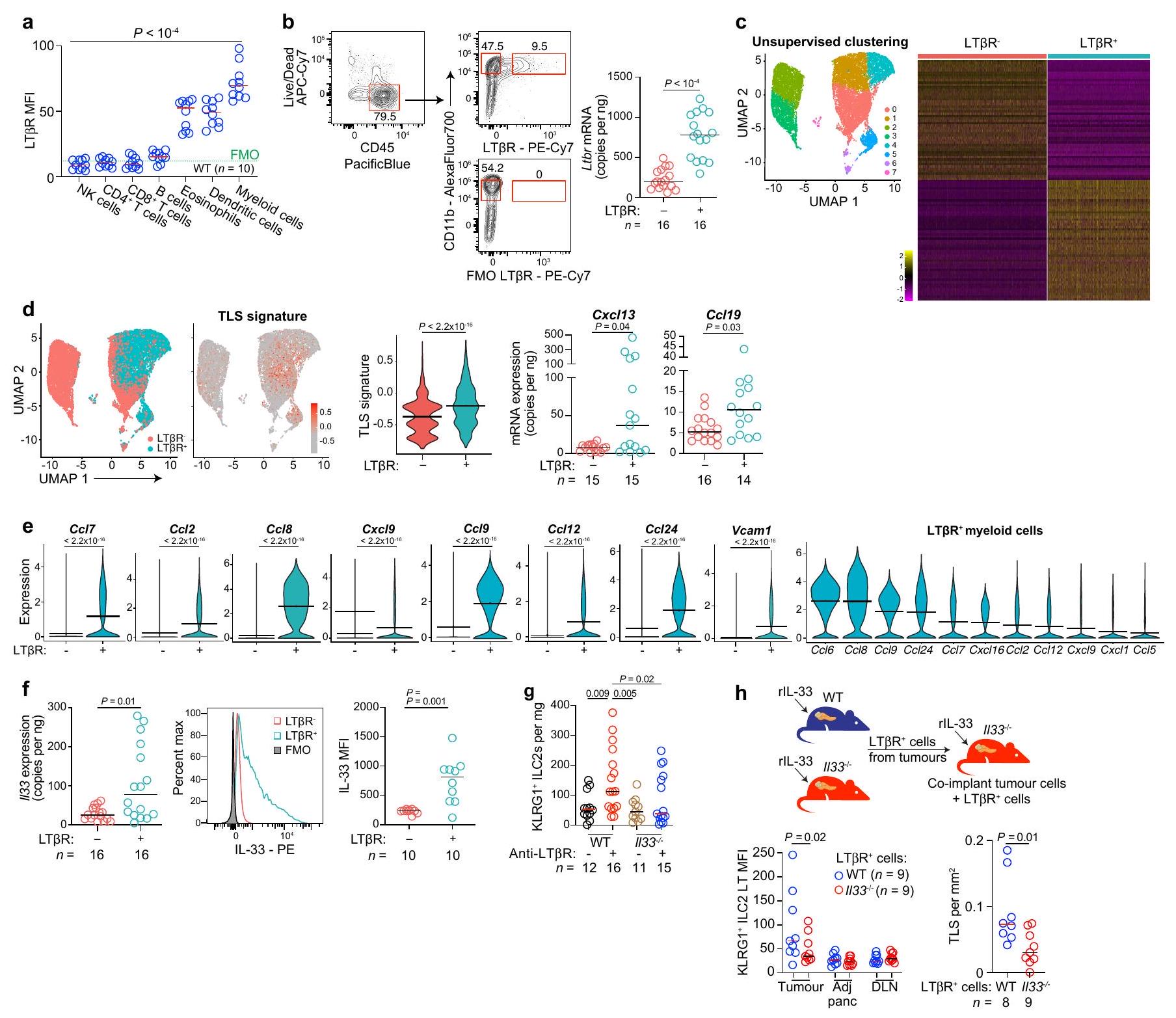
في SLOs و TLSs، تعبر خلايا المحفز عن LT الذي يرتبط بـ LTβR على خلايا منظم TLS لتحفيز التعبير عن الكيموكينات وجزيئات الالتصاق، وتنسيق تكوين الأنسجة اللمفاوية.
نسخة متميزة من النسخ الجينية (الشكل التوضيحي الممتد 5ب-هـ والجدول التكميلية 4)، مع كيموكينات تحفز TLS أعلى، بما في ذلك Cxcl13
يمكن لخلايا ILC2s اللمفاوية أن تهاجر من الأمعاء
حيث يمكن لخلايا ILC2s الهجرة إلى الأنسجة من الأمعاء
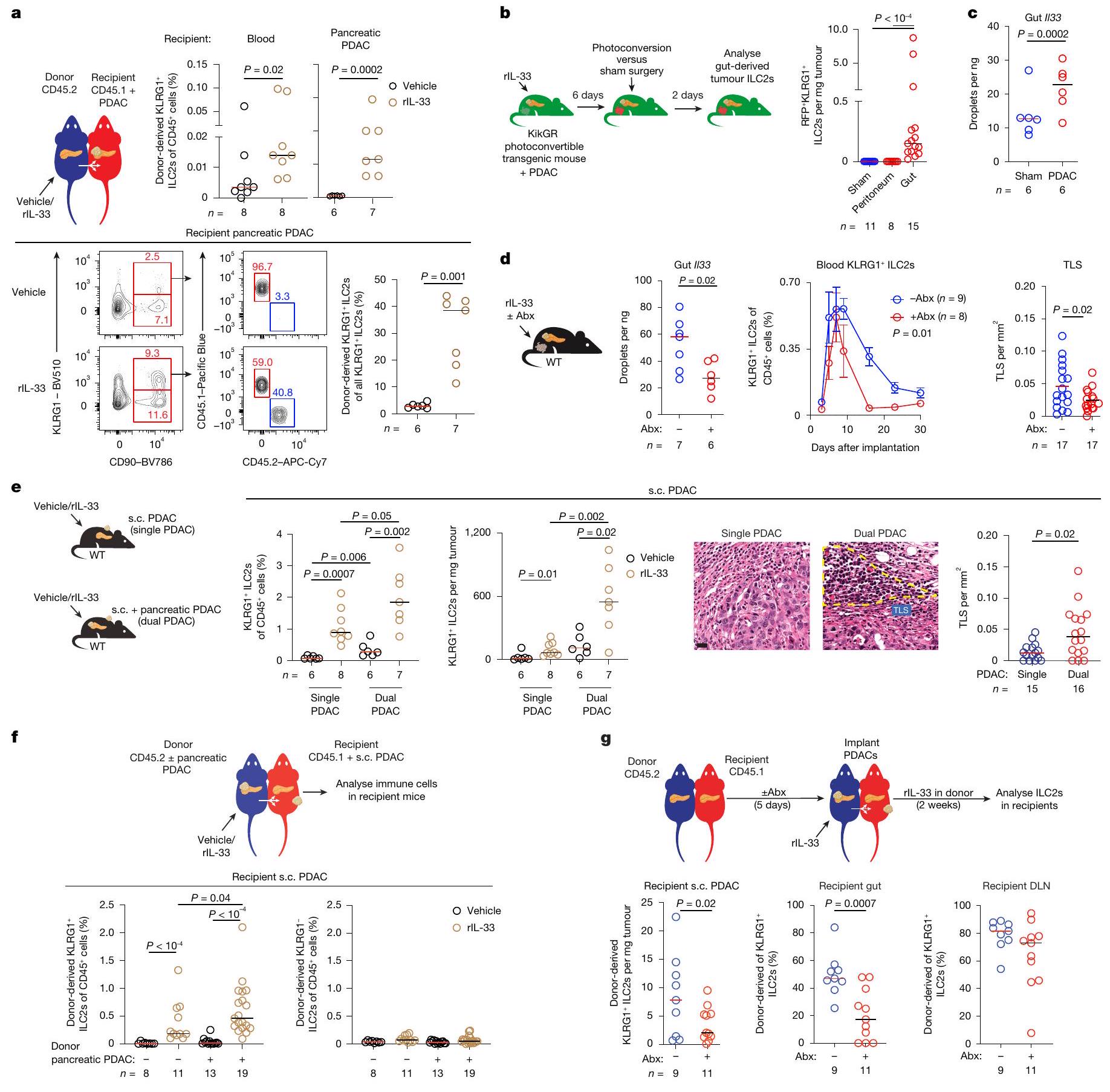
الانحدار. تم جمع البيانات في
للالتهابات الحادة حيث، على الرغم من أن كل من rIL-33 و rIL-25 قد وسعت
IL-33 المهندسة تعزز تكوين الأوعية اللمفاوية
مع وجود
تغييرات الترابط والتشكيل التي تعطل موقع ارتباط ST2 لـ IL-33، قمنا باستبدال جميع بقايا السيستين الأربعة في IL-33 البشري
نقاش
علامة مميزة لمسار TLS في الرواية. من الناحية الفسيولوجية، من المنطقي أن يبرمج هذا الهيكل التنظيمي SLOs في مواقع تشريحية محددة ويزود الخلايا المهاجرة بالآلات الجزيئية للتنقل إلى الأنسجة لتحفيز TLSs.
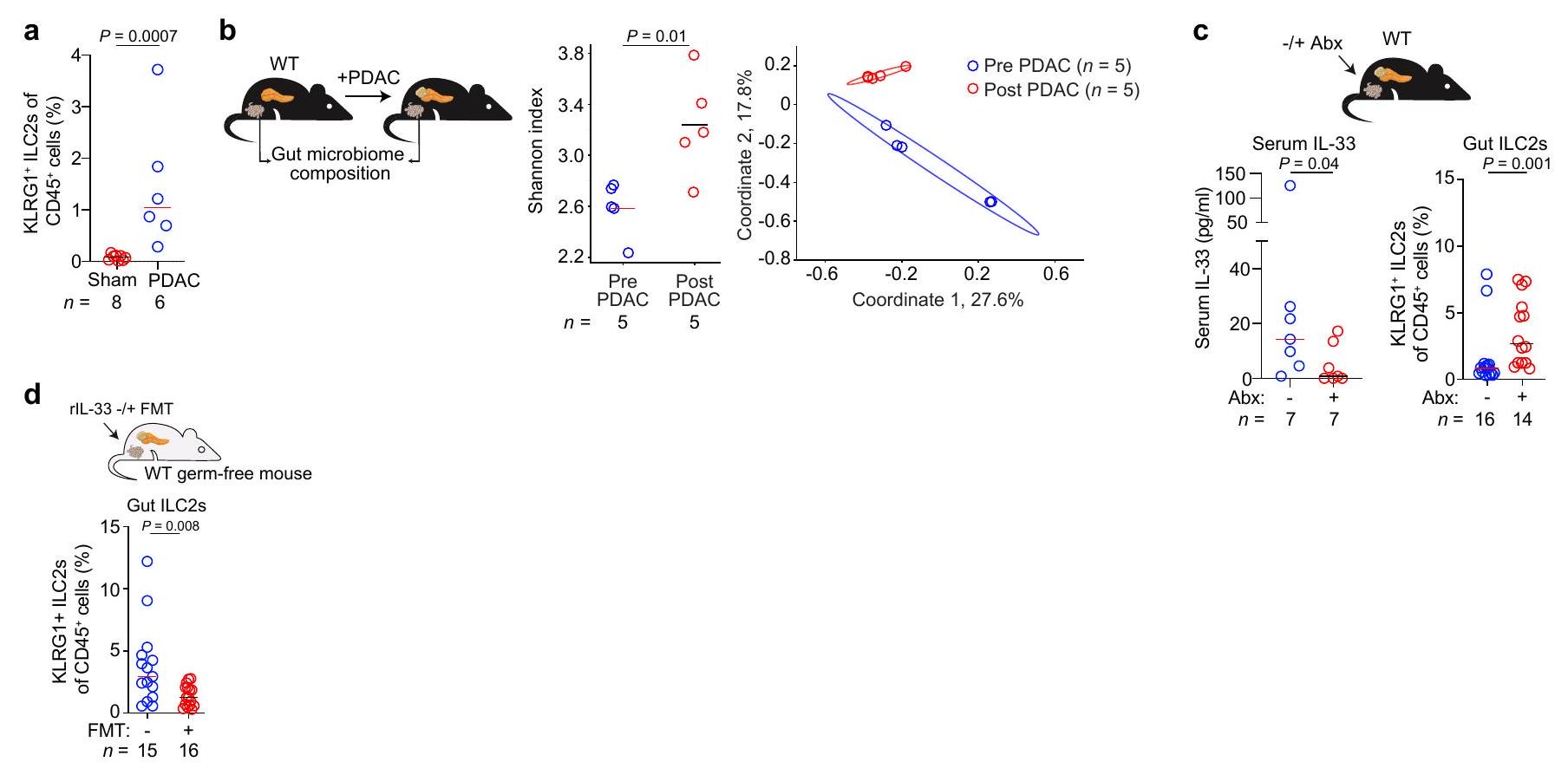
إن اكتشافنا أن سرطان البنكرياس (PDAC) يهيئ استجابة اللمفانية المضيفة من الأمعاء ويتأثر بالميكروبات المعوية هو أمر ملحوظ، حيث لا يزال الفهم الدقيق للخلايا التي تربط الميكروبات المعوية بكل من TLSs ومناعة الورم في تطور. ومع ذلك، لم نقم بالتحقيق، وبالتالي لا يمكننا استبعاد، المساهمات الوظيفية لـ ILC2s التي تهاجر إلى الأورام من مصادر أخرى، أو لـ ILC2s غير المهاجرة. وبالتالي، حيث يمكن أن تأتي ILC2s الدائرة من خزانات أنسجة مختلفة.
قدرة هندسة مسار IL-33-ST2 لتعزيز TLSs والتحكم في PDAC قد يكون لها آثار على العلاج المناعي للسرطان. حيث إن PDAC يشبه تقريبًا
المحتوى عبر الإنترنت
مقالة
- مؤلفون: مورا، ج. أ. وآخرون. تقوم خلايا ILC2s بتعزيز حجب PD-1 من خلال تنشيط المناعة ضد السرطان المحددة للأنسجة. ناتشر 579، 790-796 (2020).
- كلاوز، سي. إس. إن. وآخرون. الببتيد العصبي نيويروميدين U يحفز خلايا اللمفوية الفطرية والتهاب النوع 2. ناتشر 549، 282-286 (2017).
- والراب، أ. وآخرون. الببتيد العصبي NMU يعزز الالتهاب الرئوي التحسسي المدفوع بواسطة ILC2. ناتشر 549، 351-356 (2017).
- كاردوسو، ف. وآخرون. التنظيم العصبي لخلايا اللمفويات الفطرية من النوع 2 عبر نيويروميدين U. ناتشر 549، 277-281 (2017).
- تسوا، أ. م. وآخرون. تنظيم الببتيدات العصبية لاستجابات ILC2 غير المتكررة على أسطح الحواجز. ناتشر 611، 787-793 (2022).
- جارك، ك. ج. وآخرون. الوظائف غير المتكررة لخلايا اللمفويات الفطرية من المجموعة 2. ناتشر 611، 794-800 (2022).
- نوسباوم، ج. س. وآخرون. خلايا اللمفويات الفطرية من النوع 2 تتحكم في توازن الإيوزينوفيل. ناتشر 502، 245-248 (2013).
- غوغوي، م. وآخرون. LIF المستمد من ILC2 يرخص التقدم من المناعة النسيجية إلى المناعة النظامية. ناتشر 632، 885-892 (2024).
- أوليغانت، سي. جي. وآخرون. الحوار الذي يتم بوساطة MHCII بين خلايا اللمفويات الفطرية من المجموعة 2 و
تعمل الخلايا على تعزيز المناعة من النوع 2 وتعزز طرد الديدان الطفيلية. المناعة 41، 283-295 (2014). - أنسل، ك. م. وآخرون. حلقة تغذية راجعة إيجابية مدفوعة بالكيماوكينات تنظم الجريبات اللمفاوية. ناتشر 406، 309-314 (2000).
- لوثر، س. أ. وآخرون. أنشطة مختلفة للكيماويات المنزلية CCL19 وCCL21 وCXCL12 في تجنيد الخلايا اللمفاوية والخلايا الشجرية وتكوين الأنسجة اللمفاوية. مجلة المناعة 169، 424-433 (2002).
- ماير، د. وآخرون. يحدث تطور الأعضاء اللمفاوية خارج الموقع من خلال تعزيز بقاء خلايا المحفز للأنسجة اللمفاوية بواسطة الإنترلوكين 7. المناعة 26، 643-654 (2007).
- سرافي، م. ن.، غارسيا-زيبيدا، إ. أ.، ماكلين، ج. أ.، تشارو، إ. ف. ولستر، أ. د. بروتين جذب المونوسيتات في الفئران (MCP)-5: كيموكين CC جديد هو نظير هيكلي ووظيفي للبروتين MCP-1 البشري. ج. تجريبي. ميد. 185، 99-110 (1997).
- زاو، إكس. وآخرون. يتم إفراز CCL9 بواسطة الظهارة المرتبطة بالجريب وتستقطب CD11b من منطقة القبة في لويحات باير.
الخلايا الشجرية. J. Immunol. 171، 2797-2803 (2003). - Zhang، م. وآخرون. CCL7 يجذب cDC1 لتعزيز المناعة المضادة للورم وتسهيل العلاج المناعي عن طريق نقاط التفتيش لسرطان الرئة غير صغير الخلايا. نات. كوميونيك. 11، 6119 (2020).
- هوانغ، ي. وآخرون. خلايا KLRG1(hi) السلبية السلالة المستجيبة لـ IL-25 هي خلايا لمفاوية فطرية من النوع 2 “التهابية” متعددة الإمكانيات. نات. إيمونول. 16، 161-169 (2015).
- هوانغ، ي. وآخرون. النقل بين الأعضاء المعتمد على S1P لخلايا اللمفويات الفطرية من المجموعة 2 يدعم دفاع المضيف. ساينس 359، 114-119 (2018).
- Pu، Q. وآخرون. ميكروبيوتا الأمعاء تنظم استجابات الالتهاب لمحور الأمعاء والرئة من خلال التوسط في هجرة قسم ILC2. ج. المناعة. 207، 257-267 (2021).
- ريكاردو-غونزاليس، ر. ر. وآخرون. مسارات محددة للأنسجة تطرد ILC2s المنشطة لنشر المناعة من النوع 2. ج. إكسب. ميد. 217، 171 (2020).
- فلمار، أ.-ل. وآخرون. إنترلوكين-33 يحفز إنزيم تريبتوفان هيدروكسيلاز 1 لتعزيز المناعة التي mediated بواسطة خلايا اللمفويات الفطرية المجموعة 2. المناعةhttps://doi.org/10.1016/j.immuni.2020.02.009 (2020).
- بوشالكار، س. وآخرون. ميكروبيوم سرطان البنكرياس يعزز الأورام من خلال تحفيز كبت المناعة الفطرية والتكيفية. اكتشاف السرطان. 8، 403-416 (2018).
- كوهن، إ. س. وآخرون. أكسدة الألارمين IL-33 تنظم الالتهاب المعتمد على ST2. نات. كوميون. 6، 1-10 (2015).
- الت، سي. وآخرون. IL-33 طويل المفعول يحفز خلايا جذعية ومؤشرية دموية عالية الجودة بشكل أكثر كفاءة من عامل تحفيز مستعمرات العدلات أو AMD3100. بيولوجيا. زراعة نخاع العظم 25، 1475-1485 (2019).
- شميتز، ج. وآخرون. IL-33، سيتوكين شبيه بالإنترلوكين-1 الذي يتواصل عبر بروتين مستقبل IL-1 المرتبط ST2 ويحفز السيتوكينات المرتبطة بالنوع 2 من خلايا T المساعدة. المناعة 23، 479-490 (2005).
- سوا، س. وآخرون. تحليل علاقة النسب لجين RORyt
خلايا لمفاوية فطرية. العلوم 330، 665-669 (2010). - إيكيدا، أ. وآخرون. إنسان NKp44
تترافق خلايا اللمفويات الفطرية من المجموعة 3 مع الهياكل اللمفاوية الثلاثية المرتبطة بالأورام في سرطان القولون والمستقيم. أبحاث المناعة السرطانية. 8، 724-731 (2020). - بيترز، أ. وآخرون. خلايا Th17 تحفز تكوين جريبات لمفاوية غير طبيعية في التهاب أنسجة الجهاز العصبي المركزي. المناعة 35، 986-996 (2011).
- جاكلو، ن. وآخرون. حجب الجزيء المثبط المشترك PD-1 يحرر المناعة المضادة للورم المعتمدة على ILC2 في الميلانوما. نات. إيمونول.https://doi.org/10.1038/s41590-021-00943-z (2021).
- ألونسو-كوربيلو، د. وآخرون. برنامج وراثي بيئي محفز يبدأ تكوين الأورام. ناتشر 590، 642-648 (2021).
- هوارد، أ. د. وآخرون. تحديد مستقبلات النيوروميدين
ودورها في التغذية. الطبيعة 406، 70-74 (2000). - Qi، ف. وآخرون. تنتج البلعميات IL-33 من خلال تنشيط مسار إشارة MAPK أثناء عدوى RSV. مول. مناعة. 87، 284-292 (2017).
- كباشيما، ك. وآخرون. الحاجة إلى مستقبلات اللمفوتوكسين-بيتا الداخلية من أجل توازن خلايا الدندريت في الأنسجة اللمفاوية. المناعة 22، 439-450 (2005).
- هونغ، ل.-ي. وآخرون. السياق الخلوي للتعبير عن IL-33 يحدد التأثير على المناعة المضادة للديدان. ساي. مناعة. 5، eabc6259 (2020).
- تشانغ، م. وآخرون. مسار النقل لإفراز البروتين غير التقليدي المعتمد على الحويصلات. خلية 181، 637-652.e15 (2020).
- عالم، أ. وآخرون. الميكروبيوم الفطري يحفز إفراز IL-33 والمناعة من النوع 2 في سرطان البنكرياس. خلية السرطان 40، 153-167.e11 (2022).
(ج) المؤلفون 2025
طرق
فئران
خطوط الخلايا وإجراءات الحيوانات
من
تحليل الميكروبيوم
الـ H-rlL-33 المعاد تركيبه و H-e-rlL-33-Fc
علاج IL-33 المؤتلف، IL-25، H-rIL-33 و H-e-rIL-33-Fc
عينات بشرية
تدفق الخلايا؛ الجداول التكميلية 2 و 5). مصفوفات الأنسجة البشرية لسرطان البنكرياس الغدي
تحليل التعبير الجيني للأورام
عزل الخلايا
نقل الخلايا المايلويدية المعتمدة على ILC2
تدفق الخلايا
تم تعريفها على أنها حية
صبغة هيماتوكسيلين وإيوزين
كشف IL-33 في المصل
علم المناعة النسيجية
المناعية الفلورية
تبع ذلك حضانة مع Tyramide Alexa 647 (Invitrogen) تم تحضيرها وفقًا لتعليمات الشركة المصنعة مع تخفيفات محددة مسبقًا. بعد التلوين، تم تلوين الشرائح بعكس مع DAPI (Sigma-Aldrich) لمدة 10 دقائق وتم تغطيتها بـ Mowiol.
تسلسل مستقبلات خلايا B
التحور المفرط الجسدي
تفاعل البوليميراز المتسلسل القائم على القطرات الرقمية
تسلسل RNA أحادي الخلية
الفهارس المقدمة في المجموعة (
توقيعات النسخ لـ TLS و ILC2
التعبير في مجموعة بيانات TCGA-PAAD الموضحة أعلاه باستخدام طريقة TMM
الميكروسكوب الضوئي المترابط
دراسات في المختبر
الإحصائيات
توفر المواد
ملخص التقرير
توفر البيانات
البيانات متاحة تحت رقم الوصول إلى الأرشيف الجيني (GEO) GSE184585. تم الإبلاغ عن بيانات تسلسل RNA أحادي الخلية (scRNA-seq) لـ ILC2s سابقًا.
51. تومانو، أ. وآخرون. الدور المتميز للسموم اللمفاوية السطحية التي تعبر عنها خلايا B في تنظيم الأنسجة اللمفاوية الثانوية. المناعة 17، 239-250 (2002).
52. فوترر، أ.، مينك، ك.، لوز، أ.، كوسكو-فيلبوا، م. هـ. وبيفر، ك. مستقبل اللمفوتوكسين بيتا يتحكم في تكوين الأعضاء ونضوج الألفة في الأنسجة اللمفاوية الطرفية. المناعة 9، 59-70 (1998).
53. نوفوتشين، س. & هادجانتاكيس، أ.-ك. استخدام بروتين كيك جي آر القابل للتحويل من الأخضر إلى الأحمر للتأشير الخلوي وتحليل السلالة في خلايا ES والأجنة الفأرية. BMC Dev. Biol. 9، 49 (2009).
54. هايبك، ج. وآخرون. مسار مدفوع باللمفوتوكسين إلى سرطان الكبد الخلوي. خلية السرطان 16، 295-308 (2009).
55. ويرتز، س. وآخرون. نماذج الفئران المستحثة كيميائيًا للالتهاب المعوي الحاد والمزمن. نات. بروتوك. 12، 1295-1309 (2017).
56. عارفوزمان، م. وآخرون. الألياف الغذائية هي عامل حاسم في استجابات ILC2 المرضية والالتهاب المعوي. ج. تجريبي. ميد. 221، e20232148 (2024).
57. زغارا-رويز، د. ف. وآخرون. تطور الخلايا التائية المحددة لميكروبات الأمعاء في الغدة الصعترية. ناتشر 594، 413-417 (2021).
58. تومماسو، ب. د. وآخرون. نكست فلو يمكّن من إنشاء سير عمل حسابية قابلة للتكرار. نات. بيوتكنولوجي. 35، 316-319 (2017).
59. إيويلز، ب. أ. وآخرون. إطار عمل nf-core لخطوط أنابيب المعلوماتية الحيوية التي تم تنسيقها من قبل المجتمع. نات. بيولوجيا تقنية. 38، 276-278 (2020).
60. ستراوب، د. وآخرون. تفسيرات دراسات المجتمع الميكروبي البيئي متحيزة بسبب خط أنابيب تسلسل الأمبليكون لجين 16S rRNA المختار. فرونت. ميكروبيول. 11، 550420 (2020).
61. مارتن، م. كوتادابت يزيل تسلسلات الموصلات من قراءات التسلسل عالي الإنتاجية. مجلة EMBnet.https://doi.org/10.14806/ej.17.1.200 (2011).
62. كالاهاان، ب. ج. وآخرون. DADA2: استنتاج عينة عالية الدقة من بيانات أمبليكون إيلومينا. نات. ميثودز 13، 581-583 (2016).
63. كواست، سي. وآخرون. مشروع قاعدة بيانات جينات الرنا الريبوسومي SILVA: تحسين معالجة البيانات والأدوات المستندة إلى الويب. أبحاث الأحماض النووية. 41، D590-D596 (2013).
64. بيلي، ب. وآخرون. التحليلات الجينومية تحدد الأنماط الجزيئية لسرطان البنكرياس. ناتشر 531، 47-52 (2016).
65. ليو، ج. وآخرون. مورد بيانات سريرية متكامل من TCGA للسرطان الشامل لدفع تحليلات نتائج البقاء عالية الجودة. خلية 173، 400-416 (2018).
66. رافائيل، ب. ج. وآخرون. التوصيف الجينومي المتكامل للأدينوكارسينوما القنوية البنكرياسية. خلية السرطان 32، 185-203.e13 (2017).
67. بيرجر، أ. س. وآخرون. دراسة جزيئية شاملة عن جميع أنواع السرطان للأورام النسائية وسرطان الثدي. خلية السرطان 33، 690-705 (2018).
68. شبكة، تي. سي. جي. أ. وآخرون. التصنيف الجينومي للورم الميلاني الجلدي. خلية 161، 1681-1696 (2015).
69. باندو، ج. ك.، ليانغ، هـ.-إي. ولوكلي، ر. م. تحديد وتوزيع خلايا اللمفوية الفطرية النامية في أمعاء الفأر الجنيني. نات. إيمونول. 16، 153-160 (2014).
70. تشيانغ، إ. واي. وآخرون. الاستنزاف المستهدف للخلايا TH1 وTH17 التي تعبر عن اللمفوتوكسين-أ يمنع الأمراض المناعية الذاتية. نات. ميد. 15، 766-773 (2009).
71. رودريغيز، أ. ب. وآخرون. الآليات المناعية تنظم الهياكل اللمفاوية الثلاثية في الأورام عبر الألياف السرطانية المرتبطة بالسرطان. تقرير الخلية. 36، 109422 (2021).
72. سيلينا، ك. وآخرون. تحدد المراكز الجرثومية الأهمية التنبؤية للهياكل اللمفاوية الثلاثية وتتعرض للتأثير السلبي من الكورتيكوستيرويدات في سرطان الخلايا الحرشفية الرئوي. أبحاث السرطان. 78، 1308-1320 (2017).
73. بوش، ف. وآخرون. نضوج الهياكل اللمفاوية الثانوية وعودة سرطان القولون والمستقيم من المرحلة الثانية والثالثة. أونكوإيمونولوجي 7، e1378844 (2017).
74. كالديتارو، ج. وآخرون. الهياكل اللمفاوية الثلاثية داخل الورم مرتبطة بانخفاض خطر تكرار الإصابة المبكر بسرطان الكبد hepatocellular carcinoma. مجلة الكبد 70، 58-65 (2019).
75. فانهيرسيك، ل. وآخرون. الهياكل اللمفاوية الثلاثية الناضجة تتنبأ بفعالية مثبطات نقاط التفتيش المناعية في الأورام الصلبة بشكل مستقل عن تعبير PD-L1. نات. كانسر 2، 794-802 (2021).
76. كارلسون، سي. إس. وآخرون. استخدام القوالب الاصطناعية لتصميم اختبار PCR متعدد غير متحيز. نات. كوميونيك. 4، 2680 (2013).
77. غابيرنيت، ج. وآخرون. nf-core/airrflow: سير عمل لتحليل مجموعة مستقبلات المناعة التكيفية باستخدام إطار عمل Immcantation. PLoS Comput. Biol. 20، e1012265 (2024).
78. نوري، ن. وكلاينشتاين، س. هـ. تحليل الطفرات الجسدية لتحسين تحديد عائلات الخلايا البائية من بيانات تسلسل الجيل التالي. PLoS Comput. Biol. 16، e1007977 (2020).
79. غوبتا، ن. ت. وآخرون. تشينج-أو: مجموعة أدوات لتحليل بيانات تسلسل مجموعة الأجسام المضادة لبروتينات B على نطاق واسع. المعلوماتية الحيوية 31، 3356-3358 (2015).
80. Hänzelmann, S.، Castelo, R. & Guinney, J. GSVA: تحليل تباين مجموعة الجينات لبيانات الميكروأري وRNA-seq. BMC Bioinform. 14، 7 (2013).
81. مكارثي، د. ج.، كامبل، ك. ر.، لون، أ. ت. ل. و ويلز، ك. ف. سكاتر: المعالجة المسبقة، مراقبة الجودة، التطبيع والتصور لبيانات تسلسل RNA أحادي الخلية في R. المعلوماتية الحيوية 33، btw777 (2017).
82. كانينغهام، ف. وآخرون. إنسيبل 2022. أبحاث الأحماض النووية. 50، D988-D995 (2021).
83. كولابريكو، أ. وآخرون. TCGAbiolinks: حزمة R/Bioconductor للتحليل التكاملي لبيانات TCGA. أبحاث الأحماض النووية 44، e71 (2016).
84. سيلفا، ت. س. وآخرون. سير عمل TCGA: تحليل بيانات الجينوميات والابيجينوميات السرطانية باستخدام حزم Bioconductor. F100ORes. 5، 1542 (2016).
85. منير، م. وآخرون. وظائف جديدة في حزمة TCGAbiolinks لدراسة ودمج بيانات السرطان من GDC وGTEx. PLoS Comput. Biol. 15، e1006701 (2019).
86. روبنسون، م. د. وأوشلاك، أ. طريقة تطبيع القياس لتحليل التعبير التفاضلي لبيانات RNA-seq. جينوم بيو. 11، R25 (2010).
معلومات إضافية
يجب توجيه المراسلات والطلبات للحصول على المواد إلى فينود ب. بالاتشاندرا. تشكر مجلة نيتشر شيغيو كوياسو والمراجعين الآخرين المجهولين على مساهمتهم في مراجعة الأقران لهذا العمل.
معلومات إعادة الطبع والتصاريح متاحة علىhttp://www.nature.com/reprints.
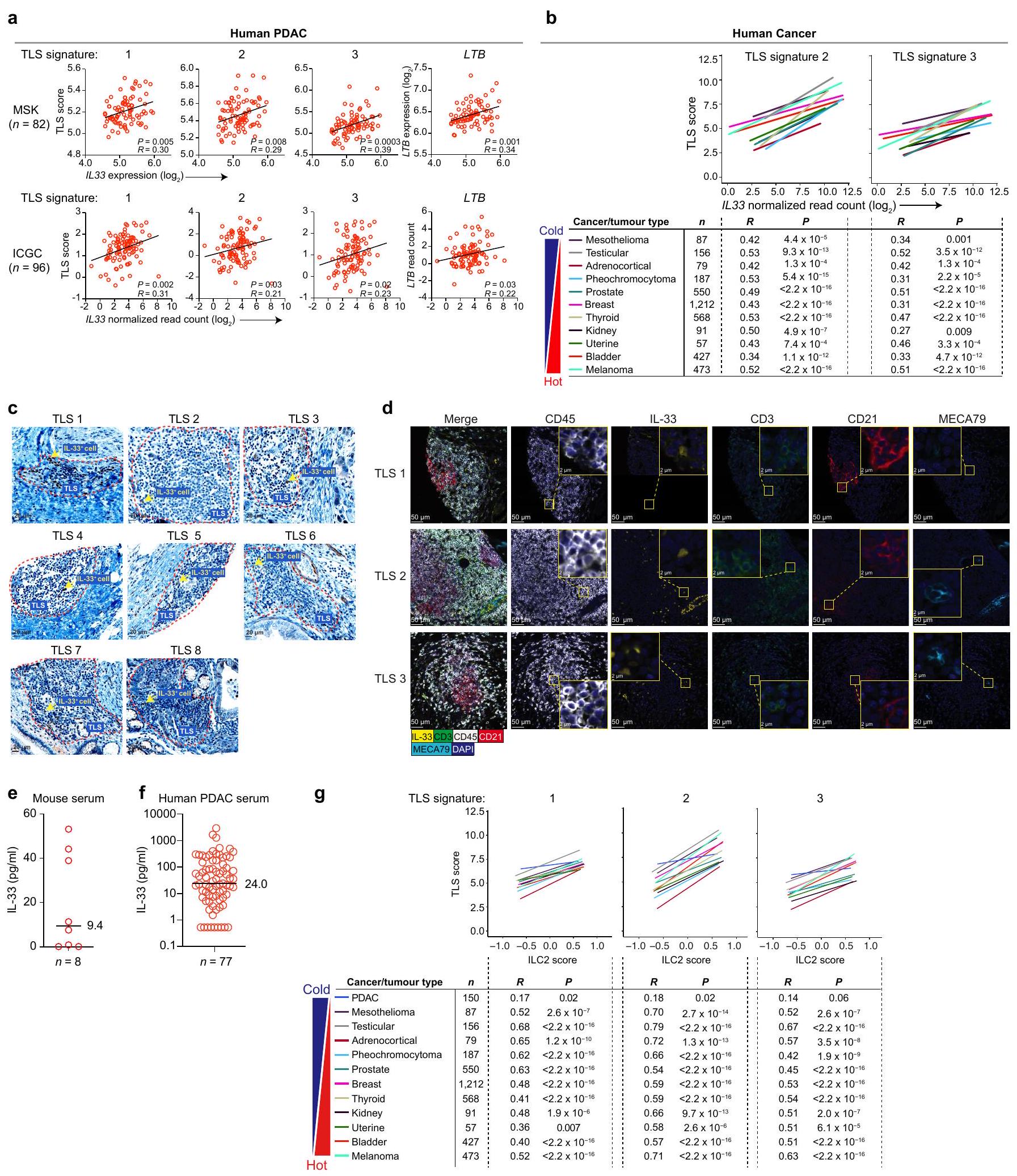
صور لـ TLSs في سرطان البنكرياس البشري. هـ، و، مستوى IL-33 في مصل الفئران المصابة بسرطان البنكرياس المعالجة بـ rlL-33 (هـ) وفي مرضى سرطان البنكرياس البشري (و). ز، ارتباط توقيع النسخ الخاص بـ ILC2 البشري المنشط بواسطة IL-33 بتوقيعات TLS (توقيعات TLS:

| CD8
|
|||
 |
|||
| ٨ | PDAC 1 (
|
||
| ٦ | ◯ | ||
 |
|||
| ٤ | أو | ||
| 2 |  |
 |
|
| منخفض | معتدل | ||



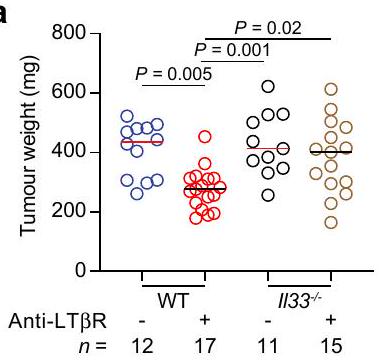
فئران الكوليتيس الناتج عن DSS المعالجة بالمركبة والمعالجة بـ rIL-33. البيانات المجمعة بعد 2 (أ)، 3 (ج، د PDAC 3، 4) و3-5 (ج، د PDAC 1، 2، 5، 6، هـ، و) أسابيع بعد زراعة الورم، مجمعة من
مقالة
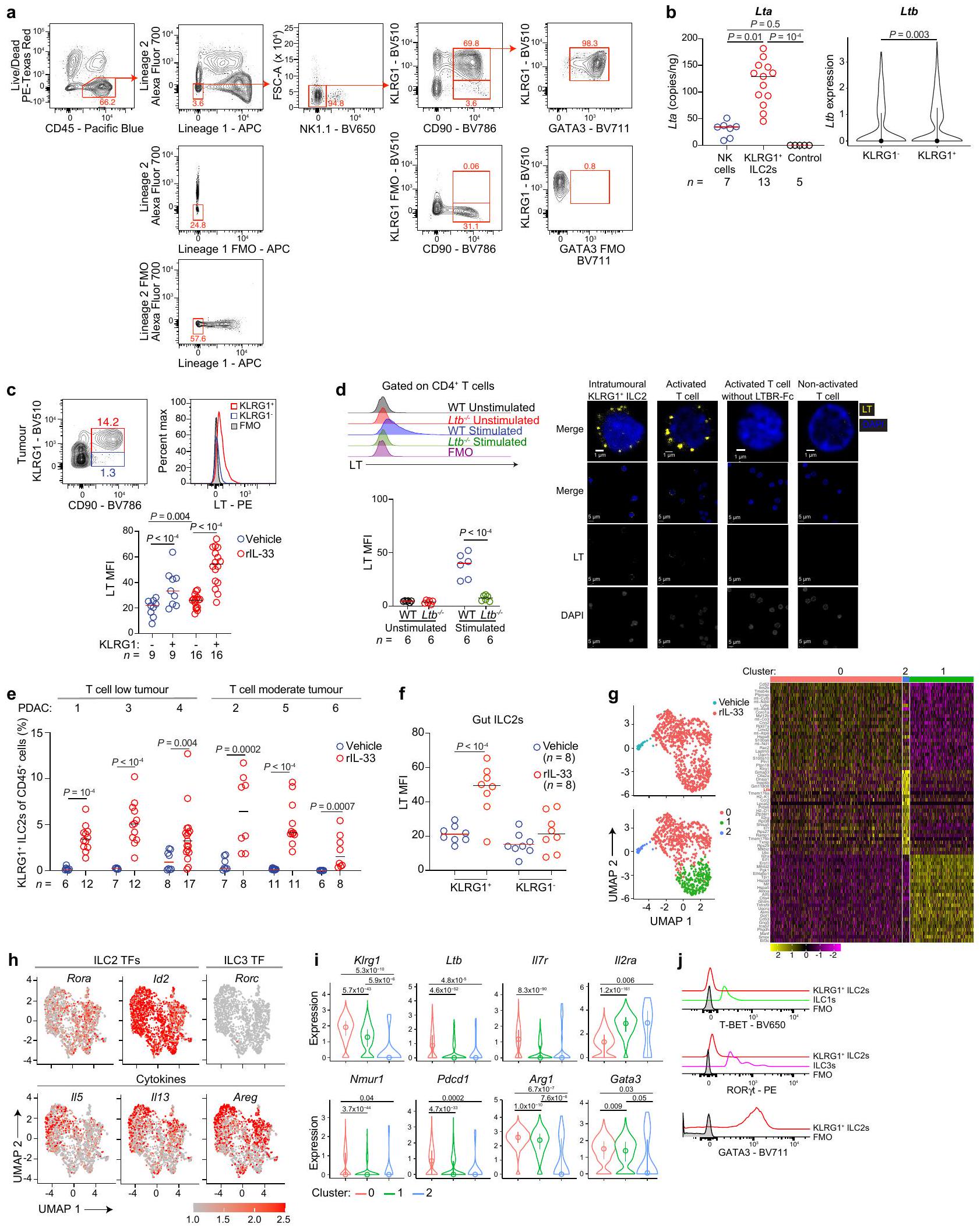
الجينات لكل مجموعة. UMAP، مخططات الكمان = عوامل النسخ ILC (h)، والعلامات (i) في المجموعات غير المراقبة في الشكل 3a، وسيتوكينات ILC2 (h). لم يكن Tbx21 قابلاً للاكتشاف. j، عوامل النسخ ILC على KLRG1 داخل الورم.
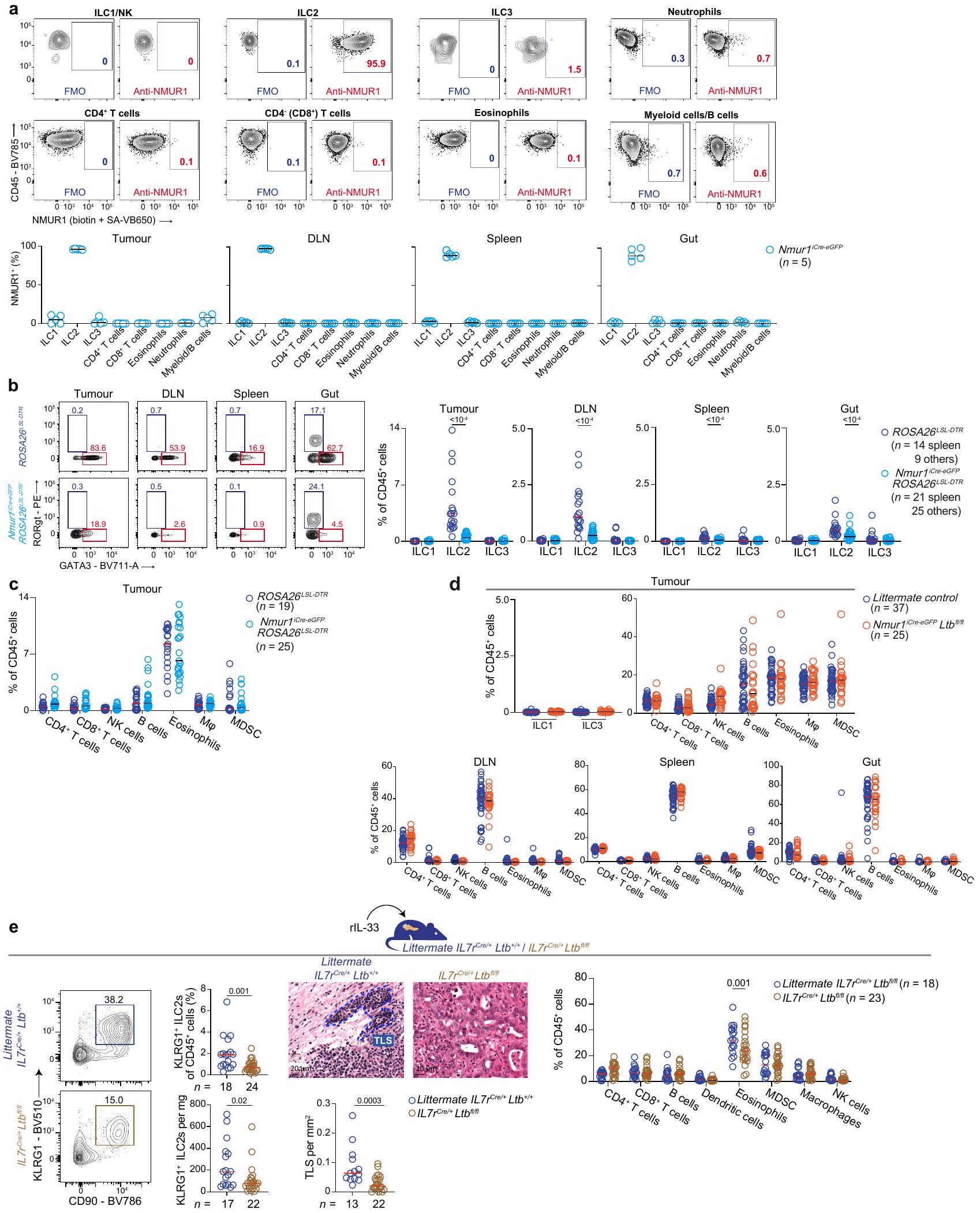
تردد الخلايا المناعية (يمين) في المعالجة بـ rll-33
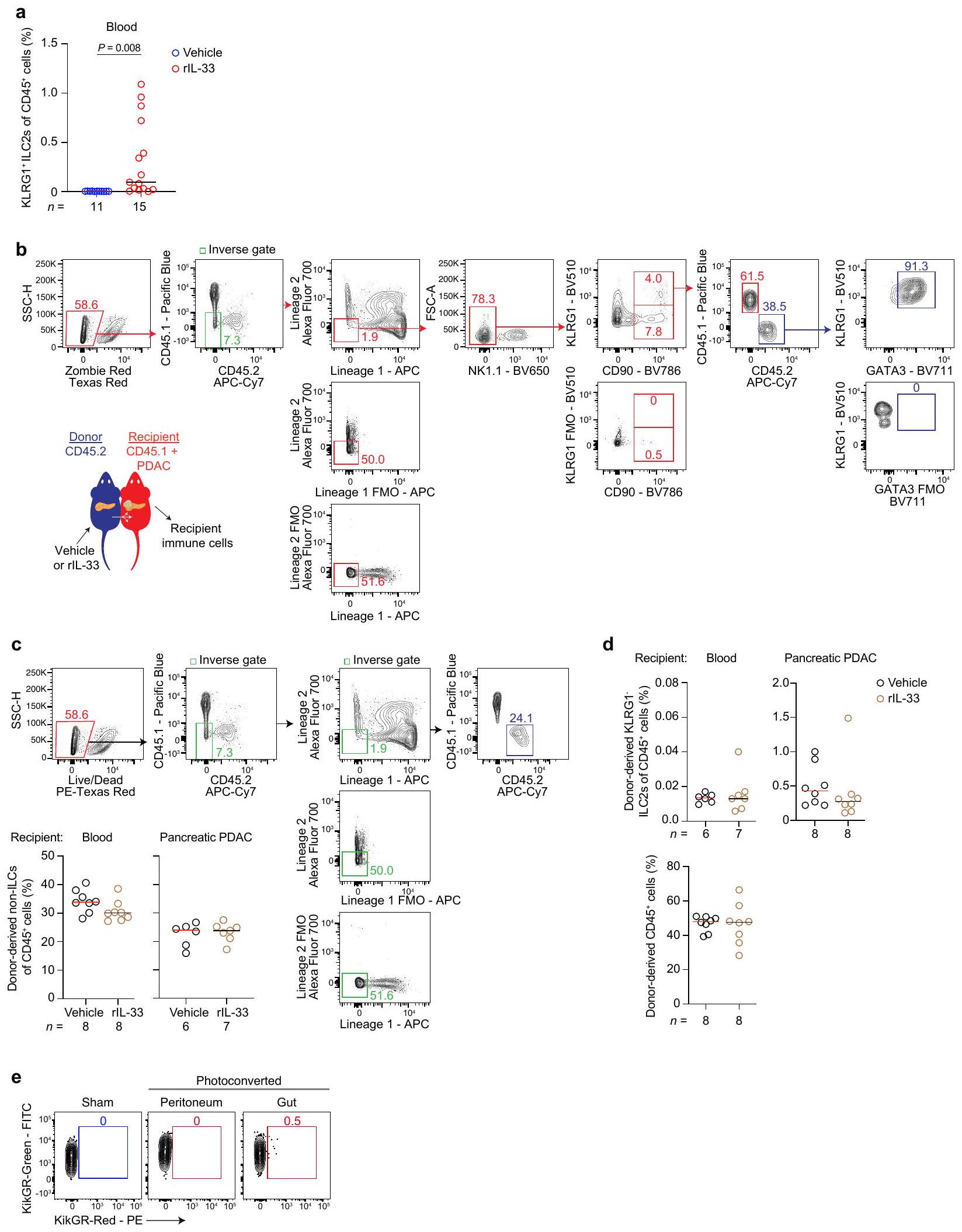
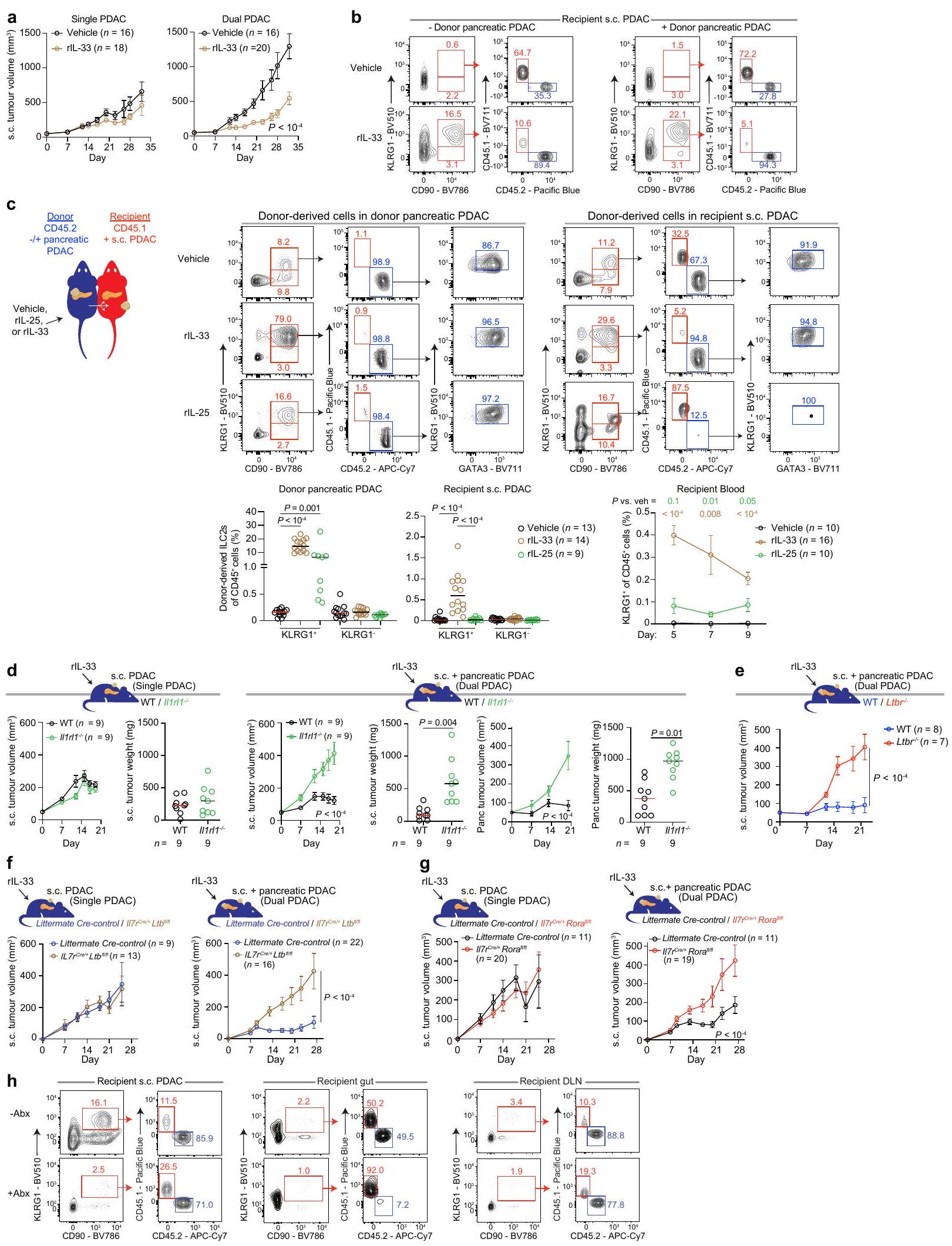
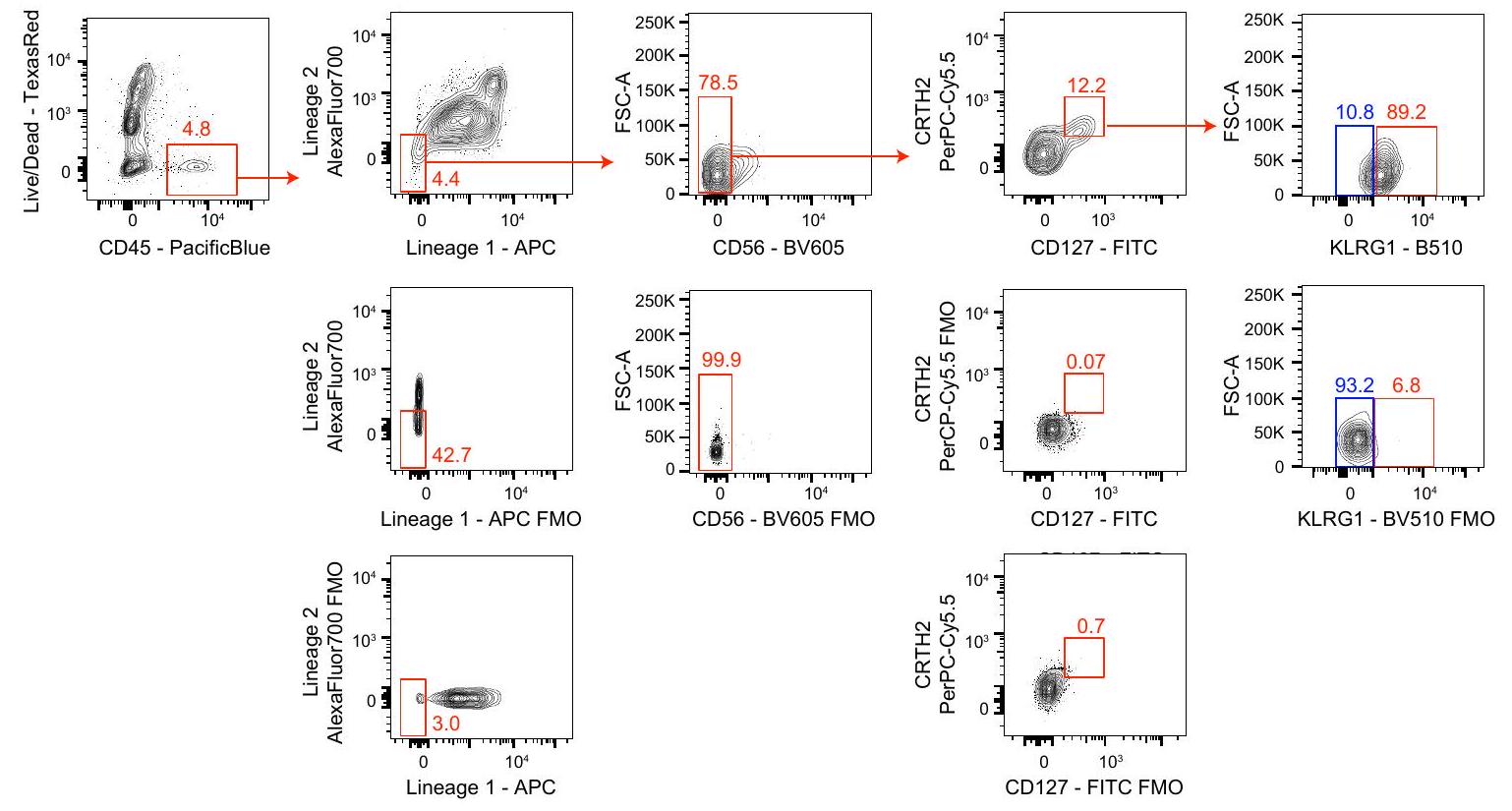
الشكل 6 من البيانات الموسعة | استراتيجية تصنيف ILC2 وتكرارها في بارابيوتيك
مقالة
تحكم في فضلات الأشقاء
b

C




مقالة
بحث الطبيعة
ملخص التقرير
الإحصائيات
غير متوفر

□
□
تم التأكيد
حجم العينة بالضبط

اختبار(ات) الإحصاء المستخدمة وما إذا كانت أحادية الجانب أو ثنائية الجانب
يجب أن تُوصف الاختبارات الشائعة فقط بالاسم؛ واصفًا التقنيات الأكثر تعقيدًا في قسم الطرق.
□

□

□

□


□ لتحليل بايزي، معلومات حول اختيار الأوليات وإعدادات سلسلة ماركوف مونت كارلو

□ لتصميمات هرمية ومعقدة، تحديد المستوى المناسب للاختبارات والتقارير الكاملة عن النتائج
□ س
تقديرات أحجام التأثير (مثل حجم تأثير كوهين)
البرمجيات والشيفرة
معلومات السياسة حول توفر كود الكمبيوتر
لتحليل تدفق الخلايا، تم تحليل جميع العينات على جهاز FACS LSR Fortessa (BD Biosciences) باستخدام FlowJo (الإصدار 10.7.1، Tree Star).
تم رقمنة الشرائح المرضية باستخدام جهاز Panoramic Flash 250 (3Dhistech، بودابست، المجر) باستخدام عدسة Zeiss 20x/0.8NA ومرشحات مخصصة لـ A488 و A546 و A594 و A647.
تم تحديد عدد الخلايا النواة في TLS باستخدام وظيفة تحليل الجسيمات في ImageJ (الإصدار 2.3.0، NHI، الولايات المتحدة الأمريكية). تم عد خلايا IL33+ في TLS يدويًا.
مجهري: لتصوير LT-PE وDAPI النووي، تم التقاط الصور على نظام مجهر ليزري مسح نقطي (SP5، لايكا، ويتزلار، ألمانيا) باستخدام عدسة تكبير 63x مع زيت.
تم إجراء اختبار تقرير ST2: تم الكشف عن امتصاص الطول الموجي 630 نانومتر باستخدام جهاز قراءة Cytation 3 (BioTek).
تسلسل مستقبلات خلايا B: تم إجراء تسلسل المناعي لمناطق CDR3 لسلاسل مستقبلات خلايا B في الفئران على الحمض النووي الجيني من عينات مثبتة بالصيغة الفورمالينية باستخدام اختبار immunoSEQ (تقنيات البيولوجيا التكيفية).
تم إجراء توليد القطرات في نظام QX200 ddPCR (بايو راد) باستخدام cDNA الناتج من 0.8-2 نانوغرام من RNA الكلي مع مجموعة OneStep RT-ddPCR المتقدمة للبروبي (بايو راد) وفقًا لبروتوكول الشركة المصنعة مع النسخ العكسي في
امتداد في
تحليل البيانات
تحليل التعبير الجيني للأورام: تم تحليل البيانات باستخدام
تدفق الخلايا: تم تحليل البيانات باستخدام FlowJo (الإصدار 10.7.1، Tree Star).
تم تحديد عدد TLSs في ثلاث مقاطع على الأقل باستخدام QuPath الإصدار 0.2.3.
تم قياس خلايا IL33+ و IL33+CD45+ باستخدام برنامج ImageJ الإصدار 2.3.0، وتم تقدير عدد الخلايا لكل وحدة مساحة من خلال حساب المساحة السطحية بناءً على وجود خلايا DAPI+.
تسلسل RNA على مستوى الخلية الواحدة: تم إجراء المعالجة الأولية لصور التسلسل باستخدام برنامج التحليل في الوقت الحقيقي من إيلومينا (RTA). مجموعة برامج 10X Genomics Cell Ranger للخلية الواحدة الإصدار 3.0.2https://support.10xgenomics.com/تم استخدام (single-cell-gene-expression/software/pipelines/latest/what-is-cellranger) لفصل العينات، ومحاذاتها إلى مرجع الجينوم الفأري mm10، وتصفيتها، وعدّ وحدات التعبير الجيني (UMIs)، وجينات نهاية الخلية المفردة 5’، ومراقبة الجودة وفقًا لمعايير الشركة المصنعة. تم تحليل البيانات المعالجة بعد ذلك في
التحور الجسدي: تم الاحتفاظ بإعادة ترتيب تسلسلات السلاسل الثقيلة المنتجة لتحليل العلاقات التكتلية لخلايا B، وتم تعريف التكتلات من خلال التجميع الطيفي المدرك لـ VDJ باستخدام حزمة R SCOPer. تم حساب ترددات الطفرات باستخدام دالة الطفرات المرصودة في حزمة R Shazam.
بيانات
معلومات السياسة حول توفر البيانات
- رموز الانضمام، معرفات فريدة، أو روابط ويب لمجموعات البيانات المتاحة للجمهور
- قائمة بالأشكال التي تحتوي على بيانات خام مرتبطة بها
- وصف لأي قيود على توفر البيانات
التقارير الخاصة بالمجال
علوم الحياة □ العلوم السلوكية والاجتماعية □ العلوم البيئية والتطورية والبيئية
لنسخة مرجعية من الوثيقة بجميع الأقسام، انظرnature.com/documents/nr-reporting-summary-flat.pdf
تصميم دراسة العلوم الحياتية
حجم العينة
تم تحديد أحجام العينات بناءً على تجربتنا وتجارب باحثين آخرين مع خطوط الخلايا المعنية. لم تُستخدم أي طرق إحصائية حيث لاحظنا العديد من التأثيرات ذات الدلالة الإحصائية في البيانات باستخدام الطرق المذكورة أعلاه لاختيار حجم العينة دون حسابات مسبقة لحجم العينة.
لم يتم استبعاد أي بيانات من التحليلات.
التقارير عن مواد وأنظمة وطرق محددة
| غير متوفر | مشارك في الدراسة |
| □ |  |
| □ | خطوط خلايا حقيقية النواة |
 |
□ علم الحفريات وعلم الآثار |
| □ | – الحيوانات وغيرها من الكائنات الحية |
| □ | المشاركون في الأبحاث البشرية |
 |
□ |
| V | □ |
|
|
مشارك في الدراسة |
|
|
|
|
|
تدفق الخلايا |
|
|
|
الأجسام المضادة
| الأجسام المضادة المستخدمة |
|
اسم الجسم المضاد لقناة الهدف الشركة المصنعة رقم الكتالوج النسخة الكمية
جهاز مضاد GATA3 PE PE الفأر من BD Biosciences 560074 L50-823 4
PD-1 BV786 BV786 فأر مضاد للبشر CD279 (PD-1) BD Biosciences 563789 EH12.1 2
RORgt BV650 BV650 مضاد للفأر البشري RORgt BD Biosciences 563424 Q21-559 2
الأجسام المضادة الثانوية لـ hLTBR-Fc BV650 BV650 فأر مضاد للبشر IgG BD Biosciences 740596 G18-145 2
الأجسام المضادة الثانوية لـ hLTBR-Fc PE PE فأر مضاد للبشر IgG BD Biosciences 555787 G18-145 2
CD117 PE-Cy5 PE/Cy5 مضاد للبشر CD117 (c-kit) BioLegend 323412 A3C6E2 2
CD11b APC APC مضاد للبشر CD11b BioLegend 301310 ICRF44 2
CD161 BV785 فيوليت برايت 785 مضاد للبشر CD161 BioLegend 339930 HP-3G10 2
CD25 APC-Cy7 APC/Cy7 مضاد للبشر CD25 BioLegend 302614 BC96 2
CD45 PacBlue الأزرق الباسيفيكي مضاد للبشر CD45 BioLegend 304029 HI30 2
CD56 BV605 فيوليت برايت 605 مضاد للبشر CD56 (NCAM) بايو ليجند 318334 HCD56 2
CRTH2 PerCP-Cy5.5 PerCP/Cy5.5 مضاد للبشر CD294 (CRTH2) BioLegend 350116 BM16 4
CRTH2 PE PE مضاد الإنسان CD294 (CRTH2) BioLegend 350106 BM16 4
FceRIa APC APC مضاد لـ FceRIa البشري BioLegend 334612 AER-37 2
ICOS BV711 بنفسجي لامع 711 مضاد للبشر/الفئران/الجرذان CD278 (ICOS) BioLegend 313548 C398.4A 2
NKp44 PE-Cy7 PE/Cy7 مضاد للبشر CD336 (NKp44) BioLegend 325116 P44-8 2
T-BET BV711 بنفسجي لامع 711 مضاد-Tbet BioLegend 6448204 B10 2
تفاعل TCR a/b AF700 أليكسا فلور 700 مضاد لـ TCR البشري a/b بايو ليجند 306730 IP26 2
KLRG1 BV510 Brilliant Violet 510 مضاد للفأر/البشر KLRG1 BioLegend 138421 2F1/KLRG1 2
CD11c APC مضاد Hu CD11c، APC Invitrogen 17-0116-42 3.92
CD127 FITC مضاد Hu CD127، FITC Invitrogen 11-1278-42 eBioRDR5 2
CD14 APC مضاد Hu CD14، APC إيفيتروجين 17-0149-42 61D3 2
CD16 APC مضاد Hu CD16 Invitrogen 17-0168-42 eBioCB16 2
CD19 AF700 مضاد Hu CD19 إيفيتروجين 56-0199-42 HIB19 2
CD3 AF700 مضاد Hu CD3، أليكسا فلور 700 إنفيتروجين 56-0037-42 OKT3 2
CD5 APC مضاد Hu CD5، APC إنفيتروجن 17-0058-42 L17F12 2
ST2 PE Anti-Hu IL-33R (ST2)، PE Invitrogen 12-9338-42 hIL33Rcap 4
اسم المنتج رقم كتالوج الصانع التطبيق التركيز/الجرعة
rhLTBR/Fc كيميرا أنظمة البحث والتطوير 629-LR تدفق
نظام البحث والتطوير Fc Chimera R&D 1008-LR
بروتين IL-33 المؤتلف من الفأر أنظمة R&D 3626-ML-010/CF العلاج (عن طريق الحقن في الصفاق)
بروتين IL-25 المؤتلف من الفأر أنظمة R&D 1399-ML-010/CF العلاج (عن طريق الحقن في الصفاق)
سم الدفتيريا (DT) EMD Millipore 322326100 نانوجرام
مادة في الجسم/ في المختبر
اسم المنتج رقم كتالوج الصانع التطبيق تفاصيل الجرعة
أجسام مضادة وحيدة النسيلة لمستقبل اللمفوتوكسين بيتا من إيفيتروجن 16-5671-82 الثقافة غير متاحة النسخة 3C8
أجسام مضادة وحيدة النسيلة لمستقبل اللمفوتوكسين بيتا من إيفيتروجن 16-5671-38 فيفو
تحكم إيزوتيب IgG1 كابا من رات إنفيتروجين
التحقق
تم التحقق من جميع الأجسام المضادة من قبل الشركة المصنعة واستخدامها وفقًا لتعليماتها. في تجاربنا، تم تضمين عينات التحكم من نوع الأيزوتيب و/أو FMO. يمكن العثور على معلومات إضافية حول التحقق على مواقع الشركات المصنعة.
خطوط خلايا حقيقية النواة
(انظر سجل ICLAC)
الحيوانات والكيانات الأخرى
| الحيوانات المخبرية | تم شراء فئران C57BL/6 (النوع البري [WT]، CD45.2) وفئران C57BL/6 CD45.1 من مختبر جاكسون. كانت فئران ||1r|1-/- (المعوزة لـ ST2) و II33-/- هدية من M.J. Rosen. كانت فئران Ltbfl/fl هدية من A.V. Tumanov. تم وصف فئران Nmur1iCre-eGFP ROSALSL-DTR سابقًا. تم تهجين Ltbfl/fl مع Nmur1iCre-eGFP و II7rCre/+ للحصول على فئران Nmur1iCre-iGFP Ltbfl/fl و II7rCre/+Ltbfl/fl. كانت فئران II7rCre/+Rorafl/fl هدية من A.N.J. McKenzie. كانت فئران Ltbr-/- هدية من T.T. Lu. كانت فئران CAG-KikGR33 هدية من G.E. Diehl. تم توفير الفئران الخالية من الجراثيم من منشأة الجنوطوبيوتيك في مركز وييل كورنيل الطبي (MSK). في جميع التجارب، كانت الفئران تتراوح أعمارها بين 6-14 أسبوعًا، وتمت مطابقتها من حيث العمر والجنس، وتم تعيينها عشوائيًا إلى مجموعات العلاج المحددة، مع إجراء ما لا يقل عن تجربتين مستقلتين طوال الوقت. تم استخدام كل من الحيوانات الذكرية والأنثوية. تم تربية الحيوانات والحفاظ عليها في منشأة حيوانات خالية من مسببات الأمراض المحددة في مركز ميموريال سلوان كيتيرينغ للسرطان. |
| الحيوانات البرية | لم يتم استخدام حيوانات برية. |
| عينات تم جمعها من الميدان | لم يتم استخدام عينات تم جمعها من الميدان في هذه الدراسة. |
| رقابة الأخلاقيات | تم تربية الحيوانات والحفاظ عليها في منشأة حيوانات خالية من مسببات الأمراض، وتم إجراء جميع التجارب وفقًا لبروتوكول معتمد من لجنة رعاية واستخدام الحيوانات المؤسسية (IACUC) في مركز ميموريال سلون كيترينغ للسرطان (MSK) وامتثالًا لجميع اللوائح الأخلاقية ذات الصلة. |
مشاركون في البحث البشري
خصائص السكان
تُفصّل الخصائص السريرية للمرضى في مصفوفة الأنسجة الدقيقة، وتدفق السيتومتر، وزراعة ILC2، ومجموعات النسخ في الجداول التكميلية 1 و2 و3 و5، وتُقدم أدناه.
الخصائص ن (%)
الجنس
ذكر 40 (49)
أنثى 42 (51)
العمر (سنة)
الوسيط (المدى interquartile) 68 (62-75)
موقع الورم
رأس 53 (65)
الجسم/الذيل 29 (35)
الإجراء
استئصال البنكرياس والاثني عشر 53 (65)
استئصال البنكرياس البعيد 29 (35)
pT
12 (2)
21 (1)
378 (95)
41 (1)
pN
033 (40)
148 (59)
x1 (1)
pM
081 (99)
11 (1)
المرحلة المرضية
IA 2 (2)
IB 1 (1)
IIA 30 (37)
IIB 47 (57)
III 1 (1)
الرابع 1 (1)
هامش جراحي
إيجابي 9 (11)
سالب 71 (87)
غير متاح 2 (2)
العلاج المساعد
نعم 61 (74)
لا 21 (26)
الخصائص السريرية المرضية لمرضى سرطان البنكرياس القنوي في مجموعة IHC و IF
الخصائص ن (%)
الجنس
Male 4 (36)
Female 7 (64)
Age (y)
Median (IQR) 70 (62-79)
Tumor location
Head 9 (82)
Body/tail 2 (18)
Procedure
Pancreaticoduodenectomy 9 (82)
Distal pancreatectomy 2 (18)
pT
10(0)
20(0)
3 11 (100)
4 (0)
pN
O (45)
16 (55)
pM
0 11 (100)
10(0)
Pathological stage
IIA 5 (45)
IIB 6 (55)
Surgical margin
Positive 4 (36)
Negative 7 (64)
Adjuvant treatment
Yes 11 (100)
No O (0)
Clinicopathological characteristics of PDAC patients in flow cytometry cohort (n = 9)
Characteristic n (%)
Sex
Male 4 (44)
Female 5 (55)
Age (y)
Median (IQR) 67 (63-80)
Procedure
Pancreaticoduodenectomy 6 (66)
Distal pancreatectomy 2 (22)
Total pancreatectomy 1 (11)
pT
14 (44)
23(33)
3 1 (11)
4 0 (0)
x 1 (11)
pN
O 4 (44)
11 (11)
22(22)
x2(22)
pM
O 4 (54)
11 (11)
23(33)
x 1 (11)
Pathological stage
l (33)
II 2 (22)
III 3 (33)
Local recurrence 1 (11)
Surgical margin
Positive 0 (0)
Negative 9(100)
Adjuvant treatment
Yes 7 (77)
No 2 (22)
Clinicopathological characteristics of PDAC patients with serum IL33 measurements (n=77)
Characteristic n (%)
Sex
Male 43 (56)
Female 34 (44)
تم تجنيد جميع المرضى المؤهلين لإجراء استئصال جراحي في مركز ميموريال سلوان كيترينغ للسرطان للمشاركة في بروتوكول معتمد من مجلس المراجعة المؤسسية. تم جمع عينات من جميع المرضى الذين قدموا موافقة مستنيرة؛ وتمت جميع إجراءات الدراسة وفقًا صارم لجميع القوانين الأخلاقية والمؤسسية. نظرًا لأن المرضى تم تجنيدهم فقط في مركز ميموريال سلوان كيترينغ للسرطان، هناك احتمال لوجود انحياز في الاختيار خاص بالمؤسسة. لا نعتقد أن هذا الانحياز المحتمل سيؤثر على نتائج هذه الدراسة.
تم جمع جميع الأنسجة في مركز ميموريال سلوان كيترينغ للسرطان بموجب بروتوكول الدراسة رقم 15-149 الذي تمت الموافقة عليه من قبل لجنة المراجعة المؤسسية لمركز ميموريال سلوان كيترينغ للسرطان. تم الحصول على موافقة مستنيرة من جميع المرضى. كانت الدراسة متوافقة تمامًا مع جميع اللوائح الأخلاقية المؤسسية.
تدفق الخلايا
المؤامرات
توضح تسميات المحاور العلامة والفلوركروم المستخدم (مثل CD4-FITC).
المقاييس على المحاور مرئية بوضوح. قم بتضمين الأرقام على المحاور فقط للرسم البياني في أسفل اليسار من المجموعة (المجموعة هي تحليل للعلامات المتطابقة).
جميع الرسوم البيانية هي رسوم بيانية متساوية الارتفاع مع نقاط شاذة أو رسوم بيانية بالألوان الزائفة.
تم توفير قيمة عددية لعدد الخلايا أو النسبة المئوية (مع الإحصائيات).
المنهجية
تحضير العينة
تم تعريف خلايا ILC2 في الفئران على أنها حية، CD45+، سلالة- (CD3، CD5، NK1.1، CD11b، CD11c، CD19، FceR1)، CD90+. كانت جميع الخلايا الحية، CD45+، سلالة-، CD90+ إيجابية لـ GATA3 (الشكل البياني الموسع 3a).
تم استخدام التعريفات التالية لخلايا المناعة الأخرى:
ILC1 - live, CD45+, lineage-, Tbet+
ILC3 - live, CD45+, lineage-,NK1.1-, Rorgt+
NK - live, CD45+, CD3-, NK1.1+
B cell - live, CD45+, CD3-, NK1.1-, CD19+
CD4+ T cell - live, CD45+, NK1.1-, CD3+, CD8-, CD4+
الحمضات – حية، CD45+، NK1.1-، CD3-، CD19-، CD11b+ SiglecF+
البلاعم – حية، CD45+، NK1.1-، CD3-، CD19-، CD11b+، F4/80+
خلية مثبطة مشتقة من النخاع العظمي (MDSC) – حية، CD45+، NK1.1-، CD3-، CD19-، CD11b+، SiglecF-، Gr-1+
الخلايا الشجرية (DCs) – حية، CD45+، NK1.1-، CD3-، CD19-، Gr-1-، F4/80-، CD11c+، MHC-II+
تم تعريف خلايا ILC2 البشرية على أنها حية، CD45+، سلالة- (CD3، CD5، CD56، CD11b، CD11c، CD14، CD16، CD19، TCRa/b، FceR1)، CD127+، CRTH2+.
خدمة المناعة وعلم الأورام، برنامج الأورام البشرية وعلم الأمراض، مركز ميموريال سلوان كيتيرينغ للسرطان، نيويورك، نيويورك، الولايات المتحدة الأمريكية. خدمة الكبد والبنكرياس والقنوات الصفراوية، قسم الجراحة، مركز ميموريال سلوان كيترينغ للسرطان، نيويورك، نيويورك، الولايات المتحدة الأمريكية. معهد جيل روبرتس للبحوث في مرض الأمعاء الالتهابي، وايل كورنيل للطب، نيويورك، نيويورك، الولايات المتحدة الأمريكية. مركز فريدمان للتغذية والالتهابات، وييل كورنيل ميديسن، جامعة كورنيل، نيويورك، نيويورك، الولايات المتحدة الأمريكية. مركز ألين لاكتشاف التفاعلات العصبية المناعية، نيويورك، نيويورك، الولايات المتحدة الأمريكية. قسم الطب في جامعة جوان وسانفورد آي. ويل، قسم أمراض الجهاز الهضمي والكبد، وييل كورنيل ميديسن، جامعة كورنيل، نيويورك، نيويورك، الولايات المتحدة الأمريكية. قسم الميكروبيولوجيا وعلم المناعة، وييل كورنيل ميديسن، جامعة كورنيل، نيويورك، نيويورك، الولايات المتحدة الأمريكية. خدمة علم الأورام الحاسوبية، قسم الوبائيات وعلم الإحصاء الحيوي، مركز ميموريال سلوان كيتيرينغ للسرطان، نيويورك، نيويورك، الولايات المتحدة الأمريكية. مركز ديفيد م. روبنشتاين لأبحاث سرطان البنكرياس، مركز ميموريال سلوان كيترينغ للسرطان، نيويورك، نيويورك، الولايات المتحدة الأمريكية. قسم الإحصاء الحيوي وعلم الأوبئة، مركز ميموريال سلوان كيتيرينغ للسرطان، نيويورك، نيويورك، الولايات المتحدة الأمريكية. مرفق تدفق الخلايا، مركز ميموريال سلوان كيتيرينغ للسرطان، نيويورك، نيويورك، الولايات المتحدة الأمريكية. قسم الميكروبيولوجيا، المناعة وعلم الوراثة الجزيئية، مركز جامعة تكساس للعلوم الصحية في سان أنطونيو، سان أنطونيو، تكساس، الولايات المتحدة الأمريكية. معهد اكتشاف العلاجات الثلاثي المؤسسي، نيويورك، نيويورك، الولايات المتحدة الأمريكية. مركز العليان لقاحات السرطان، مركز ميموريال سلوان كيتيرينغ للسرطان، نيويورك، نيويورك، الولايات المتحدة الأمريكية. علم وظائف الأعضاء، الفيزياء الحيوية وعلم الأحياء النظامية، وييل كورنيل للطب، كلية وييل كورنيل للطب، نيويورك، نيويورك، الولايات المتحدة الأمريكية. مركز سرطان ساندرا وإدوارد ماير، وييل كورنيل ميديسن، كلية وييل كورنيل للطب، نيويورك، نيويورك، الولايات المتحدة الأمريكية. معهد باركر لعلاج السرطان المناعي، وايل كورنيل للطب، نيويورك، نيويورك، الولايات المتحدة الأمريكية. سباحة عبر أمريكا ومختبر لودفيغ التعاوني، قسم علم الأدوية، وييل كورنيل للطب، نيويورك، نيويورك، الولايات المتحدة الأمريكية. ساهم هؤلاء المؤلفون بالتساوي: ماساتاكا أميساكي، عبد الرزاق زببود. البريد الإلكتروني: balachav@mskcc.org - كراتز، أ.، كامبوس-نيتو، أ.، هانسون، م. س. ورادل، ن. هـ. الالتهاب المزمن الناتج عن اللمفوتوكسين هو تكوين أنسجة لمفاوية جديدة. ج. إكسب. ميد. 183، 1461-1472 (1996).
- سكوت، آي. سي. وآخرون. يتم تنشيط الإنترلوكين-33 بواسطة أنشطة البروتياز المرتبطة بالحساسية والنخر لتنظيم نشاطه كمنبه خلال تلف الظهارة. ساي. ريب. 8، 3363 (2018).
- ساوتيس-فريدمان، سي.، بيتيبرز، ف.، كالديرارو، ج. وفريدمان، و. هـ. الهياكل اللمفاوية الثانوية في عصر علاج السرطان المناعي. نات. ريف. كانسر 19، 307-325 (2019).
- كابريتا، ر. وآخرون. الهياكل اللمفاوية الثانوية تحسن العلاج المناعي والبقاء في الميلانوما. ناتشر 577، 561-565 (2020).
- بيتيبر، ف. وآخرون. ترتبط خلايا B بالبقاء واستجابة العلاج المناعي في الساركوما. ناتشر 577، 556-560 (2020).
- هيلمينك، ب. أ. وآخرون. خلايا ب والهياكل اللمفاوية الثلاثية تعزز استجابة العلاج المناعي. ناتشر 577، 549-555 (2020).
- كوبولا، د. وآخرون. هياكل فريدة تشبه العقد اللمفاوية الهاجرة موجودة في سرطان القولون والمستقيم الأولي البشري تم تحديدها من خلال تحليل جينات المناعة. المجلة الأمريكية لعلم الأمراض 179، 37-45 (2011).
- Gu-Trantien، C. وآخرون. CD4
تسلل خلايا T المساعدة الجريبية يتنبأ ببقاء مرضى سرطان الثدي. J. Clin. Invest. 123، 2873-2892 (2013). - هيروكا، ن. وآخرون. العضو اللمفاوي الثالث داخل الورم هو مؤشر إيجابي في مرضى سرطان البنكرياس. المجلة البريطانية للسرطان 112، 1782-1790 (2015).
- ليو، ف. ي.، جيرارد، ج.-ب. وتورنكويست، هـ. ر. الإنترلوكين-33 في الصحة والمرض. نات. ريف. إيمونول. 16، 676-689 (2016).
- درايتون، د. ل.، يينغ، إكس.، لي، ج.، ليسلاور، و. ورادل، ن. هـ. يوجه LTaß خارج الموقع تكوين الأعضاء اللمفاوية مع التعبير المتزامن عن عنوان العقدة الطرفية وسلفوترانسفيراز مقيد بالأوعية الدموية اللمفاوية. ج. إكسب. ميد. 197، 1153-1163 (2003).
- لوكاشيف، م. وآخرون. استهداف اللمفوتوكسين-
مستقبل مع أجسام مضادة منشطة كعلاج محتمل للسرطان. أبحاث السرطان. 66، 9617-9624 (2006). - رينرت، ب. د.، جيمس، د.، ماكاي، ف.، براوننج، ج. ل. و هوشمان، ب. س. إن تكوين العقد اللمفاوية يتم تحفيزه من خلال الإشارات عبر اللمفوتوكسين
المستقبل. المناعة 9، 71-79 (1998). - لوخنر، م. وآخرون. الأنسجة اللمفاوية الثلاثية المستحثة بواسطة الميكروبيوم تزيد من حدة الأمراض الالتهابية في غياب خلايا RORyt و LTi. ج. تجريبي. طب. 208، 125-134 (2010).
- شومخر، ت. ن. وثومين، د. س. الهياكل اللمفاوية الثلاثية في السرطان. العلوم 375، eabf9419 (2022).
DOI: https://doi.org/10.1038/s41586-024-08426-5
PMID: https://pubmed.ncbi.nlm.nih.gov/39814891
Publication Date: 2025-01-15
IL-33-activated ILC2s induce tertiary lymphoid structures in pancreatic cancer
Received: 25 October 2021
Accepted: 19 November 2024
Published online: 15 January 2025
Open access
Check for updates
Abstract
Tertiary lymphoid structures (TLSs) are de novo ectopic lymphoid aggregates that regulate immunity in chronically inflamed tissues, including tumours. Although TLSs form due to inflammation-triggered activation of the lymphotoxin (LT)-LTβ receptor (LT/ßR) pathway
ectopic lymphoid organs, termed TLSs, are ubiquitous structures that regulate immunity in chronically inflamed tissues

survival (
that are preformed, TLSs assemble de novo in chronically inflamed tissues. As such, inflammation-induced drivers and cells that induce TLSs remain incompletely identified.
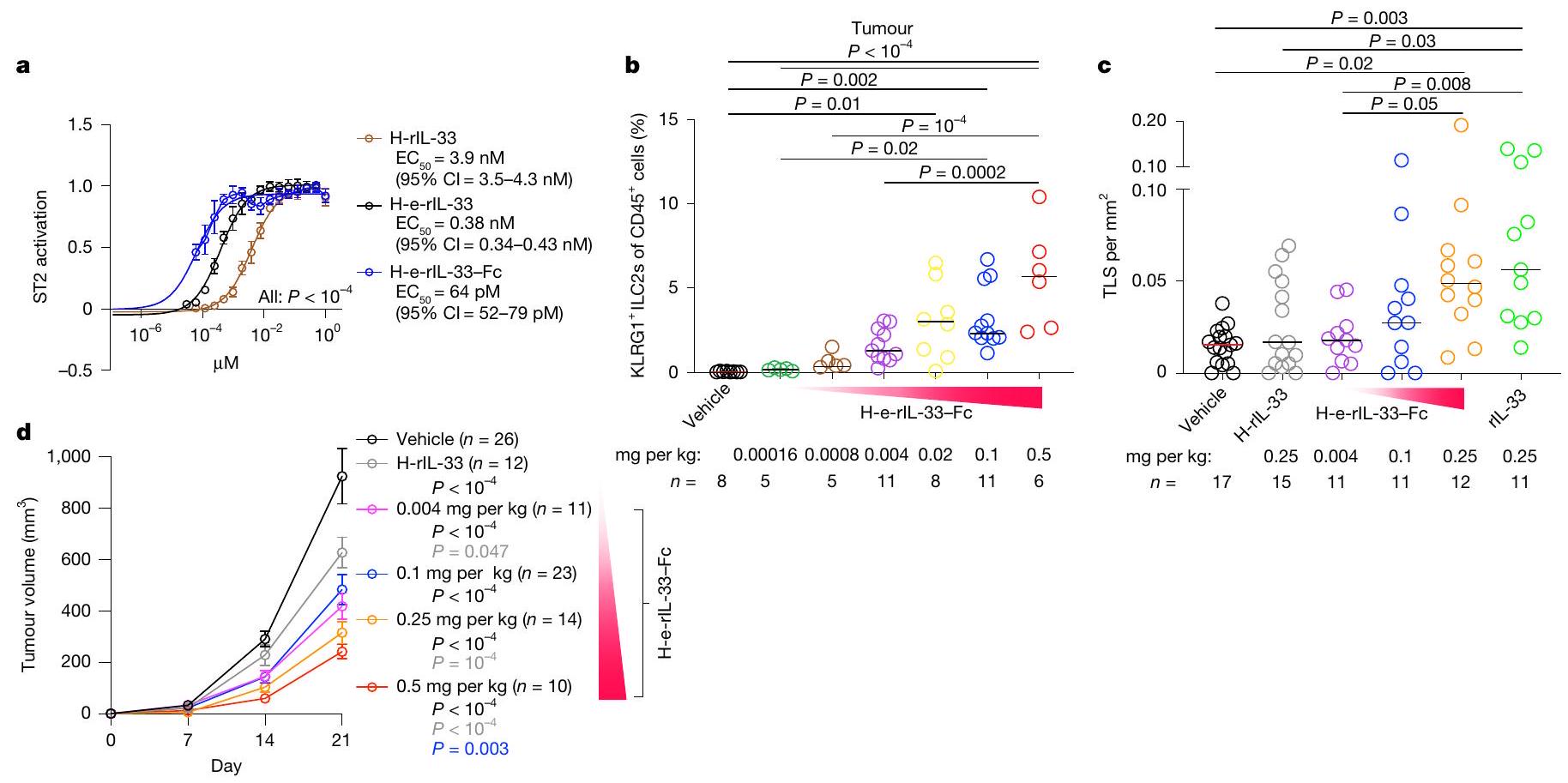
IL-33 mediates lymphoneogenesis
(Fig.1c (left), Extended Data Fig. 1c,d and Supplementary Table 2) that were more abundant in tumours compared with in adjacent pancreatic tissues (Fig. 1c (middle) and 1d (left)), and enriched in tumours with TLSs compared with those without (Fig. 1d (middle)). Furthermore, higher intratumoural IL-

in vehicle-treated and rIL-33-treated DSS-colitis mice. Data were collected 2 weeks (
weight loss and enhanced mouse survival (Extended Data Fig. 2g). Thus, the alarmin IL-33 triggers lymphoneogenesis in cancer and inflammation.
IL-33 expands lymphoneogenic ILC2s

and the number of DLN immune cells (right) in rlL-33-treated Nmur1
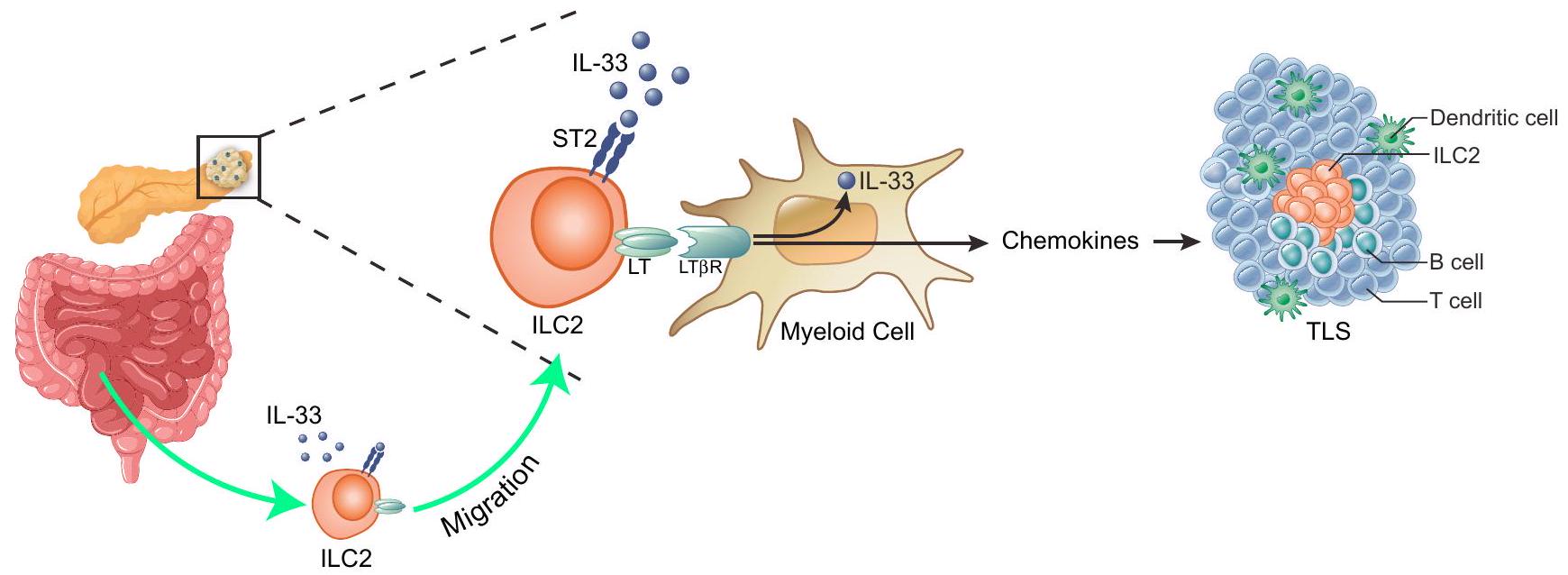
In SLOs and TLSs, inducer cells express LT that binds to LTβR on TLS organizer cells to stimulate the expression of chemokines and adhesion molecules, and coordinate lymphoneogenesis
a distinct transcriptome (Extended Data Fig. 5b-e and Supplementary Table 4), with higher TLS-inducing chemokines, including Cxcl13
Lymphoneogenic ILC2s can migrate from the gut
As ILC2s can migrate to tissues from the gut


regression. Data were collected at
to acute infections as, although both rIL-33 and rIL-25 expanded
Engineered IL-33 amplifies lymphoneogenesis
As the presence of
bonding and conformational changes that disrupt the ST2-binding site of IL-33, we substituted all four cysteine residues in human IL-33
Discussion
the hallmark of a novel TLS pathway. Physiologically, this organizational structure would logically preprogram SLOs at defined anatomical locations and equip migratory cells with molecular machinery to traffic to tissues to induce TLSs.
Our finding that PDAC primes this host lymphoneogenic response from the gut and is modulated by microbiota is notable, as a precise understanding of cells that link gut microbiota to both TLSs and tumour immunity remains in evolution. However, we did not investigate, and therefore cannot rule out, the functional contributions of ILC2s migrating to tumours from other sources, or of non-migratory ILC2s. Thus, as circulating ILC2s can derive from different tissue reservoirs
The ability to engineer the IL-33-ST2 pathway to boost TLSs and potentially control PDAC could have implications for cancer immunotherapy. As PDAC phenocopies the approximately
Online content
Article
- Moral, J. A. et al. ILC2s amplify PD-1 blockade by activating tissue-specific cancer immunity. Nature 579, 790-796 (2020).
- Klose, C. S. N. et al. The neuropeptide neuromedin U stimulates innate lymphoid cells and type 2 inflammation. Nature 549, 282-286 (2017).
- Wallrapp, A. et al. The neuropeptide NMU amplifies ILC2-driven allergic lung inflammation. Nature 549, 351-356 (2017).
- Cardoso, V. et al. Neuronal regulation of type 2 innate lymphoid cells via neuromedin U. Nature 549, 277-281 (2017).
- Tsou, A. M. et al. Neuropeptide regulation of non-redundant ILC2 responses at barrier surfaces. Nature 611, 787-793 (2022).
- Jarick, K. J. et al. Non-redundant functions of group 2 innate lymphoid cells. Nature 611, 794-800 (2022).
- Nussbaum, J. C. et al. Type 2 innate lymphoid cells control eosinophil homeostasis. Nature 502, 245-248 (2013).
- Gogoi, M. et al. ILC2-derived LIF licences progress from tissue to systemic immunity. Nature 632, 885-892 (2024).
- Oliphant, C. J. et al. MHCII-mediated dialog between group 2 innate lymphoid cells and
cells potentiates type 2 immunity and promotes parasitic helminth expulsion. Immunity 41, 283-295 (2014). - Ansel, K. M. et al. A chemokine-driven positive feedback loop organizes lymphoid follicles. Nature 406, 309-314 (2000).
- Luther, S. A. et al. Differing activities of homeostatic chemokines CCL19, CCL21, and CXCL12 in lymphocyte and dendritic cell recruitment and lymphoid neogenesis. J. Immunol. 169, 424-433 (2002).
- Meier, D. et al. Ectopic lymphoid-organ development occurs through interleukin 7-mediated enhanced survival of lymphoid-tissue-inducer cells. Immunity 26, 643-654 (2007).
- Sarafi, M. N., Garcia-Zepeda, E. A., MacLean, J. A., Charo, I. F. & Luster, A. D. Murine monocyte chemoattractant protein (MCP)-5: a novel CC chemokine that is a structural and functional homologue of human MCP-1. J. Exp. Med. 185, 99-110 (1997).
- Zhao, X. et al. CCL9 is secreted by the follicle-associated epithelium and recruits dome region Peyer’s patch CD11b
dendritic cells. J. Immunol. 171, 2797-2803 (2003). - Zhang, M. et al. CCL7 recruits cDC1 to promote antitumor immunity and facilitate checkpoint immunotherapy to non-small cell lung cancer. Nat. Commun. 11, 6119 (2020).
- Huang, Y. et al. IL-25-responsive, lineage-negative KLRG1(hi) cells are multipotential “inflammatory” type 2 innate lymphoid cells. Nat. Immunol. 16, 161-169 (2015).
- Huang, Y. et al. S1P-dependent interorgan trafficking of group 2 innate lymphoid cells supports host defense. Science 359, 114-119 (2018).
- Pu, Q. et al. Gut microbiota regulate gut-lung axis inflammatory responses by mediating ILC2 compartmental migration. J. Immunol. 207, 257-267 (2021).
- Ricardo-Gonzalez, R. R. et al. Tissue-specific pathways extrude activated ILC2s to disseminate type 2 immunity. J. Exp. Med. 217, 171 (2020).
- Flamar, A.-L. et al. Interleukin- 33 induces the enzyme tryptophan hydroxylase 1 to promote inflammatory group 2 innate lymphoid cell-mediated immunity. Immunity https://doi.org/10.1016/j.immuni.2020.02.009 (2020).
- Pushalkar, S. et al. The pancreatic cancer microbiome promotes oncogenesis by induction of innate and adaptive immune suppression. Cancer Discov. 8, 403-416 (2018).
- Cohen, E. S. et al. Oxidation of the alarmin IL-33 regulates ST2-dependent inflammation. Nat. Commun. 6, 1-10 (2015).
- Alt, C. et al. Long-acting IL-33 mobilizes high-quality hematopoietic stem and progenitor cells more efficiently than granulocyte colony-stimulating factor or AMD3100. Biol. Blood Marrow Transplant 25, 1475-1485 (2019).
- Schmitz, J. et al. IL-33, an interleukin-1-like cytokine that signals via the IL-1 receptor-related protein ST2 and induces T helper type 2-associated cytokines. Immunity 23, 479-490 (2005).
- Sawa, S. et al. Lineage relationship analysis of RORyt
innate lymphoid cells. Science 330, 665-669 (2010). - Ikeda, A. et al. Human NKp44
group 3 innate lymphoid cells associate with tumorassociated tertiary lymphoid structures in colorectal cancer. Cancer Immunol. Res. 8, 724-731 (2020). - Peters, A. et al. Th17 cells induce ectopic lymphoid follicles in central nervous system tissue inflammation. Immunity 35, 986-996 (2011).
- Jacquelot, N. et al. Blockade of the co-inhibitory molecule PD-1 unleashes ILC2-dependent antitumor immunity in melanoma. Nat. Immunol. https://doi.org/10.1038/s41590-021-00943-z (2021).
- Alonso-Curbelo, D. et al. A gene-environment-induced epigenetic program initiates tumorigenesis. Nature 590, 642-648 (2021).
- Howard, A. D. et al. Identification of receptors for neuromedin
and its role in feeding. Nature 406, 70-74 (2000). - Qi, F. et al. Macrophages produce IL-33 by activating MAPK signaling pathway during RSV infection. Mol. Immunol. 87, 284-292 (2017).
- Kabashima, K. et al. Intrinsic lymphotoxin-beta receptor requirement for homeostasis of lymphoid tissue dendritic cells. Immunity 22, 439-450 (2005).
- Hung, L.-Y. et al. Cellular context of IL-33 expression dictates impact on anti-helminth immunity. Sci. Immunol. 5, eabc6259 (2020).
- Zhang, M. et al. A translocation pathway for vesicle-mediated unconventional protein secretion. Cell 181, 637-652.e15 (2020).
- Alam, A. et al. Fungal mycobiome drives IL-33 secretion and type 2 immunity in pancreatic cancer. Cancer Cell 40, 153-167.e11 (2022).
(c) The Author(s) 2025
Methods
Mice
Cell lines and animal procedures
of
Microbiome analysis
Recombinant H-rlL-33 and H-e-rlL-33-Fc
Recombinant IL-33, IL-25, H-rIL-33 and H-e-rIL-33-Fc treatment
Human samples
flow cytometry; Supplementary Tables 2 and 5). The human PDAC tissue microarrays
Tumour transcriptomic profiling
Cell isolation
ILC2 and myeloid cell adoptive transfer
Flow cytometry
were defined as live
H&E staining
Serum IL-33 detection
Immunohistochemistry
Immunofluorescence
followed by incubation with Tyramide Alexa 647 (Invitrogen) prepared according to the manufacturer’s instructions with predetermined dilutions. After staining, the slides were counterstained with DAPI (Sigma-Aldrich) for 10 min and cover-slipped with Mowiol.
B cell receptor sequencing
Somatic hypermutation
Digital droplet PCR
scRNA-seq
indexes provided in the kit (
TLS and ILC2 transcriptional signatures
expression in the TCGA-PAAD dataset described above using the TMM method
Confocal microscopy
In vitro studies
Statistics
Material availability
Reporting summary
Data availability
data are available under Gene Expression Omnibus (GEO) accession number GSE184585. scRNA-seq data of ILC2s have been previously reported
51. Tumanov, A. et al. Distinct role of surface lymphotoxin expressed by B cells in the organization of secondary lymphoid tissues. Immunity 17, 239-250 (2002).
52. Fütterer, A., Mink, K., Luz, A., Kosco-Vilbois, M. H. & Pfeffer, K. The lymphotoxin beta receptor controls organogenesis and affinity maturation in peripheral lymphoid tissues. Immunity 9, 59-70 (1998).
53. Nowotschin, S. & Hadjantonakis, A.-K. Use of KikGR a photoconvertible green-to-red fluorescent protein for cell labeling and lineage analysis in ES cells and mouse embryos. BMC Dev. Biol. 9, 49 (2009).
54. Haybaeck, J. et al. A lymphotoxin-driven pathway to hepatocellular carcinoma. Cancer Cell 16, 295-308 (2009).
55. Wirtz, S. et al. Chemically induced mouse models of acute and chronic intestinal inflammation. Nat. Protoc. 12, 1295-1309 (2017).
56. Arifuzzaman, M. et al. Dietary fiber is a critical determinant of pathologic ILC2 responses and intestinal inflammation. J. Exp. Med. 221, e20232148 (2024).
57. Zegarra-Ruiz, D. F. et al. Thymic development of gut-microbiota-specific T cells. Nature 594, 413-417 (2021).
58. Tommaso, P. D. et al. Nextflow enables reproducible computational workflows. Nat. Biotechnol. 35, 316-319 (2017).
59. Ewels, P. A. et al. The nf-core framework for community-curated bioinformatics pipelines. Nat. Biotechnol. 38, 276-278 (2020).
60. Straub, D. et al. Interpretations of environmental microbial community studies are biased by the selected 16 S rRNA (gene) amplicon sequencing pipeline. Front. Microbiol. 11, 550420 (2020).
61. Martin, M. Cutadapt removes adapter sequences from high-throughput sequencing reads. EMBnet J. https://doi.org/10.14806/ej.17.1.200 (2011).
62. Callahan, B. J. et al. DADA2: high-resolution sample inference from Illumina amplicon data. Nat. Methods 13, 581-583 (2016).
63. Quast, C. et al. The SILVA ribosomal RNA gene database project: improved data processing and web-based tools. Nucleic Acids Res. 41, D590-D596 (2013).
64. Bailey, P. et al. Genomic analyses identify molecular subtypes of pancreatic cancer. Nature 531, 47-52 (2016).
65. Liu, J. et al. An integrated TCGA pan-cancer clinical data resource to drive high-quality survival outcome analytics. Cell 173, 400-416 (2018).
66. Raphael, B. J. et al. Integrated genomic characterization of pancreatic ductal adenocarcinoma. Cancer Cell 32, 185-203.e13 (2017).
67. Berger, A. C. et al. A comprehensive pan-cancer molecular study of gynecologic and breast cancers. Cancer Cell 33, 690-705 (2018).
68. Network, T. C. G. A. et al. Genomic classification of cutaneous melanoma. Cell 161, 1681-1696 (2015).
69. Bando, J. K., Liang, H.-E. & Locksley, R. M. Identification and distribution of developing innate lymphoid cells in the fetal mouse intestine. Nat. Immunol. 16, 153-160 (2014).
70. Chiang, E. Y. et al. Targeted depletion of lymphotoxin-a-expressing TH1 and TH17 cells inhibits autoimmune disease. Nat. Med. 15, 766-773 (2009).
71. Rodriguez, A. B. et al. Immune mechanisms orchestrate tertiary lymphoid structures in tumors via cancer-associated fibroblasts. Cell Rep. 36, 109422 (2021).
72. Silina, K. et al. Germinal centers determine the prognostic relevance of tertiary lymphoid structures and are impaired by corticosteroids in lung squamous cell carcinoma. Cancer Res. 78, 1308-1320 (2017).
73. Posch, F. et al. Maturation of tertiary lymphoid structures and recurrence of stage II and III colorectal cancer. Oncoimmunology 7, e1378844 (2017).
74. Calderaro, J. et al. Intra-tumoral tertiary lymphoid structures are associated with a low risk of early recurrence of hepatocellular carcinoma. J. Hepatol. 70, 58-65 (2019).
75. Vanhersecke, L. et al. Mature tertiary lymphoid structures predict immune checkpoint inhibitor efficacy in solid tumors independently of PD-L1 expression. Nat. Cancer 2, 794-802 (2021).
76. Carlson, C. S. et al. Using synthetic templates to design an unbiased multiplex PCR assay. Nat. Commun. 4, 2680 (2013).
77. Gabernet, G. et al. nf-core/airrflow: an adaptive immune receptor repertoire analysis workflow employing the Immcantation framework. PLoS Comput. Biol. 20, e1012265 (2024).
78. Nouri, N. & Kleinstein, S. H. Somatic hypermutation analysis for improved identification of B cell clonal families from next-generation sequencing data. PLoS Comput. Biol. 16, e1007977 (2020).
79. Gupta, N. T. et al. Change-O: a toolkit for analyzing large-scale B cell immunoglobulin repertoire sequencing data. Bioinformatics 31, 3356-3358 (2015).
80. Hänzelmann, S., Castelo, R. & Guinney, J. GSVA: gene set variation analysis for microarray and RNA-seq data. BMC Bioinform. 14, 7 (2013).
81. McCarthy, D. J., Campbell, K. R., Lun, A. T. L. & Wills, Q. F. Scater: pre-processing, quality control, normalization and visualization of single-cell RNA-seq data in R. Bioinformatics 33, btw777 (2017).
82. Cunningham, F. et al. Ensembl 2022. Nucleic Acids Res. 50, D988-D995 (2021).
83. Colaprico, A. et al. TCGAbiolinks: an R/Bioconductor package for integrative analysis of TCGA data. Nucleic Acids Res. 44, e71 (2016).
84. Silva, T. C. et al. TCGA Workflow: analyze cancer genomics and epigenomics data using Bioconductor packages. F100ORes. 5, 1542 (2016).
85. Mounir, M. et al. New functionalities in the TCGAbiolinks package for the study and integration of cancer data from GDC and GTEx. PLoS Comput. Biol. 15, e1006701 (2019).
86. Robinson, M. D. & Oshlack, A. A scaling normalization method for differential expression analysis of RNA-seq data. Genome Biol. 11, R25 (2010).
Additional information
Correspondence and requests for materials should be addressed to Vinod P. Balachandran. Peer review information Nature thanks Shigeo Koyasu and the other, anonymous, reviewer(s) for their contribution to the peer review of this work.
Reprints and permissions information is available at http://www.nature.com/reprints.

images of TLSs in human PDACs. e, f, Serum IL-33 in rlL-33-treated PDAC mice (e) and in human PDAC patients (f). g, Correlation of IL-33-activated human ILC2 transcriptional signature to TLS signatures (TLS signatures:


| CD8
|
|||
 |
|||
| 8 | PDAC 1 (
|
||
| 6 | ◯ | ||
 |
|||
| 4 | O | ||
| 2 |  |
 |
|
| Low | Moderate | ||



vehicle-treated and rIL-33-treated DSS-colitis mice. Data collected 2 (a), 3 (c, d PDAC 3, 4) and 3-5 (c, d PDAC 1, 2, 5, 6, e, f) weeks after tumour implantation, pooled from

Article
genes for each cluster. UMAP, violin plots = ILC transcription factors (h), and markers (i) in unsupervised clusters in Fig. 3a, and ILC2 cytokines (h). Tbx21 was undetectable.j, ILC transcription factors on intratumoural KLRG1

(middle) and immune cell frequency (right) in rll-33-treated


Extended Data Fig. 6| ILC2 gating strategy and frequency in parabiotic


Article
littermate Cre-control,

b

C




Article

nature research
Reporting Summary
Statistics
n/a

□
□
Confirmed
The exact sample size

The statistical test(s) used AND whether they are one- or two-sided
Only common tests should be described solely by name; describe more complex techniques in the Methods section.
□

□

□

□


□ For Bayesian analysis, information on the choice of priors and Markov chain Monte Carlo settings

□ For hierarchical and complex designs, identification of the appropriate level for tests and full reporting of outcomes
□ X
Estimates of effect sizes (e.g. Cohen’s
Software and code
Policy information about availability of computer code
For flow cytometry, all samples were analyzed on a FACS LSR Fortessa (BD Biosciences) using FlowJo (version 10.7.1, Tree Star).
Pathologic slides were digitized using Panoramic Flash 250 (3Dhistech, Budapest Hungary) using Zeiss 20x/0.8NA objective and custom filters for A488, A546, A594 and A647.
IHC: Nucleated cells in a TLS were determined and counted using the Analyze Particles function in ImageJ (ver. 2.3.0, NHI, USA). IL33+ cells in a TLS were counted manually.
Confocal: To visualize LT-PE and nuclear-DAPI, the images were taken on a point laser scanning confocal system (SP5, Leica, Wetzlar, Germany) with a 63x oil immersion objective 2.
ST2 reporter assay: 630-nm wavelength absorbance detection was performed on a Cytation 3 reader (BioTek).
B cell receptor sequencing: Immunosequencing of the CDR3 regions of mouse B cell receptor chains was performed on genomic DNA from FFPE-fixed samples using the immunoSEQ Assay (Adaptive Biotechnologies)
ddPCR: Droplet generation was performed on a QX200 ddPCR system (Bio-Rad) using cDNA generated from 0.8-2 ng total RNA with the OneStep RT-ddPCR Advanced Kit for Probes (Bio-Rad) according to the manufacturer’s protocol with reverse transcription at
extension at
Data analysis
Tumor transcriptomic profiling: Data were analyzed using
Flow cytometry: Data were analyzed using FlowJo (version 10.7.1, Tree Star).
H&E: The number of TLSs were determined in at least 3 sections using QuPath ver.0.2.3.
IF: IL33+ and IL33+CD45+ cells were quantified on ImageJ ver. 2.3.0, and cells per area estimated by calculating surface area based on presence of DAPI+ cells.
Single-cell RNA sequencing: Primary processing of sequencing images was done using Illumina’s Real Time Analysis software (RTA). 10X Genomics Cell Ranger Single Cell Software suite v3.0.2 (https://support.10xgenomics.com/ single-cell-gene-expression/software/pipelines/ latest/what-is-cellranger) was used to demultiplex samples, align to mouse genomic reference mm10, filter, count UMIs, single-cell 5′ end genes, and control quality per the manufacturer’s parameters. Processed data were subsequently analyzed in
Somatic hypermutation: Rearrangements with productive heavy chain sequences were retained for analysis of B cell clonal relationships, and clones were defined by VDJ-aware spectral clustering using the R package SCOPer. Mutation frequencies were computed using the observed mutations function in the R package Shazam
Data
Policy information about availability of data
- Accession codes, unique identifiers, or web links for publicly available datasets
- A list of figures that have associated raw data
- A description of any restrictions on data availability
Field-specific reporting
Life sciences □ Behavioural & social sciences □ Ecological, evolutionary & environmental sciences
For a reference copy of the document with all sections, see nature.com/documents/nr-reporting-summary-flat.pdf
Life sciences study design
Sample size
Sample sizes were determined based on our and other investigators experience with the respective cell lines used. No statistical methods were used as we observed many statistically significant effects in the data with the above methods of sample size selection without a priori sample size calculations.
No data were excluded from the analyses.
Reporting for specific materials, systems and methods
| n/a | Involved in the study |
| □ |  |
| □ | 【 Eukaryotic cell lines |
 |
□ Palaeontology and archaeology |
| □ | – Animals and other organisms |
| □ | 【 Human research participants |
 |
□ |
| V | □ |
|
|
Involved in the study |
|
|
|
|
|
Elow cytometry |
|
|
|
Antibodies
| Antibodies used |
|
Target Channel Antibody name Maker Catalog # Clone Amount
GATA3 PE PE Mouse anti-GATA3 BD Biosciences 560074 L50-823 4
PD-1 BV786 BV786 Mouse Anti-Human CD279 (PD-1) BD Biosciences 563789 EH12.1 2
RORgt BV650 BV650 Mouse anti-Human RORgt BD Biosciences 563424 Q21-559 2
Secondary Ab for hLTBR-Fc BV650 BV650 Mouse Anti-Human IgG BD Biosciences 740596 G18-145 2
Secondary Ab for hLTBR-Fc PE PE Mouse Anti-Human IgG BD Biosciences 555787 G18-145 2
CD117 PE-Cy5 PE/Cy5 anti-human CD117 (c-kit) BioLegend 323412 A3C6E2 2
CD11b APC APC anti-human CD11b BioLegend 301310 ICRF44 2
CD161 BV785 Brilliant Violet 785 anti-human CD161 BioLegend 339930 HP-3G10 2
CD25 APC-Cy7 APC/Cy7 anti-human CD25 BioLegend 302614 BC96 2
CD45 PacBlue Pacific Blue anti-human CD45 BioLegend 304029 HI30 2
CD56 BV605 Brilliant Violet 605 anti-human CD56 (NCAM) BioLegend 318334 HCD56 2
CRTH2 PerCP-Cy5.5 PerCP/Cy5.5 anti-human CD294 (CRTH2) BioLegend 350116 BM16 4
CRTH2 PE PE anti-human CD294 (CRTH2) BioLegend 350106 BM16 4
FceRIa APC APC anti-Human FceRIa BioLegend 334612 AER-37 2
ICOS BV711 Brilliant Violet 711 anti-human/mouse/rat CD278 (ICOS) BioLegend 313548 C398.4A 2
NKp44 PE-Cy7 PE/Cy7 anti-human CD336 (NKp44) BioLegend 325116 P44-8 2
T-BET BV711 Brilliant Violet 711 anti-Tbet BioLegend 6448204 B10 2
TCR a/b AF700 Alexa Fluor 700 anti-human TCR a/b BioLegend 306730 IP26 2
KLRG1 BV510 Brilliant Violet 510 anti-mouse/human KLRG1 BioLegend 138421 2F1/KLRG1 2
CD11c APC Anti-Hu CD11c, APC Invitrogen 17-0116-42 3.92
CD127 FITC Anti-Hu CD127, FITC Invitrogen 11-1278-42 eBioRDR5 2
CD14 APC Anti-Hu CD14, APC Invitrogen 17-0149-42 61D3 2
CD16 APC Anti-Hu CD16 Invitrogen 17-0168-42 eBioCB16 2
CD19 AF700 Anti-Hu CD19 Invitrogen 56-0199-42 HIB19 2
CD3 AF700 Anti-Hu CD3, Alexa Fluor 700 Invitrogen 56-0037-42 OKT3 2
CD5 APC Ant-Hu CD5, APC Invitrogen 17-0058-42 L17F12 2
ST2 PE Anti-Hu IL-33R (ST2), PE Invitrogen 12-9338-42 hIL33Rcap 4
Product name Maker Catalog # Application Concentration/Dose
rhLTBR/Fc Chimera R&D systems 629-LR Flow
rmLTBR/Fc Chimera R&D systems 1008-LR Flow
Recombinant Mouse IL-33 Protein R&D systems 3626-ML-010/CF Treatment (i.p.)
Recombinant Mouse IL-25 Protein R&D systems 1399-ML-010/CF Treatment (i.p.)
Diphtheria toxin (DT) EMD Millipore 322326100 ng
in vivo/ vitro material
Product name Maker Catalog # Application Dose Details
Lymphotoxin beta Receptor Monoclonal Antibody Invitrogen 16-5671-82 Culture N/A Clone 3C8
Lymphotoxin beta Receptor Monoclonal Antibody Invitrogen 16-5671-38 Vivo
Rat IgG1 kappa Isotype control Invitrogen
Validation
All antibodies were validated by the manufacturer and used per their instructions. In our experiments, isotype and/or FMO control samples were included. Additional information on validation can be found on the manufacturers’ websites.
Eukaryotic cell lines
(See ICLAC register)
Animals and other organisms
| Laboratory animals | C57BL/6 (wild-type [WT], CD45.2) and C57BL/6 CD45.1 mice were purchased from Jackson Laboratory. ||1r|1-/- (ST2 deficient) and II33-/- mice were a gift from M.J. Rosen. Ltbfl/fl mice were a gift from A.V. Tumanov. Nmur1iCre-eGFP ROSALSL-DTR mice are previously described24. Ltbfl/fl was crossed to Nmur1iCre-eGFP and II7rCre/+ to obtain Nmur1iCre-iGFP Ltbfl/fl and II7rCre/+Ltbfl/fl mice. II7rCre/+Rorafl/fl mice were a gift from A.N.J. McKenzie. Ltbr-/- mice were a gift from T.T. Lu. CAG-KikGR33 mice were a gift from G.E. Diehl. Germ-free mice were provided by the gnotobiotic facility at Weill Cornell Medical Center (MSK). For all experiments, 6-14-week old mice were age, and sex-matched and randomly assigned to specified treatment groups, with at least two independent experiments performed throughout. Both male and female animals were utilized. Animals were bred and maintained in a specific pathogen-free animal facility at Memorial Sloan Kettering Cancer Center. |
| Wild animals | No wild animals were used. |
| Field-collected samples | No field-collected samples were used in this study. |
| Ethics oversight | Animals were bred and maintained in a specific pathogen-free animal facility, and all experiments were conducted in accordance with an Institutional Animal Care and Use Committee (IACUC) approved protocol at Memorial Sloan Kettering Cancer Center (MSK) and in compliance with all relevant ethical regulations. |
Human research participants
Population characteristics
Clinical characteristics of patients in the tissue microarray, flow cytometry, ILC2 culturing, and transcriptomic cohorts are outlined in Supplementary Tables 1, 2, 3, and 5 and are provided below.
Characteristic n (%)
Sex
Male 40 (49)
Female 42 (51)
Age (y)
Median (IQR) 68 (62-75)
Tumor location
Head 53 (65)
Body/tail 29 (35)
Procedure
Pancreaticoduodenectomy 53 (65)
Distal pancreatectomy 29 (35)
pT
12 (2)
21 (1)
378 (95)
41 (1)
pN
033 (40)
148 (59)
x1 (1)
pM
081 (99)
11 (1)
Pathological Stage
IA 2 (2)
IB 1 (1)
IIA 30 (37)
IIB 47 (57)
III 1 (1)
IV 1 (1)
Surgical margin
Positive 9 (11)
Negative 71 (87)
NA 2 (2)
Adjuvant Treatment
Yes 61 (74)
No 21 (26)
Clinicopathological characteristics of PDAC patients in IHC and IF cohort (
Characteristic n (%)
Sex
Male 4 (36)
Female 7 (64)
Age (y)
Median (IQR) 70 (62-79)
Tumor location
Head 9 (82)
Body/tail 2 (18)
Procedure
Pancreaticoduodenectomy 9 (82)
Distal pancreatectomy 2 (18)
pT
10(0)
20(0)
3 11 (100)
4 (0)
pN
O (45)
16 (55)
pM
0 11 (100)
10(0)
Pathological stage
IIA 5 (45)
IIB 6 (55)
Surgical margin
Positive 4 (36)
Negative 7 (64)
Adjuvant treatment
Yes 11 (100)
No O (0)
Clinicopathological characteristics of PDAC patients in flow cytometry cohort (n = 9)
Characteristic n (%)
Sex
Male 4 (44)
Female 5 (55)
Age (y)
Median (IQR) 67 (63-80)
Procedure
Pancreaticoduodenectomy 6 (66)
Distal pancreatectomy 2 (22)
Total pancreatectomy 1 (11)
pT
14 (44)
23(33)
3 1 (11)
4 0 (0)
x 1 (11)
pN
O 4 (44)
11 (11)
22(22)
x2(22)
pM
O 4 (54)
11 (11)
23(33)
x 1 (11)
Pathological stage
l (33)
II 2 (22)
III 3 (33)
Local recurrence 1 (11)
Surgical margin
Positive 0 (0)
Negative 9(100)
Adjuvant treatment
Yes 7 (77)
No 2 (22)
Clinicopathological characteristics of PDAC patients with serum IL33 measurements (n=77)
Characteristic n (%)
Sex
Male 43 (56)
Female 34 (44)
All patients eligible for surgical resection at Memorial Sloan Kettering Cancer Center were recruited to participate in an Institutional Review Board-approved protocol. All patients who provided informed consent had samples collected; all study procedures were conducted in strict compliance with all ethical and institutional regulations. As patients were only recruited at Memorial Sloan Kettering Cancer Center, there is the potential for institution-specific selection bias. We do not believe that this potential bias would impact the results of this study.
All tissues were collected at Memorial Sloan Kettering Cancer Center under study protocol #15-149 that was approved by the Memorial Sloan Kettering Cancer Center Institutional Review Board. Informed consent was obtained for all patients. The study was in strict compliance with all institutional ethical regulations.
Flow Cytometry
Plots
The axis labels state the marker and fluorochrome used (e.g. CD4-FITC).
The axis scales are clearly visible. Include numbers along axes only for bottom left plot of group (a ‘group’ is an analysis of identical markers).
All plots are contour plots with outliers or pseudocolor plots.
A numerical value for number of cells or percentage (with statistics) is provided.
Methodology
Sample preparation
Mouse ILC2s were defined as live, CD45+, lineage- (CD3, CD5, NK1.1, CD11b, CD11c, CD19, FceR1), CD90+. All live, CD45+, lineage-, CD90+ cells were GATA3+ (Extended Data Figure 3a).
The following definitions were used for other immune cells:
ILC1 - live, CD45+, lineage-, Tbet+
ILC3 - live, CD45+, lineage-,NK1.1-, Rorgt+
NK - live, CD45+, CD3-, NK1.1+
B cell - live, CD45+, CD3-, NK1.1-, CD19+
CD4+ T cell - live, CD45+, NK1.1-, CD3+, CD8-, CD4+
Eosinophils – live, CD45+, NK1.1-, CD3-, CD19-, CD11b+ SiglecF+
Macrophage – live, CD45+, NK1.1-, CD3-, CD19-, CD11b+ , F4/80+
Myeloid derived suppressor cell (MDSC) – live, CD45+, NK1.1-, CD3-, CD19-, CD11b+ SiglecF- Gr-1+
Dendritic cells (DCs) – live, CD45+, NK1.1-, CD3-, CD19-, Gr-1-, F4/80-, CD11c+, MHC-II+
Human ILC2s were defined as live, CD45+, lineage- (CD3, CD5, CD56, CD11b, CD11c, CD14, CD16, CD19, TCRa/b, FceR1), CD127+, CRTH2+.
Immuno-Oncology Service, Human Oncology and Pathogenesis Program, Memorial Sloan Kettering Cancer Center, New York, NY, USA. Hepatopancreatobiliary Service, Department of Surgery, Memorial Sloan Kettering Cancer Center, New York, NY, USA. Jill Roberts Institute for Research in Inflammatory Bowel Disease, Weill Cornell Medicine, New York, NY, USA. Friedman Center for Nutrition and Inflammation, Weill Cornell Medicine, Cornell University, New York, NY, USA. Allen Discovery Center for Neuroimmune Interactions, New York, NY, USA. Joan and Sanford I. Weill Department of Medicine, Division of Gastroenterology and Hepatology, Weill Cornell Medicine, Cornell University, New York, NY, USA. 7Department of Microbiology and Immunology, Weill Cornell Medicine, Cornell University, New York, NY, USA. Computational Oncology Service, Department of Epidemiology & Biostatistics, Memorial Sloan Kettering Cancer Center, New York, NY, USA. David M. Rubenstein Center for Pancreatic Cancer Research, Memorial Sloan Kettering Cancer Center, New York, NY, USA. Department of Biostatistics & Epidemiology, Memorial Sloan Kettering Cancer Center, New York, NY, USA. Flow Cytometry Core Facility, Memorial Sloan Kettering Cancer Center, New York, NY, USA. Department of Microbiology, Immunology & Molecular Genetics, University of Texas Health Science Center at San Antonio, San Antonio, TX, USA. Tri-Institutional Therapeutics Discovery Institute, New York, NY, USA. The Olayan Center for Cancer Vaccines, Memorial Sloan Kettering Cancer Center, New York, NY, USA. Physiology, Biophysics & Systems Biology, Weill Cornell Medicine, Weill Cornell Medical College, New York, NY, USA. Sandra and Edward Meyer Cancer Center, Weill Cornell Medicine, Weill Cornell Medical College, New York, NY, USA. Parker Institute for Cancer Immunotherapy, Weill Cornell Medicine, New York, NY, USA. Swim Across America and Ludwig Collaborative Laboratory, Department of Pharmacology, Weill Cornell Medicine, New York, NY, USA. These authors contributed equally: Masataka Amisaki, Abderezak Zebboudj. e-mail: balachav@mskcc.org - Kratz, A., Campos-Neto, A., Hanson, M. S. & Ruddle, N. H. Chronic inflammation caused by lymphotoxin is lymphoid neogenesis. J. Exp. Med. 183, 1461-1472 (1996).
- Scott, I. C. et al. Interleukin- 33 is activated by allergen- and necrosis-associated proteolytic activities to regulate its alarmin activity during epithelial damage. Sci. Rep. 8, 3363 (2018).
- Sautès-Fridman, C., Petitprez, F., Calderaro, J. & Fridman, W. H. Tertiary lymphoid structures in the era of cancer immunotherapy. Nat. Rev. Cancer 19, 307-325 (2019).
- Cabrita, R. et al. Tertiary lymphoid structures improve immunotherapy and survival in melanoma. Nature 577, 561-565 (2020).
- Petitprez, F. et al. B cells are associated with survival and immunotherapy response in sarcoma. Nature 577, 556-560 (2020).
- Helmink, B. A. et al. B cells and tertiary lymphoid structures promote immunotherapy response. Nature 577, 549-555 (2020).
- Coppola, D. et al. Unique ectopic lymph node-like structures present in human primary colorectal carcinoma are identified by immune gene array profiling. Am. J. Pathol. 179, 37-45 (2011).
- Gu-Trantien, C. et al. CD4
follicular helper T cell infiltration predicts breast cancer survival. J. Clin. Invest. 123, 2873-2892 (2013). - Hiraoka, N. et al. Intratumoral tertiary lymphoid organ is a favourable prognosticator in patients with pancreatic cancer. Br. J. Cancer 112, 1782-1790 (2015).
- Liew, F. Y., Girard, J.-P. & Turnquist, H. R. Interleukin-33 in health and disease. Nat. Rev. Immunol. 16, 676-689 (2016).
- Drayton, D. L., Ying, X., Lee, J., Lesslauer, W. & Ruddle, N. H. Ectopic LTaß directs lymphoid organ neogenesis with concomitant expression of peripheral node addressin and a HEVrestricted sulfotransferase. J. Exp. Med. 197, 1153-1163 (2003).
- Lukashev, M. et al. Targeting the lymphotoxin-
receptor with agonist antibodies as a potential cancer therapy. Cancer Res. 66, 9617-9624 (2006). - Rennert, P. D., James, D., Mackay, F., Browning, J. L. & Hochman, P. S. Lymph node genesis is induced by signaling through the lymphotoxin
receptor. Immunity 9, 71-79 (1998). - Lochner, M. et al. Microbiota-induced tertiary lymphoid tissues aggravate inflammatory disease in the absence of RORyt and LTi cells. J. Exp. Med. 208, 125-134 (2010).
- Schumacher, T. N. & Thommen, D. S. Tertiary lymphoid structures in cancer. Science 375, eabf9419 (2022).
