DOI: https://doi.org/10.1038/s41591-024-03114-3
PMID: https://pubmed.ncbi.nlm.nih.gov/38977913
تاريخ النشر: 2024-07-01
سلامة الاستئصال بالمجال النبضي في أكثر من 17,000 مريض يعانون من الرجفان الأذيني في دراسة مانيفيست-17K
تاريخ القبول: 4 يونيو 2024
تاريخ النشر على الإنترنت: 8 يوليو 2024
(D) تحقق من التحديثات
الملخص
تظهر قائمة المؤلفين وانتماءاتهم في نهاية الورقة
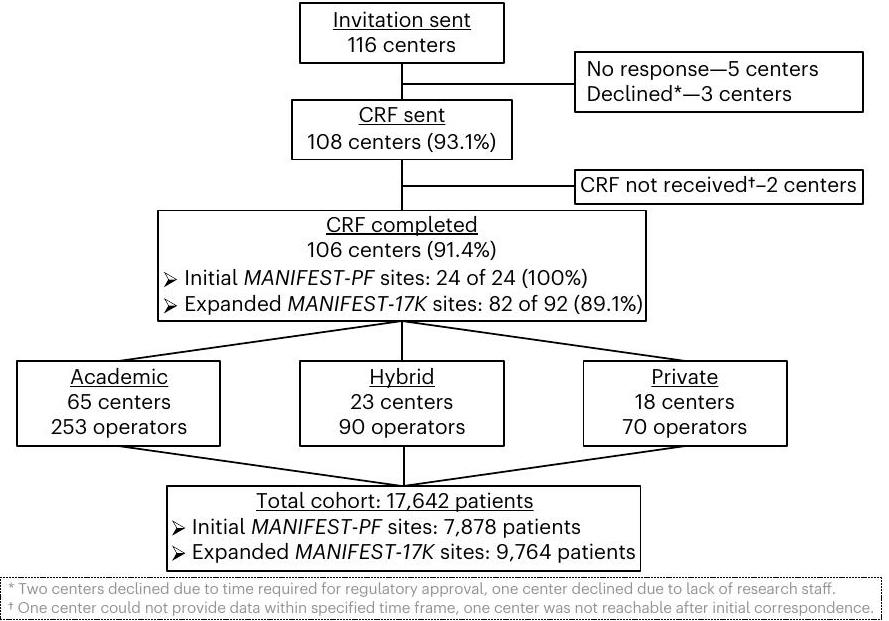
استئصال الحقل النبضي (PFA) هو تقنية ناشئة لعلاج الرجفان الأذيني (AF)، حيث تشير البيانات السريرية الأولية والبيانات المبكرة إلى بعض الدرجة من التفضيل لاستئصال الأنسجة القلبية دون إلحاق الضرر بالهياكل المجاورة. هنا في دراسة MANIFEST-17K قمنا بتقييم سلامة PFA من خلال دراسة الاستخدام بعد الموافقة لهذه الطريقة العلاجية. من بين 116 مركزًا يقومون بإجراء PFA بعد الموافقة باستخدام قسطرة بنتاسلاين، تم استلام بيانات من 106 مراكز (91.4% مشاركة) بشأن 17,642 مريضًا خضعوا لـ PFA (متوسط العمر 64،
خلال الاستئصال الحراري مع مرور الوقت، لا تزال هناك اعتبارات سلامة متبقية بما في ذلك خطر تضيق الأوردة الرئوية (PV)، السكتة الدماغية، شلل العصب الفرني وأخطر المضاعفات، الناسور الأذيني المريئي، الذي لا يزال اليوم له معدل وفيات يبلغ ~50% (المراجع 8-10).
النتائج
الخصائص الأساسية
نظرة عامة على AEs
يرجى الاطلاع على AEs الخاصة بالطاقة
| مجموعة MANIFEST-17K الكاملة
|
|
| ديموغرافي | |
| العمر (سنوات)، المتوسط (الحد الأدنى – الحد الأقصى) | 64 (11-96) |
| الإناث (%) | ٣٤.٧ |
| دلالة على الاستئصال | |
| الرجفان الأذيني المتقطع (%) | ٥٧.٨ |
| الرجفان الأذيني المستمر (%) | ٣٥.٢ |
| الرجفان الأذيني المستمر طويل الأمد (%) | ٥.٦ |
| رفرفة الأذين/تسرع الأذين (%) | 1.4 |
| تخدير | |
| التخدير العام (%) | ٤٦.٩ |
| التخدير العميق/عدم التهوية (%) | 53.1 |
الآثار الجانبية المحددة للطاقة غير المتعلقة بـ PFA
| مجموعة المرضى الكاملة من جميع مواقع MANIFEST-17K البالغ عددها 106
|
|
| المديرين الرئيسيين | 173 (0.98%) |
| الموت
|
5 (0.03%) |
| سكتة دماغية | 22 (0.12%) |
| ناسور المريء أو خلل الحركة | 0 (0%) |
| تضيق الأوردة الرئوية | 0 (0%) |
| إصابة العصب الحجابي (مستمرة)
|
0 (0%) |
| انصباب التامور
|
63 (0.36%) |
| التدخل عبر الجلد | 56 (0.32%) |
| التدخل الجراحي
|
7 (0.04%) |
| مضاعفات وعائية (مع تدخل) | 53 (0.30%) |
| تشنج الشريان التاجي | 25 (0.14%) |
| احتشاء عضلة القلب | 0 (0.0%) |
| فشل كلوي انحلال الدم (إقامة في المستشفى) | 5 (0.03%) |
| آخر (جلطة) | 1 (0.006%) |
| آثار جانبية طفيفة | 567 (3.21%) |
| نوبة إقفارية عابرة | 21 (0.12%) |
| إصابة العصب الحجابي (مؤقتة)
|
11 (0.06%) |
| انصباب التامور (دون تدخل) | ٥٩ (٠.٣٣٪) |
| التهاب التامور | 30 (0.17%) |
| المضاعفات الوعائية (بدون تدخل) | 388 (2.20%) |
| فشل كلوي بسبب انحلال الدم (دون الحاجة إلى دخول المستشفى) | 1 (0.006%) |
| مضاعفات أخرى | 57 (0.32%) |
الأشرطة الحمراء) وتمت ملاحظتها في مجموعة MANIFEST-17K المدروسة حاليًا (
| تشنج الشريان التاجي
|
|
| نوع التشنج: | |
| تشنج مرتبط بالقرب
|
22 (88%) |
| تشنج عام
|
3 (12%) |
| تغيرات تخطيط القلب الكهربائي | 23 (92%) |
| انخفاض ضغط الدم | 5 (20%) |
| المضاعفات السريرية | 4 (16%) |
| ألم في الصدر | 2 (8%) |
| الرجفان البطيني | 2 (8%) |
| تم إعطاء النيتروجليسرين عن طريق الوريد | 21 (84%) |
بما في ذلك عدد حالات PFA لكل موقع (182 (النطاق 17-707) مقابل
منحنى التعلم
| مضاعفات أخرى N=57 (0.32%) | |
| زراعة جهاز تنظيم ضربات القلب | 12 (0.07%) |
| الهواء الخثاري | 10 (0.06%) |
| خلل/انزلاق في السلك | 3 (0.02%) |
| كتلة أذينية بطينية | 3 (0.02%) |
| صداع نصفي | 3 (0.02%) |
| نفث الدم | 3 (0.02%) |
| انخفاض ضغط الدم المرتبط بالتخدير | 2 (0.01%) |
| فشل القلب | 2 (0.01%) |
| الالتهاب الرئوي | 2 (0.01%) |
| التهاب المعدة | 2 (0.01%) |
| متنوع | 15 (0.09%) |
نقاش
الإصابة. هذا يتماشى مع الدراسات السريرية السابقة، والدراسات الملاحظة، والدراسات السريرية العشوائية.
شريان تاجي أثناء استئصال الإسطوانة التاجية أو CTI، و (2) كانت الحالات المتبقية (
تطبيقات PFA ضروريًا، يجب النظر في تطبيق استراتيجيات تخفيف بسيطة مثل ترطيب المحلول الملحي.
المضاعفات المريئية، ومع معدل منخفض من المضاعفات الكبرى. حدث فشل كلوي مرتبط بتحلل الدم يتطلب غسيل الكلى، وإن كان نادرًا. أخيرًا، إن انخفاض حدوث تشنج الشرايين التاجية يخفي تداعياته الخطيرة المحتملة ويستدعي مزيدًا من الدراسة والإرشاد.
المحتوى عبر الإنترنت
References
- Mark, D. B. et al. Effect of catheter ablation vs medical therapy on quality of life among patients with atrial fibrillation. J. Am. Med. Assoc. 321, 1275-1285 (2019).
- Turagam, M. K. et al. Catheter ablation of atrial fibrillation in patients with heart failure. Ann. Intern. Med. 170, 41-50 (2018).
- Marrouche, N. F. et al. Catheter ablation for atrial fibrillation with heart failure. N. Engl. J. Med. 378, 417-427 (2018).
- Packer, D. L. et al. Ablation versus drug therapy for atrial fibrillation in heart failure: results from the CABANA trial. Circulation 143, 1377-1390 (2021).
- Kuck, K.-H. et al. Cryoballoon or radiofrequency ablation for symptomatic paroxysmal atrial fibrillation: reintervention, rehospitalization, and quality-of-life outcomes in the FIRE AND ICE trial. Eur. Heart J. 37, 2858-2865 (2016).
- Turagam, M. K. et al. Assessment of catheter ablation or antiarrhythmic drugs for first-line therapy of atrial fibrillation. JAMA Cardiol. 6, 697-705 (2021).
- Kirchhof, P. et al. Early rhythm-control therapy in patients with atrial fibrillation. N. Engl. J. Med. 383, 1305-1316 (2020).
- Tilz, R. R. et al. A worldwide survey on incidence, management, and prognosis of oesophageal fistula formation following atrial fibrillation catheter ablation: the POTTER-AF study. Eur. Heart J. 44, 2458-2469 (2023).
- Calkins, H. et al. HRS/EHRA/ECAS expert consensus statement on catheter and surgical ablation of atrial fibrillation. Europace 9, 335-379 (2007).
- Deshmukh, A. et al. In-hospital complications associated with catheter ablation of atrial fibrillation in the United States between 2000 and 2010. Circulation 128, 2104-2112 (2013).
- Kotnik, T., Rems, L., Tarek, M. & Miklavčič, D. Membrane electroporation and electropermeabilization: mechanisms and models. Annu. Rev. Biophys. 48, 63-91 (2019).
- Reddy, V. Y. et al. Ablation of atrial fibrillation with pulsed electric fields. JACC Clin. Electrophysiol. 4, 987-995 (2018).
- Neven, K. et al. Acute and long-term effects of full-power electroporation ablation directly on the porcine esophagus. Circ. Arrhythm. Electrophysiol. 10, e004672 (2017).
- Koruth, J. et al. Preclinical evaluation of pulsed field ablation: electrophysiological and histological assessment of thoracic vein isolation. Circ. Arrhythm. Electrophysiol. 12, e007781 (2019).
- Koruth, J. S. et al. Pulsed field ablation versus radiofrequency ablation: esophageal injury in a novel porcine model. Circ. Arrhythm. Electrophysiol. 13, e008303 (2020).
- Cochet, H. et al. Pulsed field ablation selectively spares the oesophagus during pulmonary vein isolation for atrial fibrillation. Europace 23, 1391-1399 (2021).
- Reddy, V. Y. et al. Pulsed field ablation for pulmonary vein isolation in atrial fibrillation. J. Am. Coll. Cardiol. 74, 315-326 (2019).
- Reddy, V. Y. et al. Pulsed field ablation of paroxysmal atrial fibrillation: 1-year outcomes of IMPULSE, PEFCAT, and PEFCAT II. JACC Clin. Electrophysiol. 7, 614-627 (2021).
- Reddy, V. Y. et al. Pulsed field ablation in patients with persistent atrial fibrillation. J. Am. Coll. Cardiol. 76, 1068-1080 (2020).
- Ekanem, E. et al. Multi-national survey on the methods, efficacy, and safety on the post-approval clinical use of pulsed field ablation (MANIFEST-PF). Europace 24, 1256-1266 (2022).
- Turagam, M. K. et al. Safety and effectiveness of pulsed field ablation to treat atrial fibrillation: one-year outcomes from the MANIFEST-PF registry. Circulation 148, 35-46 (2023).
- Schmidt, B. et al. European real-world outcomes with pulsed field ablation in patients with symptomatic atrial fibrillation: lessons from the multi-centre EU-PORIA registry. Europace 25, euad185 (2023).
- Reddy, V. Y. et al. Pulsed field or conventional thermal ablation for paroxysmal atrial fibrillation. N. Engl. J. Med. 389, 1660-1671 (2023).
- Kawasaki, R., Gauri, A., Elmouchi, D., Duggal, M. & Bhan, A. Atrioesophageal fistula complicating cryoballoon pulmonary vein isolation for paroxysmal atrial fibrillation. J. Cardiovasc. Electrophysiol. 25, 787-792 (2014).
- Metzner, A. et al. Increased incidence of esophageal thermal lesions using the second-generation
cryoballoon. Circ. Arrhythm. Electrophysiol. 6, 769-775 (2013). - Straube, F. et al. Comparison of the first and second cryoballoon: high-volume single-center safety and efficacy analysis. Circ. Arrhythm. Electrophysiol. 7, 293-299 (2014).
- Bakir, N. H. et al. Concomitant surgical ablation for atrial fibrillation is associated with increased risk of acute kidney injury but improved late survival. J. Thorac. Cardiovasc. Surg. 164, 1847-1857.e3 (2022).
- van Driel, V. J. H. M. et al. Low vulnerability of the right phrenic nerve to electroporation ablation. Heart Rhythm 12, 1838-1844 (2015).
- Yavin, H. et al. Pulsed field ablation using a lattice electrode for focal energy delivery: biophysical characterization, lesion durability, and safety evaluation. Circ. Arrhythm. Electrophysiol. 13, e008580 (2020).
- Kuroki, K. et al. Ostial dimensional changes after pulmonary vein isolation: pulsed field ablation vs radiofrequency ablation. Heart Rhythm 17, 1528-1535 (2020).
- Meissner, A. et al. Impact of irrigated energy application on the right coronary artery hemodynamics: FFR measurement in patients who underwent ablation of common type atrial flutter. J. Interv. Card. Electrophysiol. 21, 35-42 (2008).
- Wong, K. C. K. et al. High incidence of acute sub-clinical circumflex artery ‘injury’ following mitral isthmus ablation. Eur. Heart J. 32, 1881-1890 (2011).
- Reddy, V. Y. et al. Coronary arterial spasm during pulsed field ablation to treat atrial fibrillation. Circulation 146, 1808-1819 (2022).
- Zhang, C. et al. Coronary artery spasm during pulsed field vs radiofrequency catheter ablation of the mitral isthmus. JAMA Cardiol. https://doi.org/10.1001/jamacardio.2023.4405 (2023).
- Gunawardene, M. A. et al. Coronary spasm during pulsed field ablation of the mitral isthmus line. JACC Clin. Electrophysiol. 7, 1618-1620 (2021).
- Della Rocca, D. G. et al. Transient inferior ST-segment elevation and ventricular fibrillation after cavotricuspid isthmus pulsed-field ablation. JACC Clin. Electrophysiol. 9, 704-706 (2023).
- Nakamura, T. et al. Incidence and characteristics of coronary artery spasms related to atrial fibrillation ablation procedures -large-scale multicenter analysis. Circ. J. 85, 264-271 (2021).
- Kinosita, K. Jr. & Tsong, T. Y. Voltage-induced pore formation and hemolysis of human erythrocytes. Biochim. Biophys. Acta 471, 227-242 (1977).
- Moroz, V. V., Bogushevich, M. S., Chernysh, A. M., Kozlova, E. K. & Sharakshane, A. S. Effect of defibrillation pulses of different shapes on biomembranes: experimental study. Bull. Exp. Biol. Med. 137, 120-123 (2004).
- Davong, B. et al. Pulsed-field ablation on mitral isthmus in persistent atrial fibrillation: preliminary data on efficacy and safety. JACC Clin. Electrophysiol. 9, 1070-1081 (2023).
- Cheng, E. P. et al. Risk of mortality following catheter ablation of atrial fibrillation. J. Am. Coll. Cardiol. 74, 2254-2264 (2019).
- Kim, I.-C. et al. Incidence and predictors of silent embolic cerebral infarction following diagnostic coronary angiography. Int. J. Cardiol. 148, 179-182 (2011).
- Kahlert, P. et al. Silent and apparent cerebral ischemia after percutaneous transfemoral aortic valve implantation. Circulation 121, 870-878 (2010).
- Verma, A. et al. Pulsed field ablation for the treatment of atrial fibrillation: Pulsed af pivotal trial. Circulation 147, 1422-1432 (2023).
- Haeusler, K. G. et al. MRI-detected brain lesions and cognitive function in patients with atrial fibrillation undergoing left atrial catheter ablation in the randomized AXAFA-AFNET 5 trial. Circulation 145, 906-915 (2022).
© The Author(s) 2024
e-mail: vivek.reddy@mountsinai.org
طرق
نظرة عامة على الاستطلاع
إجراء PFA
تفاصيل بيانات الدراسة
إصابة العصب الحجابي (مؤقتة)، انصباب التامور (بدون تدخل)، مضاعفات وعائية (بدون تدخل)، انحلال الدم غير المتطلب للاستشفاء وأخرى.
تحليل البيانات
ملخص التقرير
توفر البيانات
مساهمات المؤلفين
المصالح المتنافسة
“جي. ك. يذكر أنه حصل على أتعاب شخصية من أبوت، بايوسنس ويبستر، بيترونيك، بوهينجر إنجلهايم، جي إي هيلث كير، ميدترونيك، فايزر، برو ميد سي إس، وفياتريس من أجل المحاضرات، اللجان الاستشارية، والاستشارات. بي. جي. حصل على منح من بي إس سي ومنحة آي إتش يو ليريك آي إتش يو-10-IAHU-04. جي.-بي. سي. تلقى تعويضات لأغراض التدريس والإشراف من ميدترونيك، أبوت، بيترونيك، بوسطن ساينتيفيك وأكوتس ميديكال. أ. بولافا حصل على دعم استشاري و/أو منح من أبوت، بيترونيك وبوسطن ساينتيفيك. ي. ب. حصل على منح بحثية من ميدترونيك وأتريكور وأتعاب استشارية من أبوت، بايوسنس ويبستر وبوسطن ساينتيفيك. جي. س. حصل على أتعاب شخصية من أبوت، باير، بوسطن ساينتيفيك، بايوسنس ويبستر إنك. ولومافيزيون خارج العمل المقدم. جي. ج. حصل على أتعاب شخصية من بوسطن ساينتيفيك. بي. س. حصل على أتعاب استشارية من بوسطن ساينتيفيك، بايوسنس ويبستر وميدترونيك. جي. سي. حصل على تمويل من بوسطن ساينتيفيك، ميدترونيك وبايوسنس ويبستر (التعليم). ك. ن. حصل على تمويل من بايوسنس ويبستر، بوسطن ساينتيفيك وميديكال فيلد. أ. ف. حصل على تمويل من بوسطن ساينتيفيك. جي. في. حصل على منح بحثية من ميدترونيك، بوسطن ساينتيفيك، أبوت، بيترونيك، داييتشي سانكيو، بي إم إس وفايزر. حصل على أتعاب من أبوت وداييتشي سانكيو، ودعم لحضور الاجتماعات من بايوسنس وبوسطن ساينتيفيك. يعمل في اللجنة الاستشارية لبوسطن ساينتيفيك وهو رئيس جمعية إيقاع القلب البلجيكية. إي. جي. يذكر أتعاب استشارية من ميدترونيك، بوسطن، مايكروبورت، أبوت وبيترونيك. بي. ك. حصل على منح بحثية من ميدترونيك، بوسطن ساينتيفيك، أبوت، بيترونيك، داييتشي سانكيو، بي إم إس وفايزر. حصل على أتعاب من أبوت وداييتشي سانكيو، ودعم لحضور الاجتماعات من بايوسنس وبوسطن ساينتيفيك. يعمل في اللجنة الاستشارية لبوسطن ساينتيفيك وهو رئيس جمعية إيقاع القلب البلجيكية. دي. شير يذكر أتعاب المتحدثين والاستشارات من بوسطن ساينتيفيك. م. م. يذكر أنه حصل على أتعاب المتحدثين من باير، بايوسنس ويبستر، بيترونيك، أمويد، أي أو بي أورفان، بوسطن ساينتيفيك، داييتشي سانكيو وبي إم إس/فايزر ومنح بحثية من بايوسنس ويبستر وأبوت. جي. إتش. يذكر أنه حصل على أتعاب المتحدثين ودعم المنح من بايوسنس ويبستر وميدترونيك. س. ب. يعمل كمستشار لميدترونيك، بوسطن ساينتيفيك، مايكروبورت وزول. آي. جي.-بي. حصل على أتعاب المتحدثين من بوسطن ساينتيفيك وأتعاب الإشراف من أبوت. أ. أ. عمل كمستشار لشركة بوسطن ساينتيفيك إنك، فارابولس إنك، غالاكسي ميديكال إنك، بايوسنس ويبستر وأرغا ميدتيك، وقد أبرم بحثًا مع بوسطن ساينتيفيك إنك، فارابولس إنك، غالاكسي ميديكال إنك، بايوسنس ويبستر، أرغا ميدتيك، فيوتشر كارديا إنك وأتاكور ميديكال إنك. ز. ج. عمل كمستشار لشركة بوسطن ساينتيفيك إنك وقد أبرم بحثًا مع أتاكور ميديكال إنك. دي. جي. حصل على منح بحثية من بوسطن ساينتيفيك. بي. دي. حصل على منح بحثية وأتعاب من بوسطن ساينتيفيك. سي. إس. هو عضو في اللجنة الاستشارية لميدترونيك في أوروبا ولجنة بوسطن ساينتيفيك الاستشارية في أوروبا. حصل على منح تعليمية من بايوسنس ويبستر وبيترونيك ومنحة بحثية من برنامج الاتحاد الأوروبي FP7 وبايوسنس ويبستر. يذكر أتعاب المحاضرات والاستشارات من أبوت، ميدترونيك، بايوسنس ويبستر، بوسطن ساينتيفيك، مايكروبورت وبيترونيك، جميعها خارج العمل المقدم. بي. إس. هو عضو في اللجنة الاستشارية لأبوت، بايوسنس ويبستر، بوسطن ساينتيفيك وميدترونيك. جي. أو. حصل على أتعاب المتحدثين من بوسطن ساينتيفيك، أبوت، بيترونيك وميدترونيك. م. غرامليخ حصل على أتعاب المتحدثين ومنح السفر من بوسطن ساينتيفيك. سي. تي. عمل في اللجنة الاستشارية وحصل على أتعاب المحاضرات/التدريس من بوسطن ساينتيفيك، ميدترونيك وأتريكور. حصل على أتعاب المحاضرات/التدريس من أبوت ميديكال. أ. دي. آر. حصل على أتعاب المتحدثين من بوسطن ساينتيفيك وأبوت. جي. إس. حصل على أتعاب المتحدثين ومنح السفر من بوسطن ساينتيفيك، بايوسنس ويبستر، م
“استشاري لشركة بوسطن ساينتيفيك، ميدترونيك ومايكروبورت CRM. تلقى A.M. أتعاب محاضرات ورسوم سفر من ميدترونيك، بوسطن ساينتيفيك، بايوسينس ويبسير، لايفتيك، BMS وباير. كما عمل كاستشاري لميدترونيك، بوسطن ساينتيفيك وبايوسينس ويبسير. عمل L.G. كاستشاري لشركة أبوت، ميدترونيك، بوسطن، بايوترونيك وجونسون آند جونسون. S.W. يذكر أنه تلقى منحًا ورسومًا شخصية من أبوت، بوسطن ساينتيفيك وميدترونيك، ورسومًا شخصية من بويرنجر إنجلهايم، بريستول مايرز سكويب، باير فيتال، أكوتوس، داييتشي وفارابولس إنك. M. غونارادين يذكر منحًا من فارابولس إنك وأبوت. تم دعم A. غوتي من خلال منحة الاتحاد الأوروبي هورايزون 2020 من مجموعة MAESTRIA برقم المنحة 965286 وتلقى رسوم متحدثين من أبوت، أسترازينيكا، باير هيلث كير، برلين كيمي، بايوترونيك، بويرنجر إنجلهايم، BMS/فايزر، بوسطن ساينتيفيك، داييتشي سانكيو، ميدترونيك، فيوفور، نوفارتس وسانوفي. C.M. تذكر أتعاب المحاضرات ورسوم المتحدثين من بوسطن ساينتيفيك، ميدترونيك، بايوسينس ويبسير، أكوتوس وأداجيو. عملت كاستشاري وعلى مجلس استشاري لبوسطن ساينتيفيك وميدترونيك. تلقت منحة بحثية من بوسطن ساينتيفيك. R.T. يذكر أنه تلقى رسوم استشارية من بوسطن ساينتيفيك، أبوت ميديكال، بايوترونيك وأتعاب محاضرات من بوسطن ساينتيفيك، أبوت ميديكال، بايوترونيك وبايوسينس ويبسير. A. جورج عمل كاستشاري لبوسطن ساينتيفيك وتلقى رسوم محاضرات من بوسطن ساينتيفيك. كما تلقى رسومًا للاستشارة و/أو المحاضرات من أبوت، أسترازينيكا، بارد، باير هيلث كير، بويرنجر إنجلهايم، بريستول-مايرز سكويب، إيلبين، جالينيكا، ليلي، ميدترونيك، ميناريني، MSD، فايزر، سانوفي، سيرفيير، يوني فارما وفيانكس. S.S. تلقى أتعاب محاضرات من ميدترونيك وأبوت، ومشاركة في تجارب سريرية مع أبوت، أبلكون، بوسطن وميدترونيك. R.B. تلقى أتعاب من بوسطن ساينتيفيك. T.D. تلقى رسوم استشارية من فارابولس (<2,000 دولار أمريكي)، رسوم متحدثين مع غالاكسي ميديكال (<1,000 دولار أمريكي) ورسوم متحدثين مع أبوت (<3,000 دولار أمريكي). A. غلونيك تلقى تعويضات عن مهام الإشراف والتحدث من ميدترونيك وعن مهام التحدث من أبوت وبوسطن. A.R. عمل كاستشاري لبوسطن ساينتيفيك. H.P. عمل كاستشاري/مجلس استشاري لأبوت، بايوسينس ويبسير، بوسطن ساينتيفيك وميدترونيك. D.D. تلقى أتعاب محاضرات متواضعة، منح سفر و/أو منحة زمالة من أبوت، أسترازينيكا، بايوترونيك، بويرنجر إنجلهايم، بوسطن ساينتيفيك، بريستول-مايرز سكويب، CVRx، ميدترونيك، مايكروبورت، فايزر وزول. D. ستيفن تلقى منحة بحثية <50,000 يورو ورسوم متحدثين <10,000 يورو من بايوسينس ويبسير وبوسطن ساينتيفيك. A.S. يذكر أنه تلقى أتعاب محاضرات واستشارات من ميدترونيك، أبوت وباير. J.S.S.G.d.J. كان استشاريًا لميدترونيك. R.W. يذكر أنه تلقى أتعاب محاضرات من أداجيو ميديكال، بويرنجر إنجلهايم، بريستول-مايرز سكويب، فايزر، بوسطن ساينتيفيك، بايوترونيك، داييتشي سانكيو، أبيوميد، باير، نوفارتس وزول. أتعاب لمهام المجلس الاستشاري من أداجيو ميديكال، بويرنجر إنجلهايم، بريستول-مايرز سكويب، فايزر، باير. يذكر أنه شارك في تجارب سريرية مع داييتشي سانكيو، بويرنجر إنجلهايم، بوسطن ساينتيفيك. يذكر أنه حصل على تمويل بحثي من بوسطن ساينتيفيك، BMS/فايزر، أبيوميد (جميعها تجارب بدأها الباحثون). C.L.-G. تلقى أتعاب من أبوت وبايوسينس ويبسير. A. بريتينشتاين تلقى رسوم استشارية من أبوت، باير هيلث كير، بايوسينس ويبسير، بايوترونيك، BMS/فايزر، بوسطن ساينتيفيك، كوك ميديكال، داييتشي سانكيو، سبيكترانيتيكس/فيلبس وميدترونيك. تلقى منح تعليمية من بايوسينس ويبسير، بايوترونيك وأكتليو. تلقى رسوم مقدمي من أبوت، باير هيلث كير، بايوترونيك، كوك
من بوسطن ساينتيفيك. جميع المؤلفين الآخرين قد أعلنوا عدم وجود تضارب في المصالح. لم يكن هناك دعم تمويلي خارجي لهذه الدراسة.
معلومات إضافية
البيانات الموسعة الجدول 1 | خصائص الموقع السريري
| نوع الممارسة | مجموعة المرضى الكاملة من جميع مواقع MANIFEST-17K* 106 موقع
|
المرضى من مواقع MANIFEST-PF الأولية* 24 موقعًا (
|
المرضى من مواقع MANIFEST-17K الموسعة* 82 موقعًا (
|
| الأكاديمي (%) | 61.3 | 62.5 | 61 |
| خاص (%) | 17 | 12.5 | 18.3 |
| هجين (%) | ٢١.٧ | ٢٥ | ٢٠.٧ |
| عدد المشغلين، المتوسط (الحد الأدنى – الحد الأقصى) | 3.9 (1-11) | 5 (2-10) | 3.6 (1-11) |
| سنوات في الممارسة، المتوسط (الحد الأدنى – الحد الأقصى) | 13.6 (3-25) | 12.2 (5-25) | 14 (3-25) |
| عدد عمليات استئصال الرجفان الأذيني السنوية، المتوسط (الحد الأدنى – الحد الأقصى) | 519 (80-2000) | ٨٠١ (٢٠٠-٢٠٠٠) | 436 (80-1200) |
| تاريخ أول حالة PFA، (الأقدم-الأحدث) | 5/2022 (3/2021-3/2023) | 6/2021 (3/2021-12/2021) | 8/2022 (11/2021-3/2023) |
| عدد حالات PFA المنفذة، المتوسط (الحد الأدنى – الحد الأقصى) | 166 (17-1277) | 328 (54-1277) | ١١٩ (١٧-٤٧٢) |
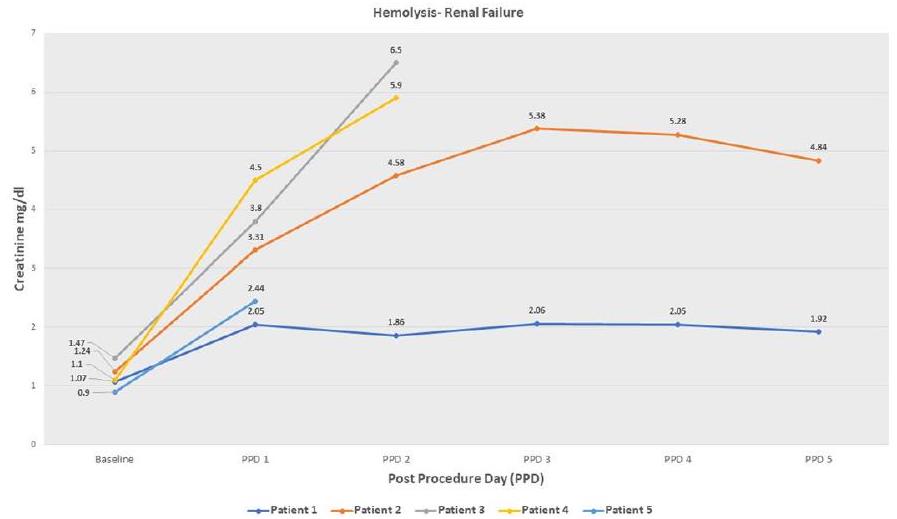
البيانات الموسعة الجدول 2 | الفشل الكلوي الحاد المرتبط بتحلل الدم: تفاصيل المريض
| الكرياتينين الأساسي | ملخص السرد | |
| المريض رقم 1 | كر
|
المريض هو رجل يبلغ من العمر 59 عامًا لديه تاريخ من الرجفان الأذيني المستمر مع استئصال بالتحريض الإشعاعي السابق الذي خضع لعملية استئصال متكررة. مجموعة الآفات التي تم تنفيذها شملت عزل الأوردة الرئوية، عزل الجدار الخلفي وخط الإسطوانة التاجية. تم تقديم إجمالي 159 تطبيقًا للـ PFA. تم ملاحظة الغثيان، القيء والبيلة الدموية بعد الإجراء. زادت مستويات الكرياتينين إلى
|
| المريض رقم 2 | كر
|
المريض هو رجل يبلغ من العمر 73 عامًا لديه تاريخ من الرجفان الأذيني المستمر واستئصال سابق وقد خضع لاستئصال متكرر. مجموعة الآفات التي تم تنفيذها شملت عزل الأوردة الرئوية، عزل الجدار الخلفي، خط الإسطوانة التاجية وخط الإسطوانة التاجية. تم تقديم إجمالي 159 تطبيقًا للـ PFA. أبلغ عن غثيان وتم ملاحظة وجود دم في البول في اليوم الأول بعد العملية. زادت مستويات الكرياتينين إلى
|
| المريض رقم 3 | كر
|
المريضة هي أنثى تبلغ من العمر 79 عامًا تعاني من خلل كلوي معروف (بروتينوريا وخلية دم حمراء في البول)، وفشل قلبي مع الحفاظ على الكسر القذفي، وAF مستمر وقد خضعت لعملية استئصال. تم تقديم إجمالي 158 تطبيقًا لـ PFA (لم يتم تفصيل مجموعات الآفات). لوحظ أنها تعاني من دم في البول وقلة البول في نفس يوم الإجراء. زادت مستويات الكرياتينين إلى
|
| المريض رقم 4 | كر
|
المريض هو رجل يبلغ من العمر 65 عامًا لديه تاريخ من ارتفاع ضغط الدم، داء السكري، مرض الشرايين المحيطية، تليف الكبد، والرجفان الأذيني المستمر الذي خضع لعملية استئصال. تم إجراء مجموعة من الإصابات شملت عزل الأوردة الرئوية، عزل الجدار الخلفي، وخط الإسطوانة التاجية. تم تقديم ما مجموعه 96 تطبيقًا للـ PFA. لوحظ أنه يعاني من بيلة دموية وانقطاع البول في يوم الإجراء. زادت مستويات الكرياتينين إلى 4.5.
|
| المريض رقم 5 | كر
|
المريضة هي أنثى تبلغ من العمر 69 عامًا ولديها تاريخ من اعتلال عضلة القلب الناتج عن تسارع ضربات القلب (EF 35-50%)، وأمراض الكبد، والرجفان الأذيني المستمر الذي خضعت لعملية استئصال له. مجموعة الآفات التي تم تنفيذها شملت عزل الأوردة الرئوية، وعزل الجدار الخلفي، وخط الإسطوانة التاجية. تم تقديم إجمالي 144 تطبيقًا للـ PFA. لوحظ أنها تعاني من بيلة دموية وانقطاع البول في يوم الإجراء. زادت مستويات الكرياتينين إلى
|
البيانات الموسعة الجدول 3 | تحليل السبب الجذري لحدوث السكتات الدماغية
| تحليل السبب الجذري – السكتة الدماغية N = 16 | |
| لا سبب قاطع | ٧ |
| تبديل القسطرة/إدارة الغلاف | ٤ |
| ACT < 300 | ٢ |
| انقطاع مضادات التخثر | 2 |
| ارتفاع ضغط الدم غير المنضبط | 1 |
البيانات الموسعة الجدول 4 | المضاعفات الوعائية كوظيفة لاستخدام الموجات فوق الصوتية الوعائية الروتينية
| مجموعة كاملة* 106 مواقع (
|
استخدام الموجات فوق الصوتية الروتينية 55 موقعًا
|
استخدام الموجات فوق الصوتية غير الروتينية في 48 موقعًا
|
|
| خصائص المرضى الأساسية | |||
| العمر (سنوات)، المتوسط (الحد الأدنى – الحد الأقصى) | 64.1 (11-96) | 64.5 (11-96) | 63.4 (20-96) |
| الإناث (%) | ٣٤.٦ | ٣٤.١ | ٣٥.٤ |
| إجمالي المضاعفات الوعائية | 441 (2.50) | 246 (2.45) | 195 (2.72) |
| ورم دموي | ٣٢٤ (١.٨٤) | 193 (1.92) | 131 (1.83) |
| تمزق كاذب | ٥٨ (٠.٣٣) | ٢٨ (٠.٢٨) | 30 (0.42) |
| ناسور الشريان الوريدي | ٤٦ (٠.٢٦) | 19 (0.19) | 27 (0.38) |
| آخر | 13 (0.07) | 6 (0.06) | 7 (0.10) |
| كبير (يتطلب تدخل) | 53 (0.30) | 17 (0.17) * | ٣٦ (٠.٥٠) * |
| طفيف (لا تدخل) | 388 (2.20) | 229 (2.28) | ١٥٩ (٢.٢٢) |
| خصائص الموقع السريري | |||
| نوع الممارسة | |||
| الأكاديمي (%) | ٦١.٤ | 70.9 | ٥٢.١ |
| خاص (%) | 17.8 | ٥.٥ | ٢٩.٢ |
| الهجين (%) | 20.8 | ٢٣.٦ | 18.8 |
| عدد المشغلين، المتوسط (الحد الأدنى – الحد الأقصى) | 3.8 (1-11) | 4 (1-11) | 3.5 (1-9) |
| سنوات في الممارسة، المتوسط (الحد الأدنى – الحد الأقصى) | 13.5 (3-25) | 12.7 (3-25) | 14.6 (5.2-25) |
| عدد عمليات استئصال الرجفان الأذيني السنوية، المتوسط (الحد الأدنى – الحد الأقصى) | 528 (80-2000) | 546 (80-1400) | 516 (100-2000) |
| عدد حالات PFA المنفذة، المتوسط (الحد الأدنى – الحد الأقصى) | 167 (17-1277) | 182 (17-707) | 151 (18-1277) |
| *دلالة إحصائية (قيمة p
|
|||
البيانات الموسعة الجدول 5 | تفاصيل وفيات المرضى
| توقيت الوفاة بعد الاستئصال | سبب الوفاة | ملخص السرد | |
| المريض رقم 1 | 9 أيام | وفاة مفاجئة غير مفسرة | إجراء استئصال غير ملحوظ، ولكن تلاه وفاة غير مفسرة بعد 9 أيام من الإجراء. لم تكشف التشريح عن أي سبب محدد للوفاة. |
| المريض رقم 2 | أسبوع واحد | انصباب القلب | رجل يبلغ من العمر 75 عامًا يعاني من استئصال معقد بتمزق وتجمع دموي حول القلب. كانت عملية سحب السائل من التامور غير ناجحة، مما استدعى إجراء عملية جراحية طارئة لفتح الصدر. ومع ذلك، تعرض المريض لتلف دماغي لا يمكن عكسه وتوفي بعد أسبوع. |
| المريض رقم 3 | 8 ساعات | فشل القلب غير المتعوض | رجل يبلغ من العمر 84 عامًا يعاني من اعتلال عضلة القلب الناتج عن تسارع ضربات القلب وتم قبوله قبل أسبوع من عملية الاستئصال بسبب فشل القلب المتعذر التعويض. بعد فشل محاولتين لتصحيح نظم القلب، خضع المريض لعملية استئصال الأذين الرئوي وعزل وريد الرئة وخط الإسطوانة التاجية. كانت العملية غير ملحوظة – فقط انخفاض مؤقت في ضغط الدم أثناء الإجراء. ولكن، حدث صدمة قلبية بعد ساعتين من الإجراء مما استدعى دعم الدورة الدموية الميكانيكية. لم يكن هناك انصباب في التامور، أو نزيف آخر، أو متلازمة الشريان التاجي الحادة. تم إيقاف دعم الدورة الدموية الميكانيكية في النهاية، وتوفي المريض. كانت نتائج التشريح غير ملحوظة، وتم نسب الوفاة إلى فشل حاد في البطين الأيسر. |
| المريض رقم 4 | 3 أيام | توقف القلب (في سياق مرض الشريان التاجي الحاد) | رجل يبلغ من العمر 62 عامًا يعاني من مرض الكلى المزمن ومرض الشريان التاجي متعدد الأوعية (مع وجود دعامة سابقة) ووظيفة بطينية يسارية محفوظة. كانت نتائج الفحص البدني غير ملحوظة، وتم إخراج المريض إلى المنزل. بعد يومين، تطور لدى المريض ألم في الصدر ودوار في المنزل وسقط. تم تنفيذ إنعاش قلبي رئوي متقدم من قبل الطاقم الطبي الطارئ خلال 6 دقائق من ظهور الأعراض – كانت النبضات الأولية هي عدم النشاط الكهربائي، ولكن عاد الدوران التلقائي. عند وصوله إلى المستشفى، حدثت رجفان بطيني، مما استدعى اتخاذ تدابير الإنعاش القلبي الرئوي المتقدم. تم بدء استخدام الأكسجة الغشائية خارج الجسم. أظهرت تصوير الأوعية التاجية عدم وجود آفات حادة. أظهر تصوير الأوعية الرئوية عدم وجود انسداد رئوي، ولم يكن هناك انصباب حول القلب حسب تخطيط صدى القلب. استمر في عدم الاستقرار الديناميكي الدموي، واستعادة عصبية ضعيفة، وتوفي بعد 24 ساعة. |
| المريض رقم 5 | 30 يومًا | نزيف المخيخ | رجل يبلغ من العمر 60 عامًا خضع لإجراء استئصال غير معقد، لكنه أصيب بصداع بعد 8 أيام من الإجراء وسرعان ما فقد الوعي. توفي بعد 30 يومًا من الاستئصال. أظهرت التشريح وجود نزيف هائل في المخيخ. |
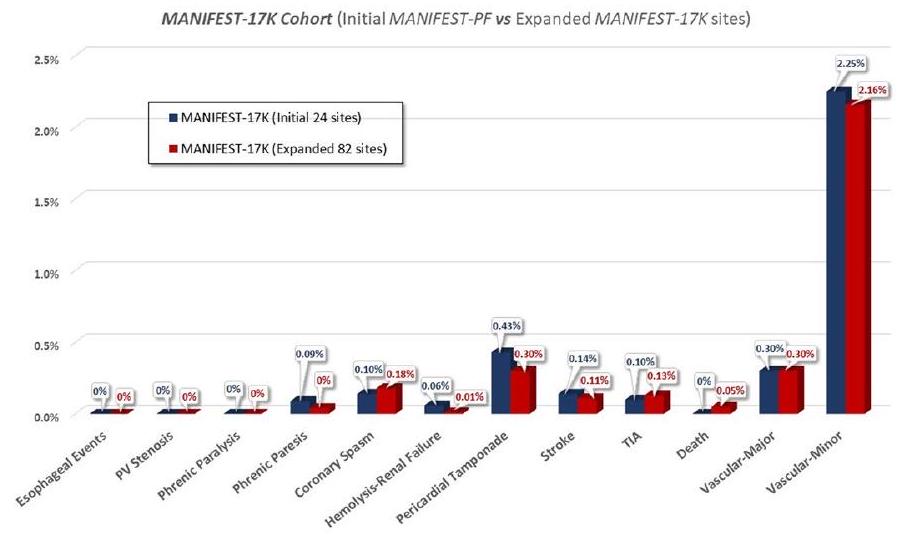
البيانات الموسعة الجدول 6 | المضاعفات في كلا المجموعتين – مواقع MANIFEST-PF الأولية مقابل مواقع MANIFEST-17K الموسعة
| مجموعة المرضى الكاملة من جميع مواقع MANIFEST-17K * 106 مواقع
|
المرضى من مواقع MANIFEST-PF الأولية* 24 موقعًا (
|
المرضى من مواقع MANIFEST-17K الموسعة * 82 موقعًا (
|
||||
| الأحداث السلبية الكبرى | 173 (0.98%) | 82 (1.04%) | 91 (0.93%) | |||
| الموت | 5 (0.03)
|
0 (0) | 5 (0.05)
|
|||
| سكتة دماغية | 22 (0.12) | 11 (0.14) | 11 (0.11) | |||
| ناسور المريء أو خلل الحركة | 0 (0) | 0 (0) | 0 (0) | |||
| تضيق الوريد الرئوي | 0 (0) | 0 (0) | 0 (0) | |||
| إصابة العصب الحجابي (مستمرة) |
|
|
|
|||
| انصباب التامور |
|
٣٤ (٠.٤٣) | ٢٩ (٠.٣٠)
|
|||
| التدخل عبر الجلد | ٥٦ (٠.٣٢) | 30 (0.38) | ٢٦ (٠.٢٧) | |||
| التدخل الجراحي | 7 (0.04)
|
4 (0.05) | 3 (0.03)
|
|||
| مضاعفات وعائية (مع تدخل) | 53 (0.30) | ٢٤ (٠.٣٠) | ٢٩ (٠.٣٠) | |||
| تشنج الشريان التاجي | 25 (0.14) | 8 (0.10) | 17 (0.17) | |||
| احتشاء عضلة القلب | 0 (0.0) | 0 (0) | 0 (0) | |||
| تحلل الدم – فشل كلوي (إقامة في المستشفى) | 5 (0.03) | 5 (0.06) | 0 (0) | |||
| آخر (جلطة دموية) | 1 (0.006) | 0 (0) | 1 (0.01) | |||
| أحداث سلبية طفيفة | 567 (3.21%) | 264 (3.35%) | 303 (3.10%) | |||
| نوبة إقفارية عابرة | 21 (0.12) | 8 (0.10) | 13 (0.13) | |||
| إصابة العصب الحجابي (عابرة) | 11 (0.06)
|
7 (0.09)
|
4 (0.04)
|
|||
| انصباب التامور (بدون تدخل) | ٥٩ (٠.٣٣) | ٢٤ (٠.٣٠) | ٣٥ (٠.٣٦) | |||
| التهاب التامور | 30 (0.17) | 12 (0.15) | 18 (0.18) | |||
| المضاعفات الوعائية (بدون تدخل) | 388 (2.20) | 177 (2.25) | 211 (2.16) | |||
| تحلل الدم – فشل كلوي (بدون دخول المستشفى) | 1 (0.006) | 0 (0) | 1 (0.01) | |||
| مضاعفات أخرى | 57 (0.32) | ٣٦ (٠.٤٦) | 21 (0.21) | |||
|
||||||
محفظة الطبيعة
آخر تحديث من المؤلف(ين): 15/5/2024
ملخص التقرير
الإحصائيات
تم التأكيد
لاختبار الفرضية الصفرية، فإن إحصائية الاختبار (على سبيل المثال،
تحتوي مجموعتنا على الإنترنت حول الإحصائيات لعلماء الأحياء على مقالات تتناول العديد من النقاط المذكورة أعلاه.
البرمجيات والشيفرة

بيانات
معلومات السياسة حول توفر البيانات
- رموز الانضمام، معرفات فريدة، أو روابط ويب لمجموعات البيانات المتاحة للجمهور
- وصف لأي قيود على توفر البيانات
- بالنسبة لمجموعات البيانات السريرية أو بيانات الطرف الثالث، يرجى التأكد من أن البيان يتماشى مع سياستنا
البحث الذي يتضمن مشاركين بشريين، بياناتهم، أو مواد بيولوجية
| التقارير عن الجنس والنوع الاجتماعي | تم الإبلاغ عن بيانات الجنس والنوع بشكل ذاتي وبشكل استباقي وفقًا لإرشادات مجلة Nature. |
| التقارير عن العرق أو الإثنية أو غيرها من التجمعات الاجتماعية ذات الصلة | لم يتم جمع بيانات عن العرق أو الإثنية كجزء من هذه الدراسة |
| خصائص السكان | كان هناك إجمالي 17,642 مريضًا، بمتوسط عمر 64 عامًا (يتراوح بين 11-96) و34.7% إناث |
| التوظيف | كانت هذه دراسة رصدية لبيانات مستوى المركز. تم إرسال وثيقة دعوة إلى كل مركز مشارك عبر البريد الإلكتروني. |
| رقابة الأخلاقيات | تمت الموافقة على هذه الدراسة من قبل اللجنة الأخلاقية في مستشفى هومولكا |
التقارير المتخصصة في المجال
علوم الحياة
لنسخة مرجعية من الوثيقة بجميع الأقسام، انظرnature.com/documents/nr-reporting-summary-flat.pdf
تصميم دراسة العلوم الحياتية
| حجم العينة | كانت هذه دراسة رصدية استعادية ولم يتم إجراء حساب حجم العينة. |
| استثناءات البيانات | تم استخدام جميع البيانات المبلغ عنها من قبل المراكز المشاركة |
| استنساخ | لم يكن هناك تكرار للبيانات حيث كانت هذه دراسة جديدة على مجموعة مرضى فريدة لم يتم تقييمها من قبل. |
| التوزيع العشوائي | نظرًا للطبيعة الاستعادية للدراسة، لم يتم إجراء عشوائية مستقبلية. |
| عمى | نظرًا للطبيعة الاستعادية للدراسة التي تدرس نفس التدخل وعدم وجود دواء وهمي، لم يُعتبر التعمية ضرورية للدراسة. |
التقارير عن مواد وأنظمة وطرق محددة

النباتات
| مخزونات البذور | تقرير عن مصدر جميع مخزونات البذور أو المواد النباتية الأخرى المستخدمة. إذا كان ذلك مناسبًا، يرجى ذكر مركز مخزون البذور ورقم الفهرس. إذا تم جمع عينات نباتية من الحقل، يرجى وصف موقع الجمع، التاريخ وإجراءات أخذ العينات. | ||
| أنماط جينية نباتية جديدة | وصف الطرق التي تم من خلالها إنتاج جميع الأنماط الجينية النباتية الجديدة. يشمل ذلك تلك التي تم إنشاؤها من خلال الأساليب الجينية المتحولة، وتحرير الجينات، والطفرات المعتمدة على المواد الكيميائية/الإشعاع، والتهجين. بالنسبة لخطوط الجينات المتحولة، وصف طريقة التحويل، وعدد الخطوط المستقلة التي تم تحليلها، والجيل الذي أجريت عليه التجارب. بالنسبة لخطوط تحرير الجينات، وصف المحرر المستخدم، والتسلسل الداخلي المستهدف للتحرير، وتسلسل RNA الدليل المستهدف (إذا كان ذلك مناسبًا) وكيفية عمل المحرر. | ||
| المصادقة |
|
- البريد الإلكتروني: vivek.reddy@mountsinai.org
- إيمانويل إكانيم ©
بيتر نوزيل توبيا ريشلين جوزيف كاوتزنر بيبين فان دير فورت بيير جاي جيان-باتيستا كيركيا آلان بولافا يوري بلاو تومáš سكالá مارتن فيالا ماتياس دويتشيفر غابور سيبلاكي بوريس شميت غريغوار ماسولي © كارس نيفن © أوليفييه توماس يوهان فيجن إستيل غاندجباخش دانيال شير أرني يوهانسون ديفيد كين سيرج بوفيدا فيليب موري إغناسيو غارسيا-بولاو أنتي أنيتش بيتر ستين هانسن فرانك راكزا أنطوان ليبيليير إيف غيومار ديراج غوبتا جورن فان أوبستال باسكال ديفاي كريستيان ستيشرلينغ فيليب سومر بافل كوتشيرا خواكين أوسكار فاريبورز تابريزي أنطوان رو مايكل غرامليش ستيفانو بيانشي © بيدرو أدراغاو فرانشيسكو سوليميني كلوديو توندو أنتونيو ديلو روسو يورغن شرايك أرمين لوك عبيدة رنا © جيريت فرومير فريديريك أنسلم إنغو كرايس رافائيل روسو أندرياس ميتزنر لازلو جيلر صموئيل هـ. بالدينجر أنجل فيريرو ستيفان ويليمز أندرياس غوت غريغ ميلور شيبوا ماثيو ،
DOI: https://doi.org/10.1038/s41591-024-03114-3
PMID: https://pubmed.ncbi.nlm.nih.gov/38977913
Publication Date: 2024-07-01
Safety of pulsed field ablation in more than 17,000 patients with atrial fibrillation in the MANIFEST-17K study
Accepted: 4 June 2024
Published online: 8 July 2024
(D) Check for updates
Abstract
A list of authors and their affiliations appears at the end of the paper
Pulsed field ablation (PFA) is an emerging technology for the treatment of atrial fibrillation (AF), for which pre-clinical and early-stage clinical data are suggestive of some degree of preferentiality to myocardial tissue ablation without damage to adjacent structures. Here in the MANIFEST-17K study we assessed the safety of PFA by studying the post-approval use of this treatment modality. Of the 116 centers performing post-approval PFA with a pentaspline catheter, data were received from 106 centers (91.4% participation) regarding 17,642 patients undergoing PFA (mean age 64,
rates during thermal ablation have improved over time, there remain residual safety considerations including the risk for pulmonary vein (PV) stenosis, stroke, phrenic nerve palsy and the deadliest complication, atrio-esophageal fistula, which even today has a mortality of ~50% (refs. 8-10).
Results
Baseline characteristics

AEs overview
PFA energy-specific AEs
| Full MANIFEST-17K cohort (
|
|
| Demographic | |
| Age (years), mean (minimum-maximum) | 64 (11-96) |
| Female (%) | 34.7 |
| Indication for ablation | |
| Paroxysmal atrial fibrillation (%) | 57.8 |
| Persistent atrial fibrillation (%) | 35.2 |
| Long-standing persistent atrial fibrillation (%) | 5.6 |
| Atrial flutter/atrial tachycardia (%) | 1.4 |
| Sedation | |
| General anesthesia (%) | 46.9 |
| Deep sedation/no intubation (%) | 53.1 |
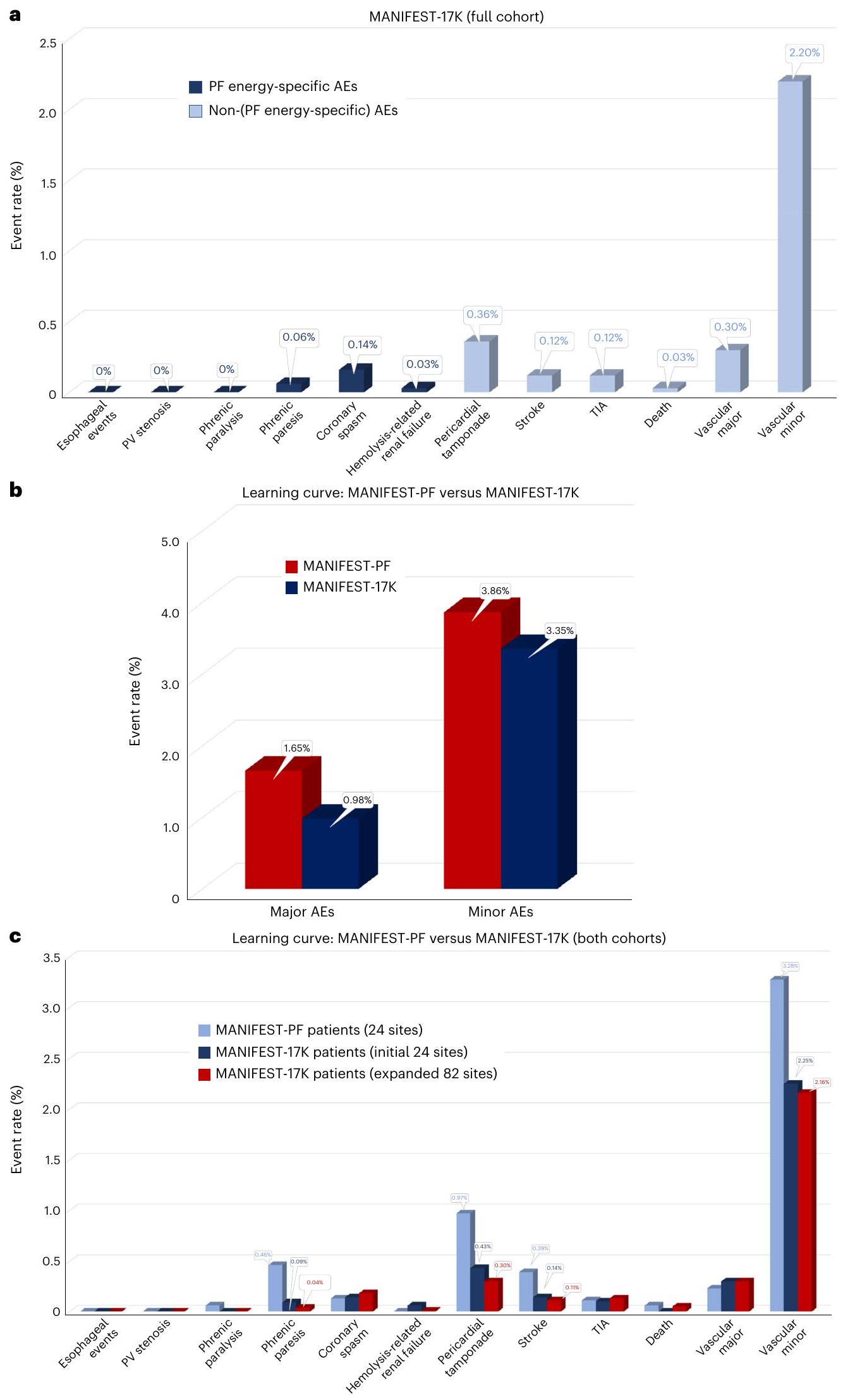
Non-PFA energy-specific AEs
| Full patient cohort from all 106 MANIFEST-17K sites
|
|
| Major AEs | 173 (0.98%) |
| Death
|
5 (0.03%) |
| Stroke | 22 (0.12%) |
| Esophageal fistula or dysmotility | 0 (0%) |
| Pulmonary vein stenosis | 0 (0%) |
| Phrenic nerve injury (persistent)
|
0 (0%) |
| Pericardial tamponade
|
63 (0.36%) |
| Percutaneous intervention | 56 (0.32%) |
| Surgical intervention
|
7 (0.04%) |
| Vascular complication (with intervention) | 53 (0.30%) |
| Coronary artery spasm | 25 (0.14%) |
| Myocardial infarction | 0 (0.0%) |
| Hemolysis renal failure (hospitalization) | 5 (0.03%) |
| Other (thrombosis) | 1 (0.006%) |
| Minor AEs | 567 (3.21%) |
| Transient ischemic attack | 21 (0.12%) |
| Phrenic nerve injury (transient)
|
11 (0.06%) |
| Pericardial effusion (no intervention) | 59 (0.33%) |
| Pericarditis | 30 (0.17%) |
| Vascular complications (no intervention) | 388 (2.20%) |
| Hemolysis renal failure (no hospitalization) | 1 (0.006%) |
| Other complications | 57 (0.32%) |

red bars) and observed in the currently studied MANIFEST-17K cohort (
| Coronary spasm (
|
|
| Type of spasm: | |
| Proximity-related spasm
|
22 (88%) |
| Generalized spasm
|
3 (12%) |
| EKG changes | 23 (92%) |
| Hypotension | 5 (20%) |
| Clinical sequelae | 4 (16%) |
| Chest pain | 2 (8%) |
| Ventricular fibrillation | 2 (8%) |
| Intravenous nitroglycerin administered | 21 (84%) |
including the number of PFA cases per site (182 (range 17-707) versus
Learning curve
| Other complications N=57 (0.32%) | |
| Pacemaker implant | 12 (0.07%) |
| Air emboli | 10 (0.06%) |
| Lead malfunction/dislocation | 3 (0.02%) |
| Atrioventricular block | 3 (0.02%) |
| Migraine | 3 (0.02%) |
| Hemoptysis | 3 (0.02%) |
| Anesthesia-related hypotension | 2 (0.01%) |
| Heart failure | 2 (0.01%) |
| Pneumonia | 2 (0.01%) |
| Gastritis | 2 (0.01%) |
| Miscellaneous | 15 (0.09%) |
Discussion
injury. This is consistent with prior pre-clinical, observational and randomized clinical studies.
to a coronary artery during mitral isthmus or CTI ablation, and (2) the remaining (
of PFA applications is necessary, one should consider applying simple mitigation strategies such as saline hydration.
esophageal complications, and with a low rate of major complications. Hemolysis-related renal failure requiring hemodialysis did occur, albeit rarely. Finally, the low incidence of coronary arterial spasm belies its potentially serious implications and warrants further study and guidance.
Online content
References
- Mark, D. B. et al. Effect of catheter ablation vs medical therapy on quality of life among patients with atrial fibrillation. J. Am. Med. Assoc. 321, 1275-1285 (2019).
- Turagam, M. K. et al. Catheter ablation of atrial fibrillation in patients with heart failure. Ann. Intern. Med. 170, 41-50 (2018).
- Marrouche, N. F. et al. Catheter ablation for atrial fibrillation with heart failure. N. Engl. J. Med. 378, 417-427 (2018).
- Packer, D. L. et al. Ablation versus drug therapy for atrial fibrillation in heart failure: results from the CABANA trial. Circulation 143, 1377-1390 (2021).
- Kuck, K.-H. et al. Cryoballoon or radiofrequency ablation for symptomatic paroxysmal atrial fibrillation: reintervention, rehospitalization, and quality-of-life outcomes in the FIRE AND ICE trial. Eur. Heart J. 37, 2858-2865 (2016).
- Turagam, M. K. et al. Assessment of catheter ablation or antiarrhythmic drugs for first-line therapy of atrial fibrillation. JAMA Cardiol. 6, 697-705 (2021).
- Kirchhof, P. et al. Early rhythm-control therapy in patients with atrial fibrillation. N. Engl. J. Med. 383, 1305-1316 (2020).
- Tilz, R. R. et al. A worldwide survey on incidence, management, and prognosis of oesophageal fistula formation following atrial fibrillation catheter ablation: the POTTER-AF study. Eur. Heart J. 44, 2458-2469 (2023).
- Calkins, H. et al. HRS/EHRA/ECAS expert consensus statement on catheter and surgical ablation of atrial fibrillation. Europace 9, 335-379 (2007).
- Deshmukh, A. et al. In-hospital complications associated with catheter ablation of atrial fibrillation in the United States between 2000 and 2010. Circulation 128, 2104-2112 (2013).
- Kotnik, T., Rems, L., Tarek, M. & Miklavčič, D. Membrane electroporation and electropermeabilization: mechanisms and models. Annu. Rev. Biophys. 48, 63-91 (2019).
- Reddy, V. Y. et al. Ablation of atrial fibrillation with pulsed electric fields. JACC Clin. Electrophysiol. 4, 987-995 (2018).
- Neven, K. et al. Acute and long-term effects of full-power electroporation ablation directly on the porcine esophagus. Circ. Arrhythm. Electrophysiol. 10, e004672 (2017).
- Koruth, J. et al. Preclinical evaluation of pulsed field ablation: electrophysiological and histological assessment of thoracic vein isolation. Circ. Arrhythm. Electrophysiol. 12, e007781 (2019).
- Koruth, J. S. et al. Pulsed field ablation versus radiofrequency ablation: esophageal injury in a novel porcine model. Circ. Arrhythm. Electrophysiol. 13, e008303 (2020).
- Cochet, H. et al. Pulsed field ablation selectively spares the oesophagus during pulmonary vein isolation for atrial fibrillation. Europace 23, 1391-1399 (2021).
- Reddy, V. Y. et al. Pulsed field ablation for pulmonary vein isolation in atrial fibrillation. J. Am. Coll. Cardiol. 74, 315-326 (2019).
- Reddy, V. Y. et al. Pulsed field ablation of paroxysmal atrial fibrillation: 1-year outcomes of IMPULSE, PEFCAT, and PEFCAT II. JACC Clin. Electrophysiol. 7, 614-627 (2021).
- Reddy, V. Y. et al. Pulsed field ablation in patients with persistent atrial fibrillation. J. Am. Coll. Cardiol. 76, 1068-1080 (2020).
- Ekanem, E. et al. Multi-national survey on the methods, efficacy, and safety on the post-approval clinical use of pulsed field ablation (MANIFEST-PF). Europace 24, 1256-1266 (2022).
- Turagam, M. K. et al. Safety and effectiveness of pulsed field ablation to treat atrial fibrillation: one-year outcomes from the MANIFEST-PF registry. Circulation 148, 35-46 (2023).
- Schmidt, B. et al. European real-world outcomes with pulsed field ablation in patients with symptomatic atrial fibrillation: lessons from the multi-centre EU-PORIA registry. Europace 25, euad185 (2023).
- Reddy, V. Y. et al. Pulsed field or conventional thermal ablation for paroxysmal atrial fibrillation. N. Engl. J. Med. 389, 1660-1671 (2023).
- Kawasaki, R., Gauri, A., Elmouchi, D., Duggal, M. & Bhan, A. Atrioesophageal fistula complicating cryoballoon pulmonary vein isolation for paroxysmal atrial fibrillation. J. Cardiovasc. Electrophysiol. 25, 787-792 (2014).
- Metzner, A. et al. Increased incidence of esophageal thermal lesions using the second-generation
cryoballoon. Circ. Arrhythm. Electrophysiol. 6, 769-775 (2013). - Straube, F. et al. Comparison of the first and second cryoballoon: high-volume single-center safety and efficacy analysis. Circ. Arrhythm. Electrophysiol. 7, 293-299 (2014).
- Bakir, N. H. et al. Concomitant surgical ablation for atrial fibrillation is associated with increased risk of acute kidney injury but improved late survival. J. Thorac. Cardiovasc. Surg. 164, 1847-1857.e3 (2022).
- van Driel, V. J. H. M. et al. Low vulnerability of the right phrenic nerve to electroporation ablation. Heart Rhythm 12, 1838-1844 (2015).
- Yavin, H. et al. Pulsed field ablation using a lattice electrode for focal energy delivery: biophysical characterization, lesion durability, and safety evaluation. Circ. Arrhythm. Electrophysiol. 13, e008580 (2020).
- Kuroki, K. et al. Ostial dimensional changes after pulmonary vein isolation: pulsed field ablation vs radiofrequency ablation. Heart Rhythm 17, 1528-1535 (2020).
- Meissner, A. et al. Impact of irrigated energy application on the right coronary artery hemodynamics: FFR measurement in patients who underwent ablation of common type atrial flutter. J. Interv. Card. Electrophysiol. 21, 35-42 (2008).
- Wong, K. C. K. et al. High incidence of acute sub-clinical circumflex artery ‘injury’ following mitral isthmus ablation. Eur. Heart J. 32, 1881-1890 (2011).
- Reddy, V. Y. et al. Coronary arterial spasm during pulsed field ablation to treat atrial fibrillation. Circulation 146, 1808-1819 (2022).
- Zhang, C. et al. Coronary artery spasm during pulsed field vs radiofrequency catheter ablation of the mitral isthmus. JAMA Cardiol. https://doi.org/10.1001/jamacardio.2023.4405 (2023).
- Gunawardene, M. A. et al. Coronary spasm during pulsed field ablation of the mitral isthmus line. JACC Clin. Electrophysiol. 7, 1618-1620 (2021).
- Della Rocca, D. G. et al. Transient inferior ST-segment elevation and ventricular fibrillation after cavotricuspid isthmus pulsed-field ablation. JACC Clin. Electrophysiol. 9, 704-706 (2023).
- Nakamura, T. et al. Incidence and characteristics of coronary artery spasms related to atrial fibrillation ablation procedures -large-scale multicenter analysis. Circ. J. 85, 264-271 (2021).
- Kinosita, K. Jr. & Tsong, T. Y. Voltage-induced pore formation and hemolysis of human erythrocytes. Biochim. Biophys. Acta 471, 227-242 (1977).
- Moroz, V. V., Bogushevich, M. S., Chernysh, A. M., Kozlova, E. K. & Sharakshane, A. S. Effect of defibrillation pulses of different shapes on biomembranes: experimental study. Bull. Exp. Biol. Med. 137, 120-123 (2004).
- Davong, B. et al. Pulsed-field ablation on mitral isthmus in persistent atrial fibrillation: preliminary data on efficacy and safety. JACC Clin. Electrophysiol. 9, 1070-1081 (2023).
- Cheng, E. P. et al. Risk of mortality following catheter ablation of atrial fibrillation. J. Am. Coll. Cardiol. 74, 2254-2264 (2019).
- Kim, I.-C. et al. Incidence and predictors of silent embolic cerebral infarction following diagnostic coronary angiography. Int. J. Cardiol. 148, 179-182 (2011).
- Kahlert, P. et al. Silent and apparent cerebral ischemia after percutaneous transfemoral aortic valve implantation. Circulation 121, 870-878 (2010).
- Verma, A. et al. Pulsed field ablation for the treatment of atrial fibrillation: Pulsed af pivotal trial. Circulation 147, 1422-1432 (2023).
- Haeusler, K. G. et al. MRI-detected brain lesions and cognitive function in patients with atrial fibrillation undergoing left atrial catheter ablation in the randomized AXAFA-AFNET 5 trial. Circulation 145, 906-915 (2022).
© The Author(s) 2024
e-mail: vivek.reddy@mountsinai.org
Methods
Survey overview
The PFA procedure
Study data specifics
phrenic nerve injury (transient), pericardial effusion (no intervention), vascular complications (no intervention), hemolysis not requiring hospitalization and others.
Data analysis
Reporting summary
Data availability
Author contributions
Competing interests
J.K. reports personal fees from Abbott, Biosense Webster, Biotronik, Boehringer Ingelheim, GE Healthcare, Medtronic, Pfizer, ProMed CS, and Viatris for lectures, advisory boards, and consultancy. P.J. has received grants by BSC and ANR grant IHU LIRYC ANR-10-IAHU-04. G.-B.C. received compensation for teaching purposes and proctoring from Medtronic, Abbott, Biotronik, Boston Scientific and Acutus Medical. A. Bulava received consultant and/or grant support from Abbott, Biotronik and Boston Scientific. Y.B. received research grants from Medtronic and Atricure and consulting fees from Abbott, Biosense Webster and Boston Scientific. G.S. received personal fees from Abbott, Bayer, Boston Scientific, Biosense Webster Inc. and LumaVision outside the submitted work. G.J. received personal fees from Boston Scientific. B.S. received consulting fees from Boston Scientific, Biosense Webster and Medtronic. J.C. has received funding from Boston Scientific, Medtronic and Biosense Webster (Education). K.N. has received funding from Biosense Webster, Boston Scientific and Field Medical. A.F. has received funding from Boston Scientific. J.V. has received research grants from Medtronic, Boston Scientific, Abbott, Biotronik, Daiichi Sankyo, BMS and Pfizer. He received honoraria from Abbott and Daiichi Sankyo, and support for meeting attendance from Biosense and Boston Scientific. He serves on the advisory board for Boston Scientific and is the Chairman of the Belgian Heart Rhythm Association. E.G. reports consulting fees from Medtronic, Boston, Microport, Abbott and Biotronik. P.K. has received research grants from Medtronic, Boston Scientific, Abbott, Biotronik, Daiichi Sankyo, BMS and Pfizer. He received honoraria from Abbott and Daiichi Sankyo, and support for meeting attendance from Biosense and Boston Scientific. He serves on the advisory board for Boston Scientific and is the Chairman of the Belgian Heart Rhythm Association. D. Scherr reports speaker and consulting fees from Boston Scientific. M.M. reports receiving speaker fees from Bayer, Biosense Webster, Biotronik, Amomed, AOP Orphan, Boston Scientific, Daiichi Sankyo and BMS/Pfizer and research grants from Biosense Webster and Abbott. J.H. reports receiving speaker fees and grant support from Biosense Webster and Medtronic. S.B. serves as a consultant for Medtronic, Boston Scientific, Microport and Zoll. I.G.-B. received speaker honoraria from Boston Scientific and proctorship fees from Abbott. A.A. has served as a consultant to Boston Scientific Inc., Farapulse Inc., Galaxy Medical Inc., Biosense and Webster and Arga Medtech, and has contracted research with Boston Scientific Inc., Farapulse Inc., Galaxy Medical Inc., Biosense and Webster, Arga Medtech,Future Cardia Inc. and Atacor Medical Inc. Z.J. served as consultant to Boston Scientific Inc and has contracted research with Atacor Medical Inc. D.G. has received research grants from Boston Scientific. P.D. has received research grants and honoraria from Boston Scientific. C.S. is a member of Medtronic Advisory Board Europe and Boston Scientitic Advisory Board Europe. He has received educational grants from Biosense Webster and Biotronik and a research grant from the European Union’s FP7 program and Biosense Webster. He reports lecture and consulting fees from Abbott, Medtronic, Biosense Webster, Boston Scientific, Microport and Biotronik, all outside the submitted work. P.S. is a member of the advisory board for Abbott, Biosense Webster, Boston Scientific and Medtronic. J.O. received speaking honoraria from Boston Scientific, Abbot, Biotronik and Medtronic. M. Gramlich received speaker honoraria and travel grants from Boston Scientific. C.T. served on the advisory board of and has received lecture/tutoring fees from Boston Scientific, Medtronic and Atricure. He has received lecture/tutoring fees from Abbott Medical. A.D.R. received speaker honoraria from Boston Scientific and Abbott. J.S. received speaker’s honoraria and travel grants from Boston Scientific, Biosense Webster, Medtronic, Bayer HealthCare and Bristol-Myers Squibb. A.L. received consulting fees from Boston Scientific, Biosense Webster, Pfizer, Bristol-Myers Squibb and Medtronic. G.F. received lecture honoraria and travel grants from Boston Scientific. F.A. received honoraria and served as a
consultant for Boston Scientific, Medtronic and Microport CRM. A.M. received lecture honoraria and travel fees from Medtronic, Boston Scientific, Biosense Webster, Lifetech, BMS and Bayer. He also served as a consultant for Medtronic, Boston-Scientific and Biosense Webster. L.G. served as a consultant for Abbott, Medtronic, Boston, Biotronik and Johnson and Johnson. S.W. reports receiving grants and personal fees from Abbott, Boston Scientific and Medtronic, and personal fees from Boehringer Ingelheim, Brystol Myers Squibb, Bayer Vital, Accutus, Daiichi and Farapulse Inc. M. Gunawardene reports grants from Farapulse Inc. and Abbott. A. Goette was supported by EU Grant Horizon 2020 MAESTRIA Consortium grant number 965286 and has received speaker fees from Abbott, AstraZeneca, Bayer Health Care, Berlin Chemie, Biotronik, Boehringer Ingelheim, BMS/Pfizer, Boston Scientific, Daiichi Sankyo, Medtronic, Viofor, Novartis and Sanofi. C.M. reports honoraria and speaker’s fees from Boston Scientific, Medtronic, Biosense Webster, Acutus and Adagio. She served as a consultant and on the advisory board for Boston Scientific and Medtronic. She received research grant from Boston Scientific. R.T. reports receiving consulting fees from Boston Scientific, Abbot Medical, Biotronik and speaker’s honoraria from Boston Scientific, Abbot Medical, Biotronik and Biosense Webster. A. George has served as a consultant to Boston Scientific and has received fees for lectures from Boston Scientific. He has also received fees for consultation and/or lecturing from Abbot, AstraZeneca, Bard, Bayer Healthcare, Boehringer Ingelheim, Bristol-Myers Squibb, ELPEN, Galenica, Lilly, Medtronic, Menarini, MSD, Pfizer, Sanofi, Servier, Unifarma and Vianex. S.S. received speaker’s honoraria from Medtronic and Abbott, and participation in clinical trials with Abbott, Ablacon, Boston and Medtronic. R.B. received honoraria from Boston Scientific. T.D. received consulting fees from Farapulse (<2,000 US$), speaker fees with Galaxy Medical (<1,000 US$) and speaker fees with Abbott (<3,000 US$). A. Glowniak received compensation for proctoring and speaking duties from Medtronic and for speaking duties from Abbott and Boston. A.R. served as a consultant for Boston Scientific. H.P. served as a consultant/advisory board for Abbott, Biosense Webster, Boston Scientific and Medtronic. D.D. received modest lecture honoraria, travel grants and/or a fellowship grant from Abbott, Astra Zeneca, Biotronik, Boehringer Ingelheim, Boston Scientific, Bristol-Myers Squibb, CVRx, Medtronic, Microport, Pfizer and Zoll. D. Steven received research grant <50,000 € and speaker fees <10,000 € from Biosense Webster and Boston Scientific. A.S. reports receiving lecture and consulting honoraria from Medtronic, Abbott and Bayer. J.S.S.G.d.J. was a consultant for Medtronic. R.W. reports receiving honoraria for lectures from Adagio medical, Boehringer Ingelheim, Bristol-Myers Squibb, Pfizer, Boston Scientific, Biotronik, Daiichi Sankyo, Abiomed, Bayer, Novartis, Zoll. Honoraria for advisory board activities from Adagio medical, Boehringer Ingelheim, Bristol-Myers Squibb,Pfizer, Bayer. He reports participating in clinical trials with Daiichi Sankyo, Boehringer Ingelheim, Boston Scientific. He reports research funding from boston Scientific, BMS/ Pfizer, Abiomed (all investigator-initiated trials). C.L.-G. received honoraria from Abbott and Biosense Webster. A. Breitenstein received consulting fees from Abbott, Bayer Health Care, Biosense Webster, Biotronik, BMS/Pfizer, Boston Scientific, Cook Medical, Daiichi Sankyo, Spectranetics/Philips and Medtronic. He received educational grants from Biosense Webster, Biotronik and Actelion. He received presenter fees from Abbott, Bayer Health Care, Biotronik, Cook Medical, BMS/Pfizer, Boston Scientific, Daiichi Sankyo, Medtronic and Spectranetics/Philips. J.I. received fees from Boston Scientific and an educational grant from Boston Scientific. D.L. has served as a consultant to Boston Scientific (now divested); and unrelated to this manuscript, he serves as a consultant for Ablacon, ATriAN, Bayer, Biosense Webster, Medtronic and Philips. J.R.-M. has received research funding and speaker/proctorship fees from Boston Scientific. D.R.M. has received speaker honoraria and research grants
from Boston Scientific. All of the remaining authors have declared no conflicts of interest. There was no external funding support for this study.
Additional information


Extended Data Table 1 | Clinical Site Characteristics
| Practice type | Full Patient Cohort from All MANIFEST-17K Sites* 106 Sites (
|
Patients from Initial MANIFEST-PF Sites* 24 Sites (
|
Patients from Expanded MANIFEST-17K Sites* 82 Sites (
|
| Academic (%) | 61.3 | 62.5 | 61 |
| Private (%) | 17 | 12.5 | 18.3 |
| Hybrid (%) | 21.7 | 25 | 20.7 |
| No. of operators, mean (min-max) | 3.9 (1-11) | 5 (2-10) | 3.6 (1-11) |
| Years in practice, mean (min-max) | 13.6 (3-25) | 12.2 (5-25) | 14 (3-25) |
| Annual no. of AF ablations, mean (min-max) | 519 (80-2000) | 801 (200-2000) | 436 (80-1200) |
| Date of first PFA case, (earliest-latest) | 5/2022 (3/2021-3/2023) | 6/2021 (3/2021-12/2021) | 8/2022 (11/2021-3/2023) |
| No. of PFA cases performed, mean (min-max) | 166 (17-1277) | 328 (54-1277) | 119 (17-472) |
Extended Data Table 2 | Hemolysis-Related Acute Renal Failure: Patient Details
| Baseline Creatinine | Narrative Summary | |
| Patient #1 | Cr
|
Patient is a 59-year-old male with history of persistent AF with prior radiofrequency ablation who underwent repeat ablation. The lesion set performed included pulmonary vein isolation, posterior wall isolation and mitral isthmus line. A total of 159 PFA applications were delivered. Nausea, vomiting and hematuria were noted post procedure. Creatinine increased to
|
| Patient #2 | Cr
|
Patient is a 73-year-old male with a history of persistent AF and prior ablation who underwent repeat ablation. The lesion set performed included pulmonary vein isolation, posterior wall isolation, mitral isthmus line and cavotricuspid isthmus line. A total of 159 PFA applications were delivered. He reported nausea and hematuria was noted PPD 1. Creatinine increased to
|
| Patient #3 | Cr
|
Patient is a 79-year-old female with known renal dysfunction (proteinuria and erythrocyturia), heart failure with preserved ejection fraction, persistent AF who underwent ablation. A total of 158 PFA applications were delivered (lesion sets not detailed). She was noted to have hematuria and oliguria on the same day of the procedure. Creatinine increased to
|
| Patient #4 | Cr
|
Patient is a 65-year-old male with history of hypertension, diabetes mellitus, peripheral artery disease, cirrhosis, persistent AF who underwent ablation. The lesion set performed included pulmonary vein isolation, posterior wall isolation, and mitral isthmus line. A total of 96 PFA applications were delivered. He was noted to have hematuria and anuria on the day of the procedure. Creatinine increased to 4.5
|
| Patient #5 | Cr
|
Patient is a 69-year-old female with a history of tachycardia induced cardiomyopathy (EF 35-50%), hepatopathy, persistent AF who underwent ablation. The lesion set performed included pulmonary vein isolation, posterior wall isolation and mitral isthmus line. A total of 144 PFA applications were delivered. She was noted to have hematuria and anuria on the day of the procedure. Creatinine increased to
|
Extended Data Table 3 | Root Cause Analysis of Stroke Events
| Root Cause Analysis – Stroke N = 16 | |
| No definitive cause | 7 |
| Catheter exchanges/Sheath management | 4 |
| ACT < 300 | 2 |
| Interruption of anticoagulation | 2 |
| Uncontrolled Hypertension | 1 |
Extended Data Table 4 | Vascular Complications as a Function of Routine Vascular Ultrasound Usage
| Full Cohort* 106 Sites (
|
Routine Ultrasound Use 55 Sites (
|
Not Routine Ultrasound Use 48 sites
|
|
| Baseline Patient characteristics | |||
| Age (years), Mean (min-max) | 64.1 (11-96) | 64.5 (11-96) | 63.4 (20-96) |
| Female (%) | 34.6 | 34.1 | 35.4 |
| Total vascular complications | 441 (2.50) | 246 (2.45) | 195 (2.72) |
| Hematoma | 324 (1.84) | 193 (1.92) | 131 (1.83) |
| Pseudoaneurysm | 58 (0.33) | 28 (0.28) | 30 (0.42) |
| AV fistula | 46 (0.26) | 19 (0.19) | 27 (0.38) |
| Other | 13 (0.07) | 6 (0.06) | 7 (0.10) |
| Major (requiring intervention) | 53 (0.30) | 17 (0.17) * | 36 (0.50) * |
| Minor (no intervention) | 388 (2.20) | 229 (2.28) | 159 (2.22) |
| Clinical Site Characteristics | |||
| Practice type | |||
| Academic (%) | 61.4 | 70.9 | 52.1 |
| Private (%) | 17.8 | 5.5 | 29.2 |
| Hybrid (%) | 20.8 | 23.6 | 18.8 |
| No. of operators, mean (min-max) | 3.8 (1-11) | 4 (1-11) | 3.5 (1-9) |
| Years in practice, mean (min-max) | 13.5 (3-25) | 12.7 (3-25) | 14.6 (5.2-25) |
| Annual no. of AF ablations, mean (min-max) | 528 (80-2000) | 546 (80-1400) | 516 (100-2000) |
| No. of PFA cases performed, mean (min-max) | 167 (17-1277) | 182 (17-707) | 151 (18-1277) |
| *Statistically significant ( p value
|
|||
Extended Data Table 5| Details of Patient Deaths
| Timing of Death Post-Ablation | Cause of Death | Narrative Summary | |
| Patient #1 | 9 days | Unexplained Sudden Death | Unremarkable ablation procedure, but followed by unexplained death 9 days postprocedure. Autopsy failed to reveal any specific cause of death. |
| Patient #2 | 1 week | Cardiac Tamponade | 75-year-old man with ablation complicated by perforation and cardiac tamponade. Pericardiocentesis was unsuccessful, and thus requiring emergent surgical sternotomy. However, patient suffered irreversible brain damage and died 1 week later. |
| Patient #3 | 8 hours | Decompensated Heart Failure | 84-year-old man with tachycardia induced cardiomyopathy and admission 1 week preablation for decompensated heart failure. After 2 failed cardioversions, patient underwent PFA: pulmonary vein isolation and mitral isthmus line. Procedure was unremarkable – only transient intra-procedural hypotension. But, cardiogenic shock ensued 2 hours post-procedure necessitating mechanical circulatory support. There was no pericardial effusion, other bleeding, or acute coronary syndrome. Mechanical circulatory support was eventually discontinued, and patient died. Autopsy findings were unremarkable, and death was attributed to severe LV failure. |
| Patient #4 | 3 days | Cardiac Arrest (in setting of severe CAD) | 62 -year-old man with chronic kidney disease and multivessel coronary artery disease (prior stent), and preserved LV function. PFA unremarkable, and patient was discharged home. Two days later, patient developed chest pain and dizziness at home and collapsed. ACLS instituted by emergency personnel within 6 min of symptoms – initial rhythm was asystole, but spontaneous circulation returned. Upon arrival to hospital, ventricular fibrillation occurred, prompting ACLS measures. Extracorporeal membrane oxygenation was instituted. Coronary angiography revealed no acute lesions. Pulmonary angiography revealed no pulmonary embolism, and no pericardial effusion by echocardiography. He had continued hemodynamic instability, poor neurological recovery and died 24 hours later. |
| Patient #5 | 30 days | Cerebellar Hemorrhage | 60-year-old man underwent an uncomplicated ablation procedure, but he developed headache 8 days post-procedure and rapidly became unconscious. He died 30 days after ablation. Autopsy revealed massive cerebellar hemorrhage. |
Extended Data Table 6 | Complications in Both Cohorts – Initial MANIFEST-PF Sites vs Expanded MANIFEST-17K Sites
| Full Patient Cohort from All MANIFEST-17K Sites * 106 Sites (
|
Patients from Initial MANIFEST-PF Sites* 24 Sites (
|
Patients from Expanded MANIFEST-17K Sites * 82 Sites (
|
||||
| Major Adverse Events | 173 (0.98%) | 82 (1.04%) | 91 (0.93%) | |||
| Death | 5 (0.03)
|
0 (0) | 5 (0.05)
|
|||
| Stroke | 22 (0.12) | 11 (0.14) | 11 (0.11) | |||
| Esophageal fistula or dysmotility | 0 (0) | 0 (0) | 0 (0) | |||
| Pulmonary vein stenosis | 0 (0) | 0 (0) | 0 (0) | |||
| Phrenic nerve injury (persistent) |
|
|
|
|||
| Pericardial tamponade |
|
34 (0.43) | 29 (0.30)
|
|||
| Percutaneous intervention | 56 (0.32) | 30 (0.38) | 26 (0.27) | |||
| Surgical intervention | 7 (0.04)
|
4 (0.05) | 3 (0.03)
|
|||
| Vascular complication (with intervention) | 53 (0.30) | 24 (0.30) | 29 (0.30) | |||
| Coronary artery spasm | 25 (0.14) | 8 (0.10) | 17 (0.17) | |||
| Myocardial Infarction | 0 (0.0) | 0 (0) | 0 (0) | |||
| Hemolysis-Renal Failure (hospitalization) | 5 (0.03) | 5 (0.06) | 0 (0) | |||
| Other (thrombosis) | 1 (0.006) | 0 (0) | 1 (0.01) | |||
| Minor Adverse Events | 567 (3.21%) | 264 (3.35%) | 303 (3.10%) | |||
| Transient Ischemic Attack | 21 (0.12) | 8 (0.10) | 13 (0.13) | |||
| Phrenic nerve injury (transient) | 11 (0.06)
|
7 (0.09)
|
4 (0.04)
|
|||
| Pericardial effusion (no intervention) | 59 (0.33) | 24 (0.30) | 35 (0.36) | |||
| Pericarditis | 30 (0.17) | 12 (0.15) | 18 (0.18) | |||
| Vascular complications (no intervention) | 388 (2.20) | 177 (2.25) | 211 (2.16) | |||
| Hemolysis-Renal Failure (no hospitalization) | 1 (0.006) | 0 (0) | 1 (0.01) | |||
| Other complications | 57 (0.32) | 36 (0.46) | 21 (0.21) | |||
|
||||||
natureportfolio
Last updated by author(s): 5/15/2024
Reporting Summary
Statistics
Confirmed
For null hypothesis testing, the test statistic (e.g.
Our web collection on statistics for biologists contains articles on many of the points above.
Software and code

Data
Policy information about availability of data
- Accession codes, unique identifiers, or web links for publicly available datasets
- A description of any restrictions on data availability
- For clinical datasets or third party data, please ensure that the statement adheres to our policy
Research involving human participants, their data, or biological material
| Reporting on sex and gender | Data on sex and gender was self reported prospectively and in accordance to Nature’s guidelines |
| Reporting on race, ethnicity, or other socially relevant groupings | Data on race or ethnicity was not collected as part of this study |
| Population characteristics | There were a total of 17,642 patients, average age of 64 (range 11-96) and 34.7% female |
| Recruitment | This was a observational study of center level data. An invitation document was sent to each participating center via email. |
| Ethics oversight | This study was approved by the Ethical Committee at Homolka Hospital |
Field-specific reporting
Life sciences
For a reference copy of the document with all sections, see nature.com/documents/nr-reporting-summary-flat.pdf
Life sciences study design
| Sample size | This was a retrospective observational study design and sample size calculation was not performed |
| Data exclusions | All data reported by participating centers was utilized |
| Replication | There was no data replication as this was a new study on a unique patient population not previously evaluated |
| Randomization | Given the retrospective nature of the study, prospective randomization was not performed |
| Blinding | Given the retrospective nature of the study studying the same intervention and no placebo, blinding was not deemed to be necessary for the study |
Reporting for specific materials, systems and methods

Plants
| Seed stocks | Report on the source of all seed stocks or other plant material used. If applicable, state the seed stock centre and catalogue number. If plant specimens were collected from the field, describe the collection location, date and sampling procedures. | ||
| Novel plant genotypes | Describe the methods by which all novel plant genotypes were produced. This includes those generated by transgenic approaches, gene editing, chemical/radiation-based mutagenesis and hybridization. For transgenic lines, describe the transformation method, the number of independent lines analyzed and the generation upon which experiments were performed. For gene-edited lines, describe the editor used, the endogenous sequence targeted for editing, the targeting guide RNA sequence (if applicable) and how the editor | ||
| Authentication |
|
- e-mail: vivek.reddy@mountsinai.org
- Emmanuel Ekanem ©
, Petr Neuzil , Tobias Reichlin , Joseph Kautzner , Pepijn van der Voort , Pierre Jais , Gian-Battista Chierchia , Alan Bulava , Yuri Blaauw , Tomas Skala , Martin Fiala , Mattias Duytschaever , Gabor Szeplaki , Boris Schmidt , Grégoire Massoullie © , Kars Neven © , Olivier Thomas , Johan Vijgen , Estelle Gandjbakhch , Daniel Scherr , Arne Johannessen , David Keane , Serge Boveda , Philippe Maury , Ignacio García-Bolao , Ante Anic , Peter Steen Hansen , Franck Raczka , Antoine Lepillier , Yves Guyomar , Dhiraj Gupta , Jurren Van Opstal , Pascal Defaye , Christian Sticherling , Philipp Sommer , Pavel Kucera , Joaquin Osca , Fariborz Tabrizi , Antoine Roux , Michael Gramlich , Stefano Bianchi © , Pedro Adragão , Francesco Solimene , Claudio Tondo , Antonio Dello Russo , Jürgen Schreieck , Armin Luik , Obaida Rana © , Gerrit Frommeyer , Frédéric Anselme , Ingo Kreis , Raphael Rosso , Andreas Metzner , Laszlo Geller , Samuel H. Baldinger , Angel Ferrero , Stephan Willems , Andreas Goette , Greg Mellor , Shibu Mathew ,
