المجلة: Scientific Reports، المجلد: 14، العدد: 1
DOI: https://doi.org/10.1038/s41598-024-68316-8
PMID: https://pubmed.ncbi.nlm.nih.gov/39075155
تاريخ النشر: 2024-07-29
DOI: https://doi.org/10.1038/s41598-024-68316-8
PMID: https://pubmed.ncbi.nlm.nih.gov/39075155
تاريخ النشر: 2024-07-29
تقارير علمية
Fe3O4@SiO2@NTMPThio-Cu: نهج مستدام وصديق للبيئة لتخليق مشتقات الهتروسكل باستخدام محفز نانوي جديد من قالب دندريمر
الكلمات الرئيسية: الكيمياء الخضراء، الجسيمات النانوية المغناطيسية، الدندريمر، سبيروكسيندول-بيران، زانثين
لقد زاد التركيز على الكيمياء المتقدمة والصديقة للبيئة في التخليق العضوي العصري بشكل كبير في السنوات القليلة الماضية، مثل عدم استخدام المواد الكيميائية والمذيبات الخطرة أو الضارة، واستخدام المحفزات القابلة لإعادة التدوير والرخيصة، وتجنب ظروف التفاعل غير المناسبة. على مر السنين، كان هناك اهتمام متزايد باستخدام المواد الكيميائية أو المذيبات الصديقة للبيئة، واقتصاد الذرات المقبول، وتحسين ظروف التخليق العضوي لتقليل استهلاك الطاقة.
لقد زاد التركيز على الكيمياء المتقدمة والصديقة للبيئة في التخليق العضوي العصري بشكل كبير في السنوات القليلة الماضية، مثل عدم استخدام المواد الكيميائية والمذيبات الخطرة أو الضارة، واستخدام المحفزات القابلة لإعادة التدوير والرخيصة، وتجنب ظروف التفاعل غير المناسبة. على مر السنين، كان هناك اهتمام متزايد باستخدام المواد الكيميائية أو المذيبات الصديقة للبيئة، واقتصاد الذرات المقبول، وتحسين ظروف التخليق العضوي لتقليل استهلاك الطاقة.
اليوم، واحدة من أكبر التحديات في صناعة التطورات العضوية هي إيجاد طرق لاستخدام تقنيات كيميائية نظيفة ومستدامة لإنتاج مواد كيميائية مفيدة. من بين الأساليب لتحقيق هذا الهدف المهم هو استخدام المحفزات المستقرة التي تعمل في الكيمياء الخضراء. تشير تحقيقات الباحثين إلى أن استخدام المحفزات غير المتجانسة في العمليات الصناعية الكيميائية قد اكتسب مكانة خاصة. هذه المحفزات صديقة للبيئة وتساعد في إنتاج وقود مستدام والعديد من المواد الكيميائية الأساسية.
تعتبر تقنية النانو واحدة من أهم أجزاء المجالات العلمية الحديثة. تتيح علوم النانو للعلماء في مجالات مختلفة مثل الطب والهندسة والكيمياء تحقيق تقدم كبير يتماشى مع أهدافهم على المستويات الجزيئية والخلوية. في السنوات الأخيرة، وبفضل حجمها الفريد ومساحتها السطحية العالية، وجدت الجسيمات النانوية المغناطيسية تطبيقات خاصة في الصناعة والعلوم البيولوجية، مثل العلاج الجيني، وتوصيل الأدوية، وتخزين المعلومات، وأجهزة الاستشعار، وغيرها.
تم اعتبار الجسيمات النانوية المغناطيسية بسبب ميزاتها الخاصة مثل السمية المنخفضة، التوافق مع البيئة، رخص تكلفة السطح الذي يمكن تغييره مع مجموعات مختلفة، وسهولة الإزالة المغناطيسية.
الاهتمام في الدراسات
لقد اكتسبت الدندريمر، وهي نوع من البوليمرات المتفرعة المكونة من وحدات متكررة تمتد للخارج من نواة مركزية، شعبية كبيرة. وقد حظيت باهتمام كبير بسبب تناظرها الهندسي العالي القابل للتحكم، ووزنها الجزيئي، وبنيتها الجزيئية المحددة جيدًا. بالإضافة إلى قابليتها للذوبان في الماء، وتعدد القيم، واحتجاز جزيئات الأدوية المحبة للماء، تم الإشارة إلى الدندريمر كنظم توصيل الأدوية البوليمرية.
ثيوسيماكاربازيد هو مكون هيكلي مفيد له القدرة على أداء وظائف كيميائية في الجزيئات النشطة بيولوجيًا، ويمكن أن تؤدي المزيد من الدراسات حول هذه البنية إلى اكتشاف أساس لنوع جديد من العوامل العلاجية. تظهر الأبحاث أن مشتقاتها لها أنشطة مضادة للبكتيريا، ومضادة للأورام، ومضادة للفطريات، ومضادة للتشنجات. من ناحية أخرى، تعتبر أيضًا مضادات أكسدة جيدة (الشكل 1). إنها مجموعة خاصة من المركبات العضوية المعروفة ليس فقط بتنوع أنشطتها البيولوجية ولكن أيضًا كعامل خالب للمعادن ومضاد للتآكل.
الزانثينات هي مركبات حلقية غير متجانسة. تحتوي هذه المجموعة من المركبات العضوية على مجموعة واسعة من الخصائص البيولوجية والطبية، بما في ذلك مضادات السرطان، والعلاج الضوئي الديناميكي، والمضادات البكتيرية، والمضادات الفيروسية، ومضادات الالتهاب.
استنادًا إلى أبحاثنا السابقة حول تخليق المحفزات وتطبيقاتها
تجريبي
تم شراء جميع المواد الكيميائية من ميرك وسيغما ألدريش واستخدمت دون تنقية. تم الحصول على أنماط حيود الأشعة السينية (XRD) باستخدام جهاز فيليبس PW-1830. تم استخدام جهاز Electro thermal 9100 لتحديد نقاط الانصهار. تم تسجيل منحنيات التحليل المغناطيسي باستخدام نموذج VSM MDKB من شركة دانش پاجوهان كافير، كاشان، إيران. تم الكشف عن طيف FT-IR باستخدام مطياف الأشعة تحت الحمراء شيمادزو IR-470.
تحضير
الخطوات الاصطناعية لـ
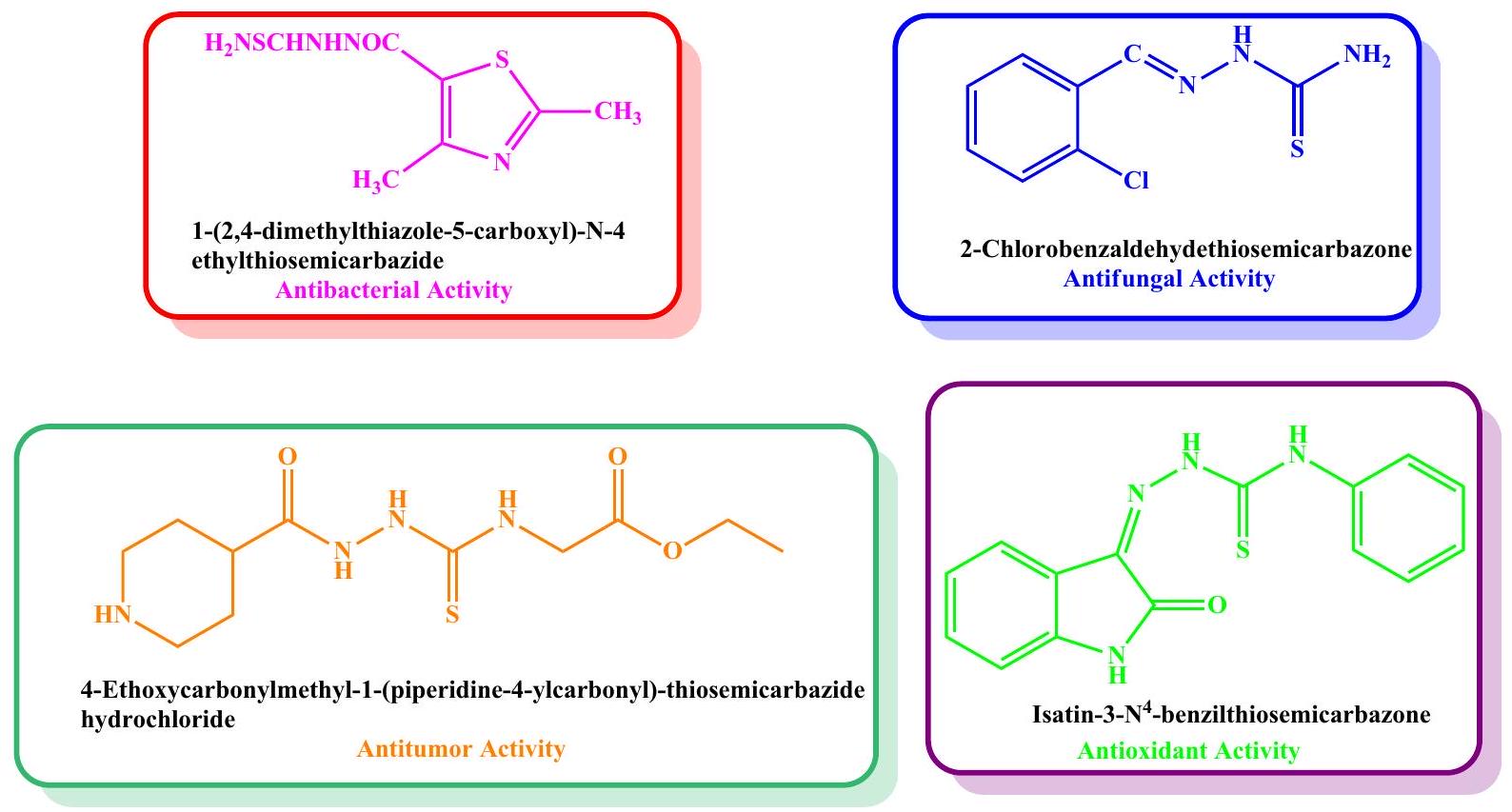
الشكل 1. بعض هياكل الثيوسيماكاربازيد لها خصائص بيولوجية.
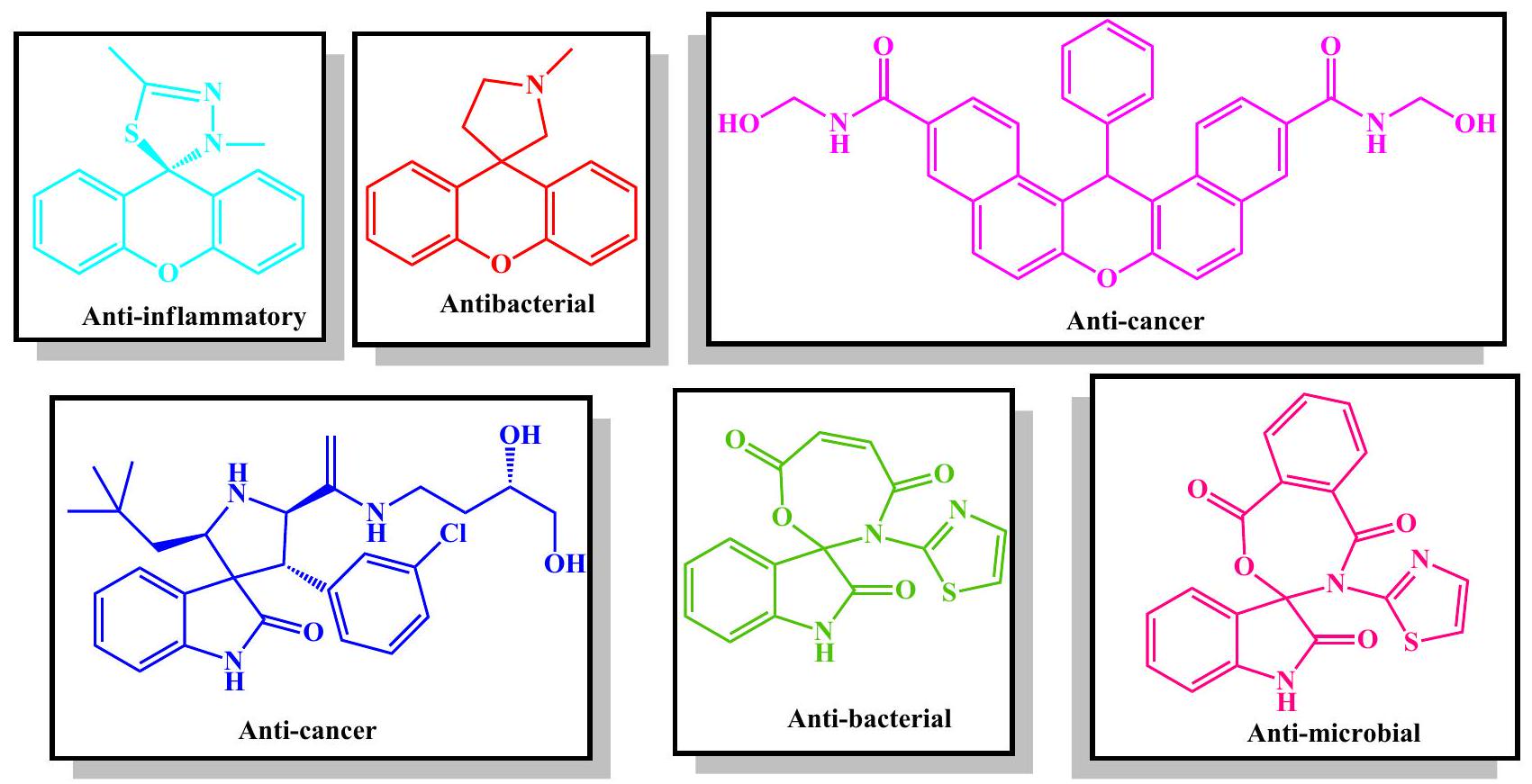
الشكل 2. المركبات النشطة بيولوجيًا ذات هياكل الزانثين والسبيروكسيندول.
تحضير
تم تعريض 1 جرام من الجسيمات النانوية من الخطوة السابقة لموجات فوق صوتية في THF جاف (40 مل). في الخطوة التالية، تم إضافة كلوريد السيانوريك (TCT) (0.5 جرام) و
تحضير
1 جرام من
تحضير
1 جرام من
تحضير
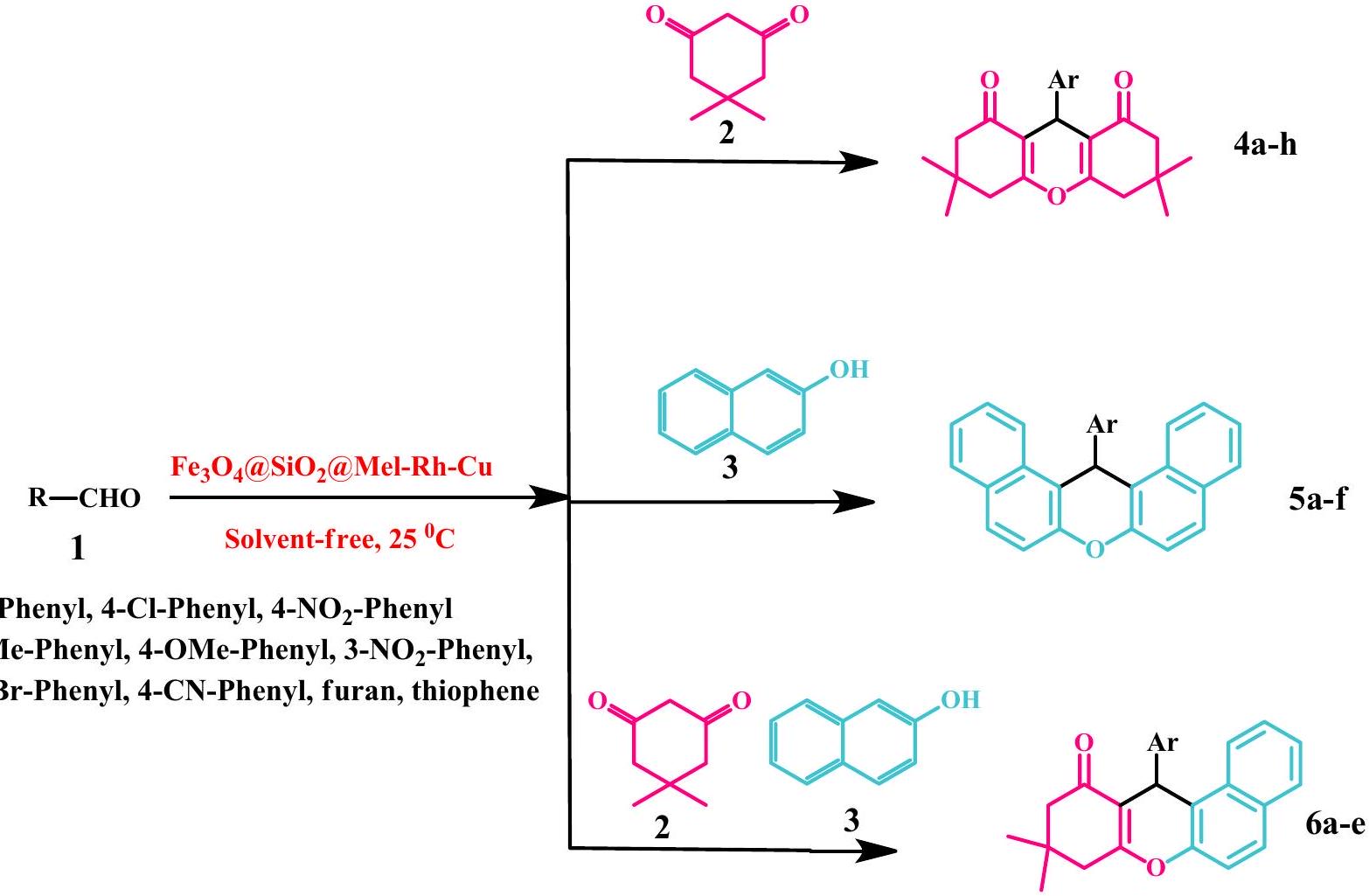
الإجراء العام لتخليق الزانثينات
خليط من الديميدون (2 مليمول) و/أو
الإجراء العام لتخليق مشتقات سبيروكسيندول-بيران (10a-t)
1 مليمول من الإيزاتين، 1 مليمول من المالونونيتريل، 1 مليمول من مركبات الديكربونيل 1,3، و
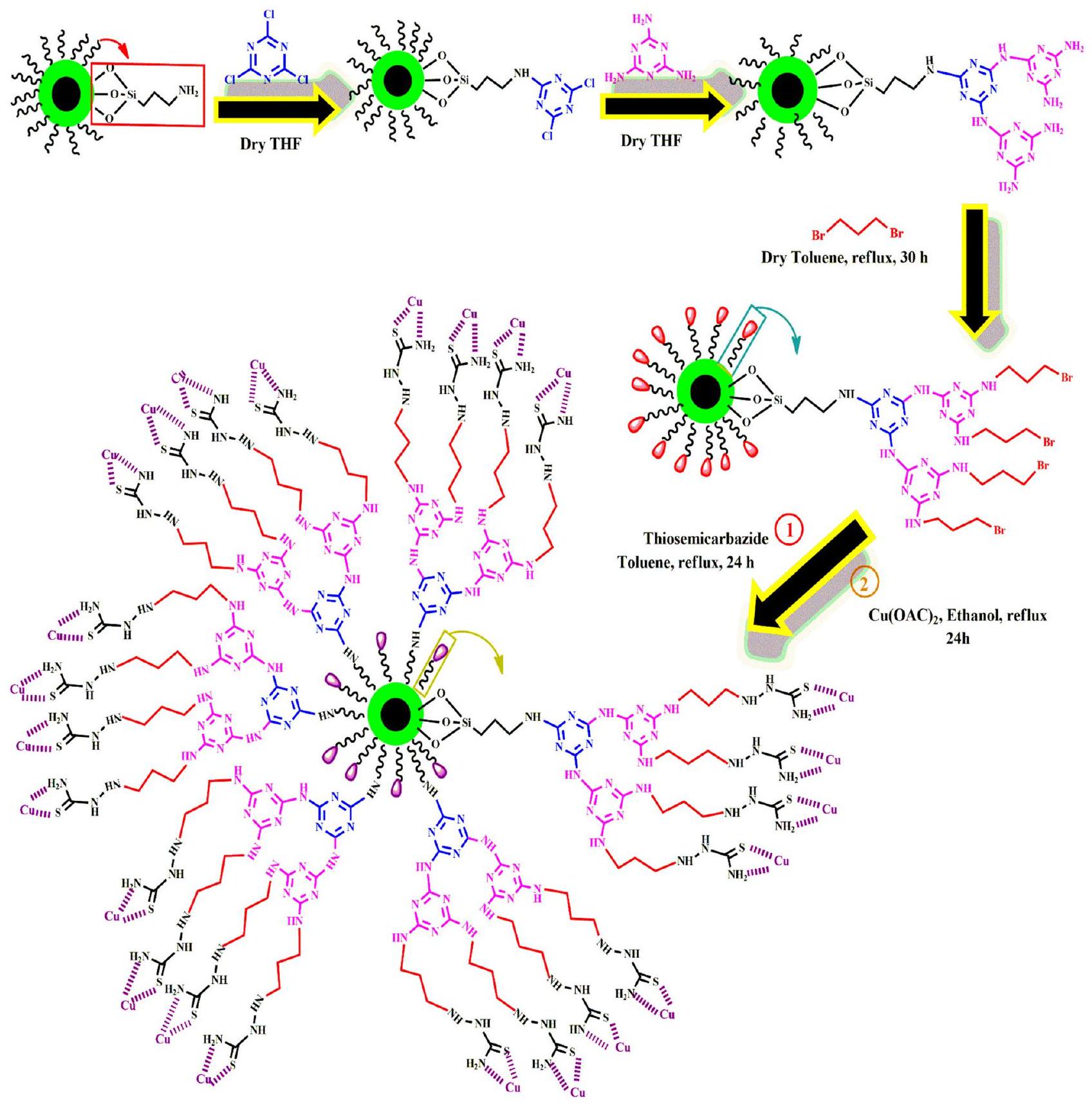
المخطط 1. تحضير
بيانات طيفية للمنتجات المختارة
مركب
مركب
المركب (5أ)
المركب (5ج)
المركب (5f)
المخطط 2. تحضير الزانثينات في وجود

المخطط 3. تحضير مشتقات سبيروكسيندول-بيران في وجود
المركب (6ب)
المركب (6د)
المركب (10أ)
مركب (10 ف)
مركب (10م)
مركب (10o)
مركب (10ل)
الموافقة الأخلاقية
لا يحتوي هذا العمل على أي دراسات مع مشاركين بشريين أو حيوانات أجراها أي من المؤلفين.
النتائج والمناقشات
تم تقديم تصميم عقلاني يهدف إلى إعداد محفز نانوي جديد عالي الأداء وقابل لإعادة التدوير يعتمد على الدندريمر ويحتوي على ثيوسيماكاربازيد (المخطط 1). أولاً، تم تصنيع جزيئات مغناطيسية باستخدام طريقة الترسيب المشترك، ثم تم تغليفها بطبقة من السيليكا لحمايتها وتحقيق سطح قابل للتعديل مع شكل كروي. في الخطوة التالية، تم تعديل السطح باستخدام APTES، وبعد ذلك، تم وضع 1، 3-ديبروموبروبان، كلوريد السيانوريك، الميلاتونين، وثيوسيماكاربازيد في الخطوة الأخيرة. ثم تم وضع معدن النحاس في ظروف مناسبة لإجراء تفاعلات تحضير مشتقات الزانثين وسبيروكسيندول-بيران.
تم فحص المجموعات الوظيفية في فترات تخليق المحفز باستخدام مطيافية FT-IR (الشكل 3). القمة في منطقة
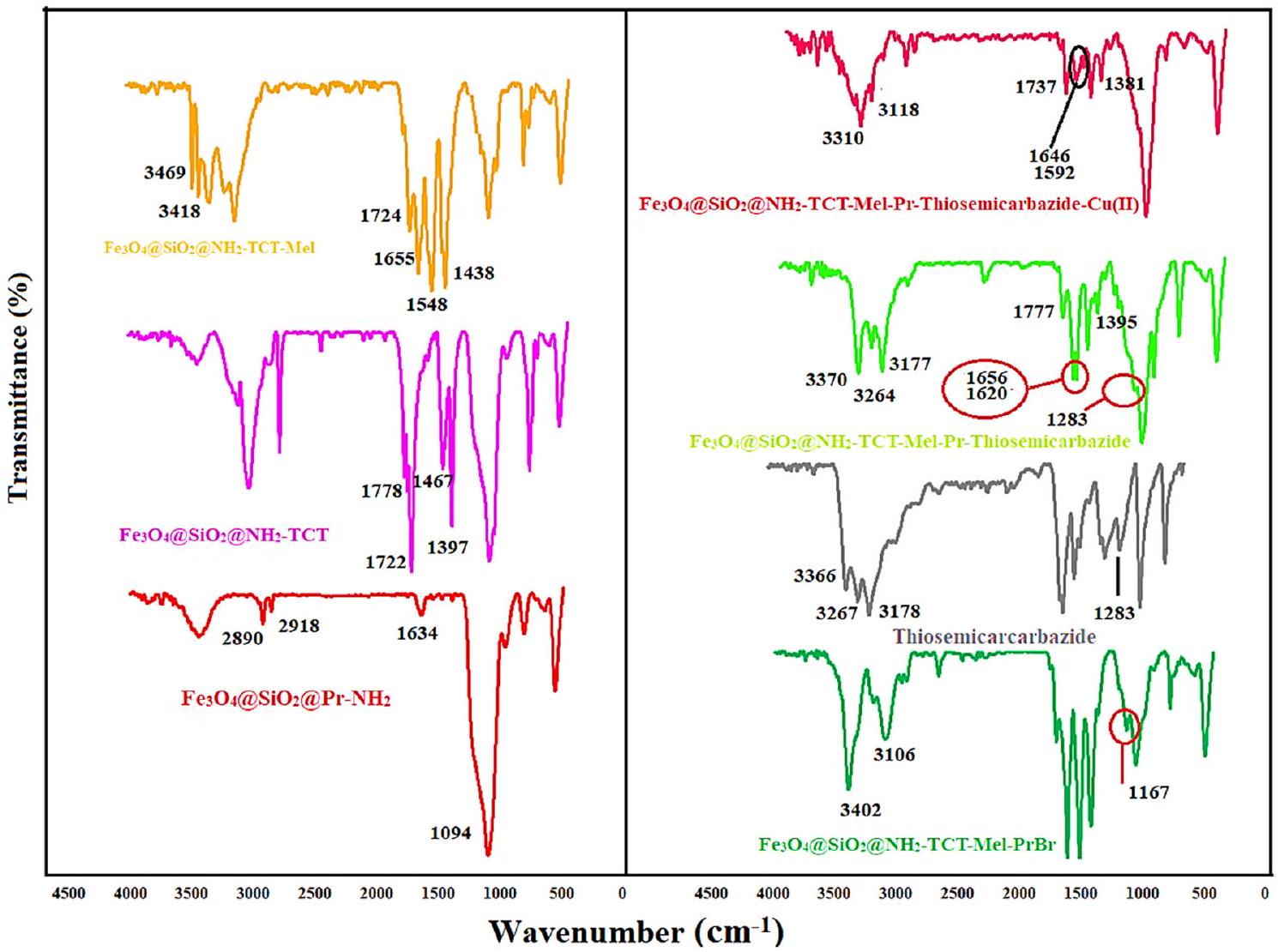
الشكل 3. خطوات تخليق FT-IR
رابطة تساهمية للثيوسيماكربازيد مع الكاربازيد مع أطياف امتصاص الأشعة تحت الحمراء عند 3177 و 3264
البلورية لـ
الاستقرار الحراري لـ
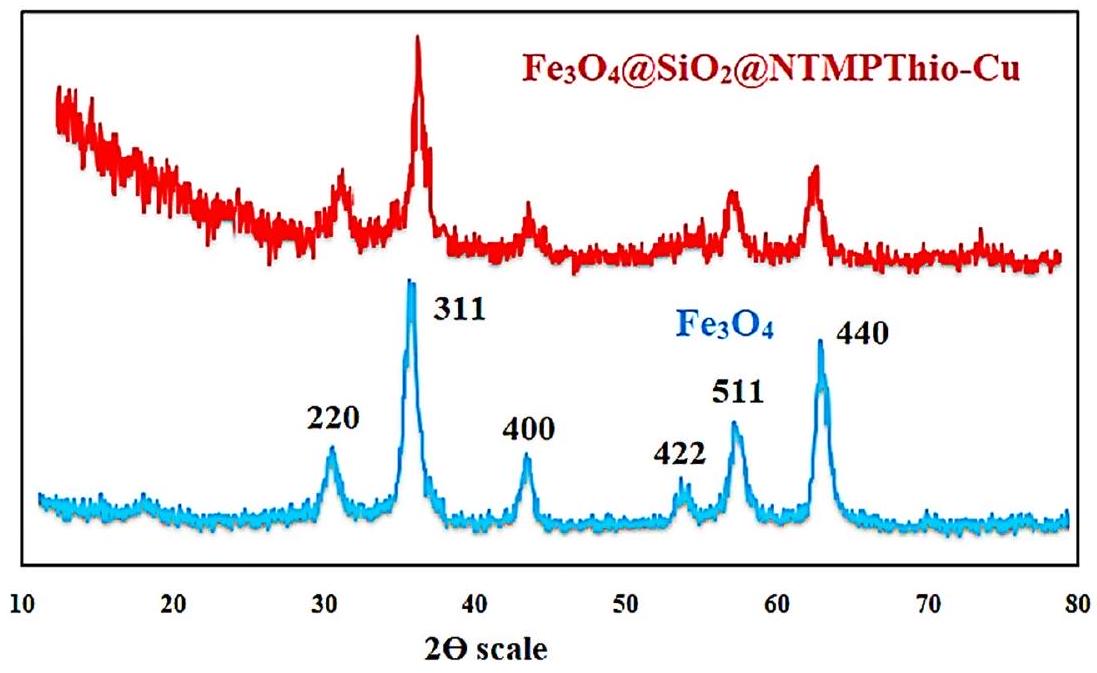
الشكل 4. أنماط حيود الأشعة السينية (XRD) لـ

الشكل 5. منحنيات TGA لـ (A)
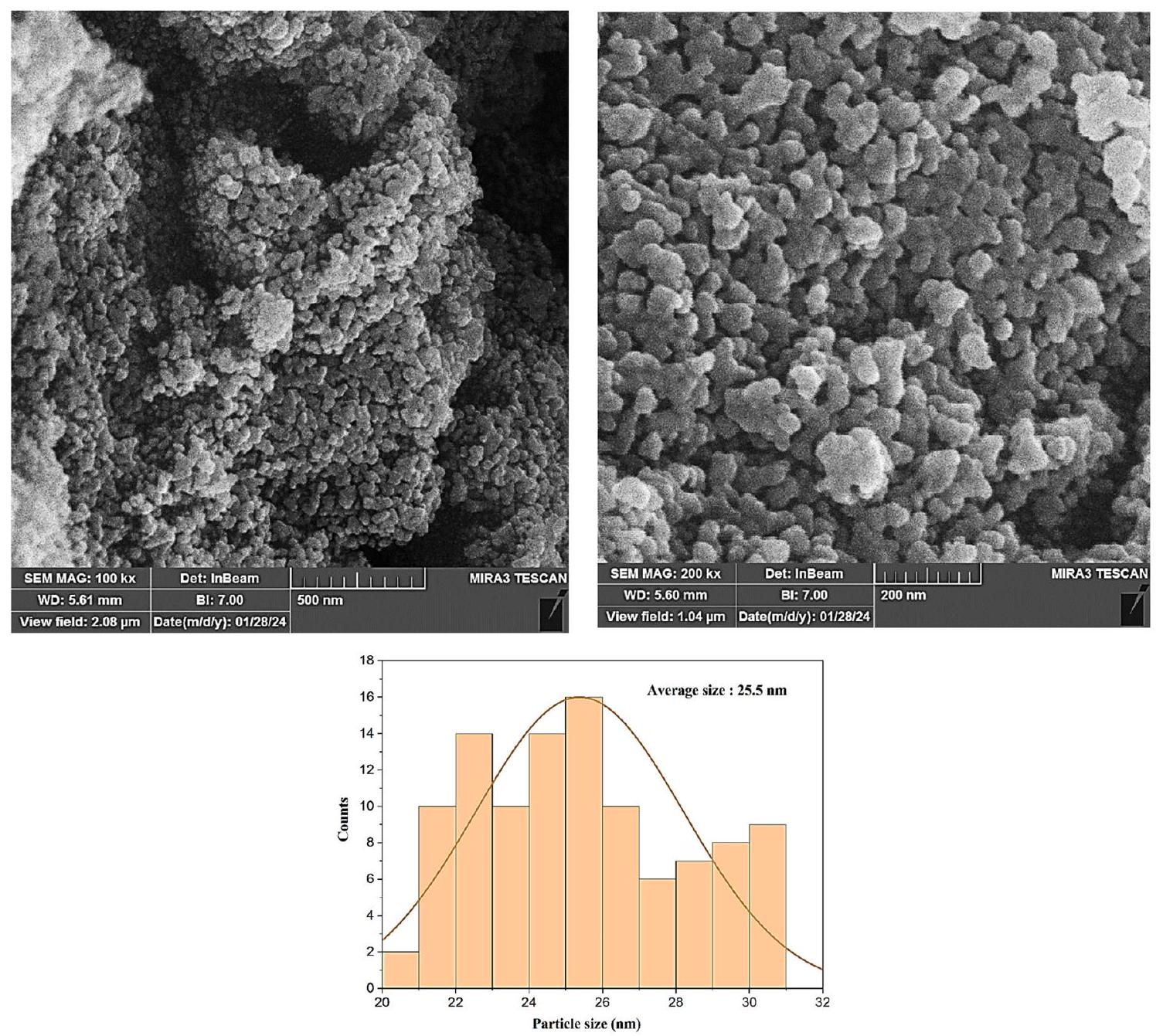
الشكل 6. صور FE-SEM لـ

الشكل 7. صور TEM لـ
تظهر الفحوصات المورفولوجية باستخدام TEM و FE-SEM أن الجسيمات النانوية المغناطيسية. من خلال وضع طبقة السيليكا وتثبيت الروابط على الركيزة، فإن لها هيكلًا كرويًا بمتوسط حجم جسيم يبلغ 25.5 نانومتر. صور TEM لـ
السلوك المغناطيسي لـ
في هذه المخطوطة، سعينا لاستغلال الخاصية الأساسية لمعدن النحاس على دندريمر. بالنظر إلى مزايا استخدام أنظمة التحفيز غير المتجانسة، فإن تخليق هذه الأنظمة له أهمية كبيرة. لتحقيق هذا الهدف، كان من الضروري اختيار دعم مناسب ومواد ربط لتحقيق النتيجة المرجوة. تقدم السيليكا النانوية نفسها كخيار مناسب بسبب وجود مجموعات وظيفية مناسبة على سطحها. بعد ذلك، تم استخدام كلوريد السيانوريك، تلاه الميلاتونين وثيوسيماكاربازيد لإنتاج قوالب دندريمر متعددة الفروع. أخيرًا، تم تشكيل معقد معدن النحاس بمساعدة الذرات في ثيوسيماكاربازيد. علاوة على ذلك، لتسهيل فصل وإعادة استخدام المحفز، تم مغنطة النانوكاتاليست. سمح ذلك بفصل سهل من بيئة التفاعل من خلال استخدام مجال مغناطيسي خارجي، مما مكن من إعادة الاستخدام في الخطوات اللاحقة.
تفاعل التخليق للزانثينات، والسبيروكسيندول-بيرانات في وجود
لكشف الظروف المثلى لتخليق الزانثينات، تفاعل
بعد تحديد الظروف المثلى، تم تقييم أداء المحفز. باستخدام تفاعل الألدهيدات الأريلية،
بعد ذلك، لتحديد الظروف المثلى في تخليق مشتقات سبيروكسيندول-بيران، تم اختيار مالونيتريل (1 مليمول)، ديميدون (1 مليمول)، وإيزاتين (1 مليمول) كردود فعل نموذجية. أولاً، كانت التفاعل في جوار
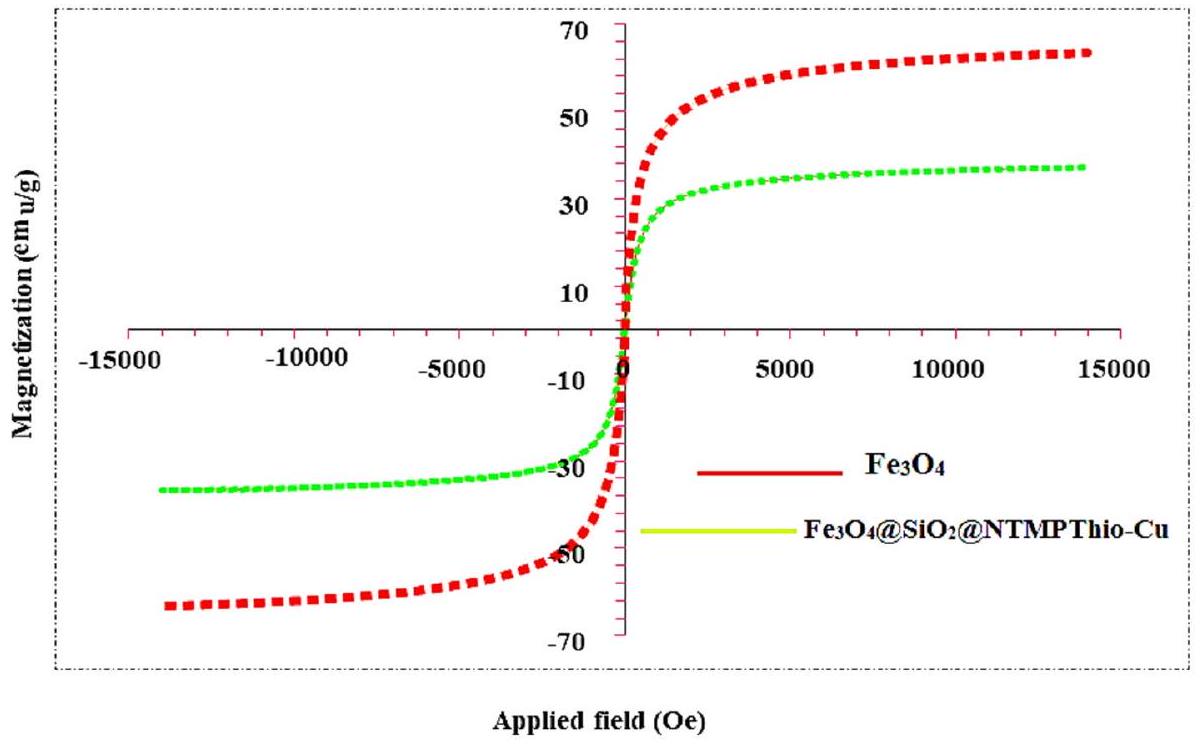
الشكل 8. طيف VSM لـ
| دخول | المحفز (ملغ) | مذيب | درجة الحرارة (
|
الوقت (دقيقة) | العائد (%) |
| 1 |
|
إيثانول | 25 | 12 | 85 |
| 2 |
|
|
25 | 12 | 60 |
| ٣ |
|
|
٢٥ | 12 | 75 |
| ٤ |
|
|
٢٥ | 12 | ٨٠ |
| ٥ |
|
خالي من المذيبات | ٢٥ | 12 | 97 |
| ٦ |
|
خالي من المذيبات | 40 | 12 | 97 |
| ٧ |
|
خالي من المذيبات | 60 | 12 | 97 |
| ٨ |
|
خالي من المذيبات | ٢٥ | 12 | 90 |
| 9 |
|
خالي من المذيبات | ٢٥ | 12 | 97 |
| 10 |
|
خالي من المذيبات | ٢٥ | 12 | 97 |
| 11 |
|
خالي من المذيبات | ٢٥ | 12 | 97 |
| 12 | – | خالي من المذيبات | 25 | 12 | أثر |
الجدول 1. تخليق الزانثينات باستخدام
المدخلات 8-10). كانت التفاعل النموذجي غير فعال في غياب المحفز، وفي وجود
لتوسيع نطاق التفاعل، قمنا بتشغيل
في الأدبيات السابقة، تم استخدام العديد من المحفزات في تخليق مشتقات الزانثين وسبيروكسيندولبيران. في المتابعة، تم تقييم أداء المحفز المُصنَّع من خلال مقارنته بمحفزات أخرى في تفاعلات نموذجية (الجدول 5). كما هو موضح،
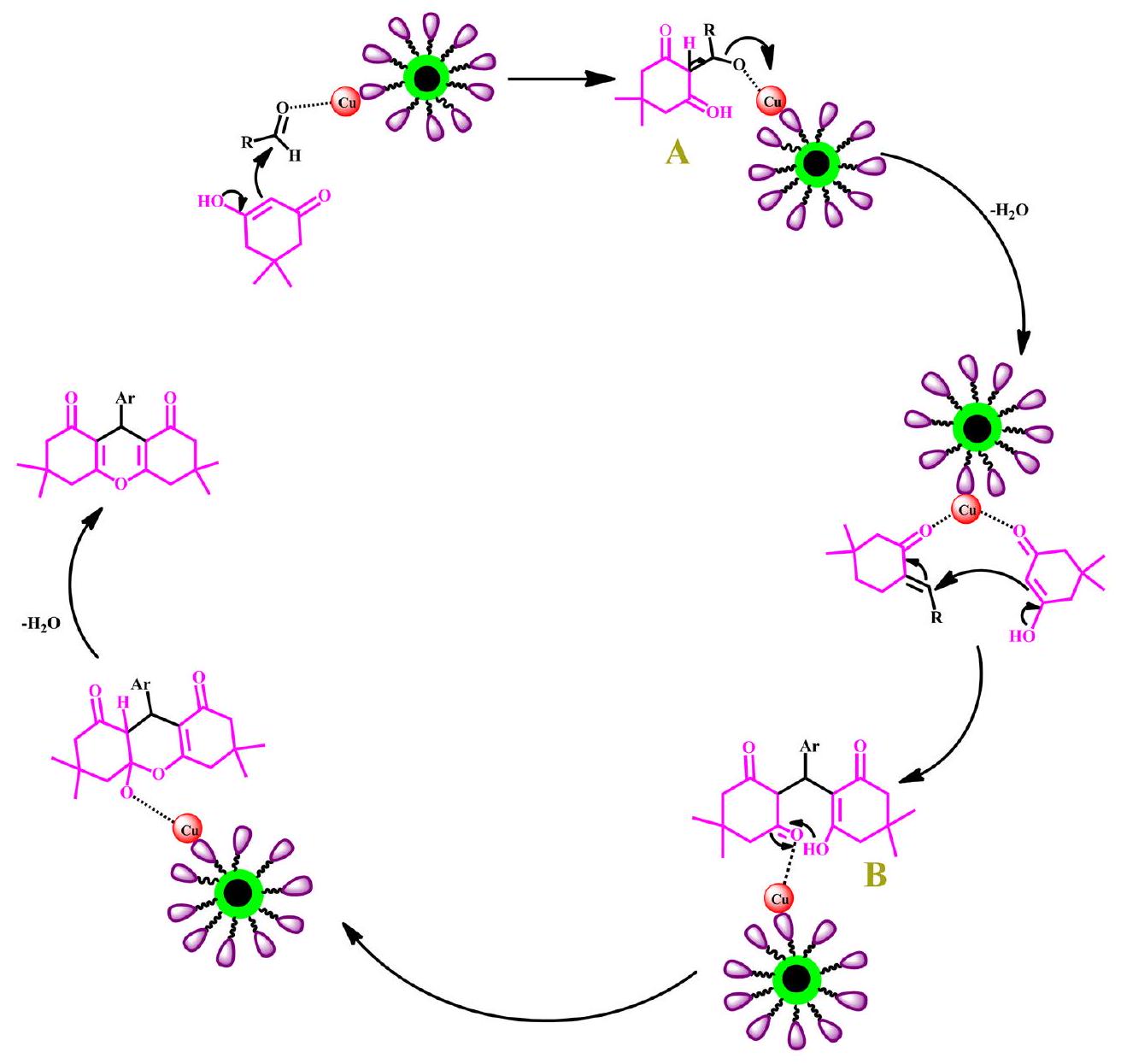
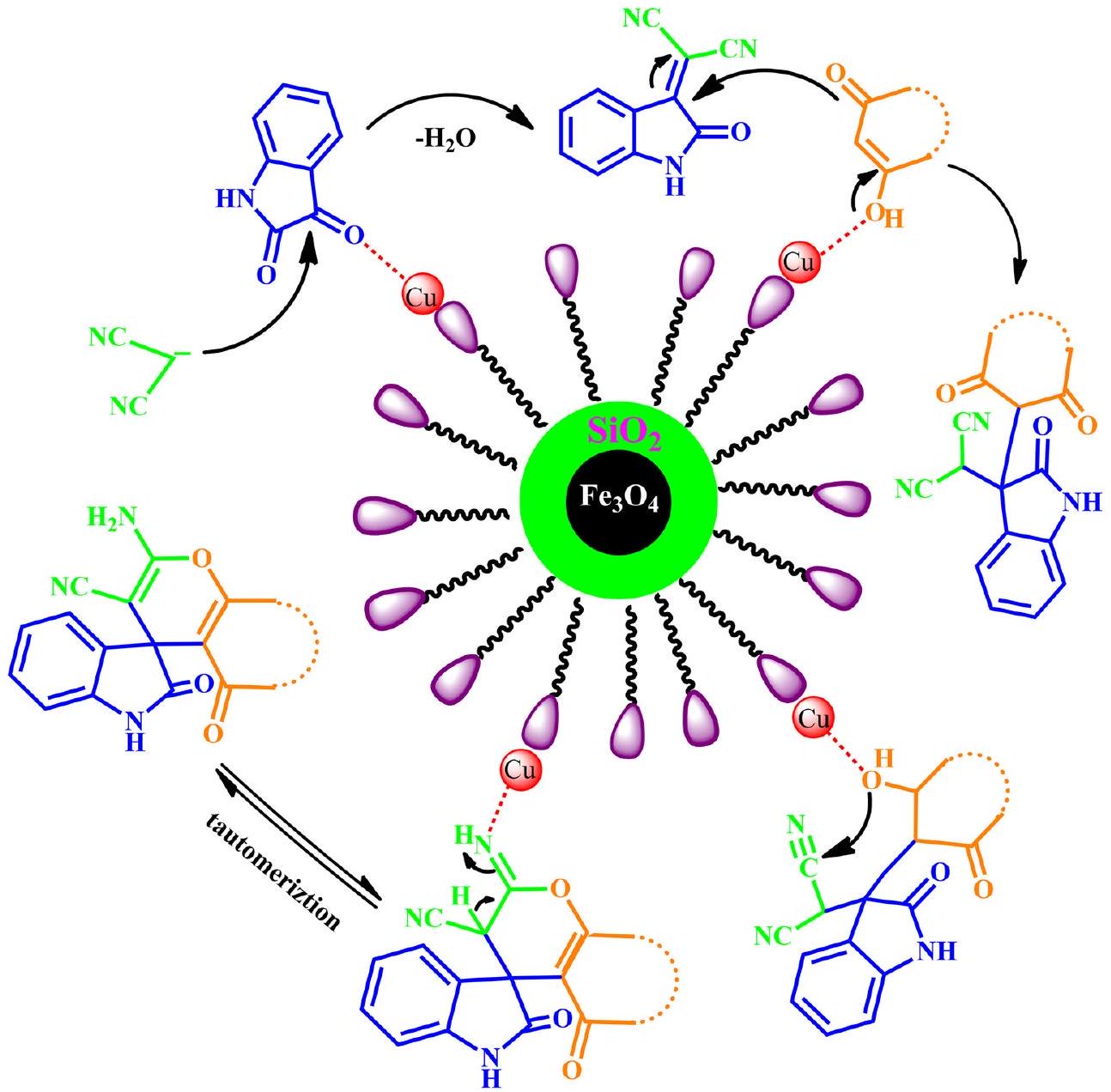
آلية التخليق للزانثينات ومشتقات سبيروكسيندول-بيران موضحة في المخططات 4 و 5.
آلية تركيب مشتقات الزانثين: في البداية، من خلال تنشيط مجموعة الكربونيل، يجعل المحفز الألدهيدات أكثر حساسية للهجوم النووي بواسطة الديميدون لتكوين الوسط (A)، في الخطوة التالية، يتم إضافة جزيء آخر من الديميدون بواسطة تفاعل مايكل لتكوين الوسط (B). من خلال القضاء على
آلية تركيب مشتقات الزانثين: في البداية، من خلال تنشيط مجموعة الكربونيل، يجعل المحفز الألدهيدات أكثر حساسية للهجوم النووي بواسطة الديميدون لتكوين الوسط (A)، في الخطوة التالية، يتم إضافة جزيء آخر من الديميدون بواسطة تفاعل مايكل لتكوين الوسط (B). من خلال القضاء على
المسار المحتمل لتخليق سبيروكسيندول-بيران في وجود
إعادة تدوير المحفز
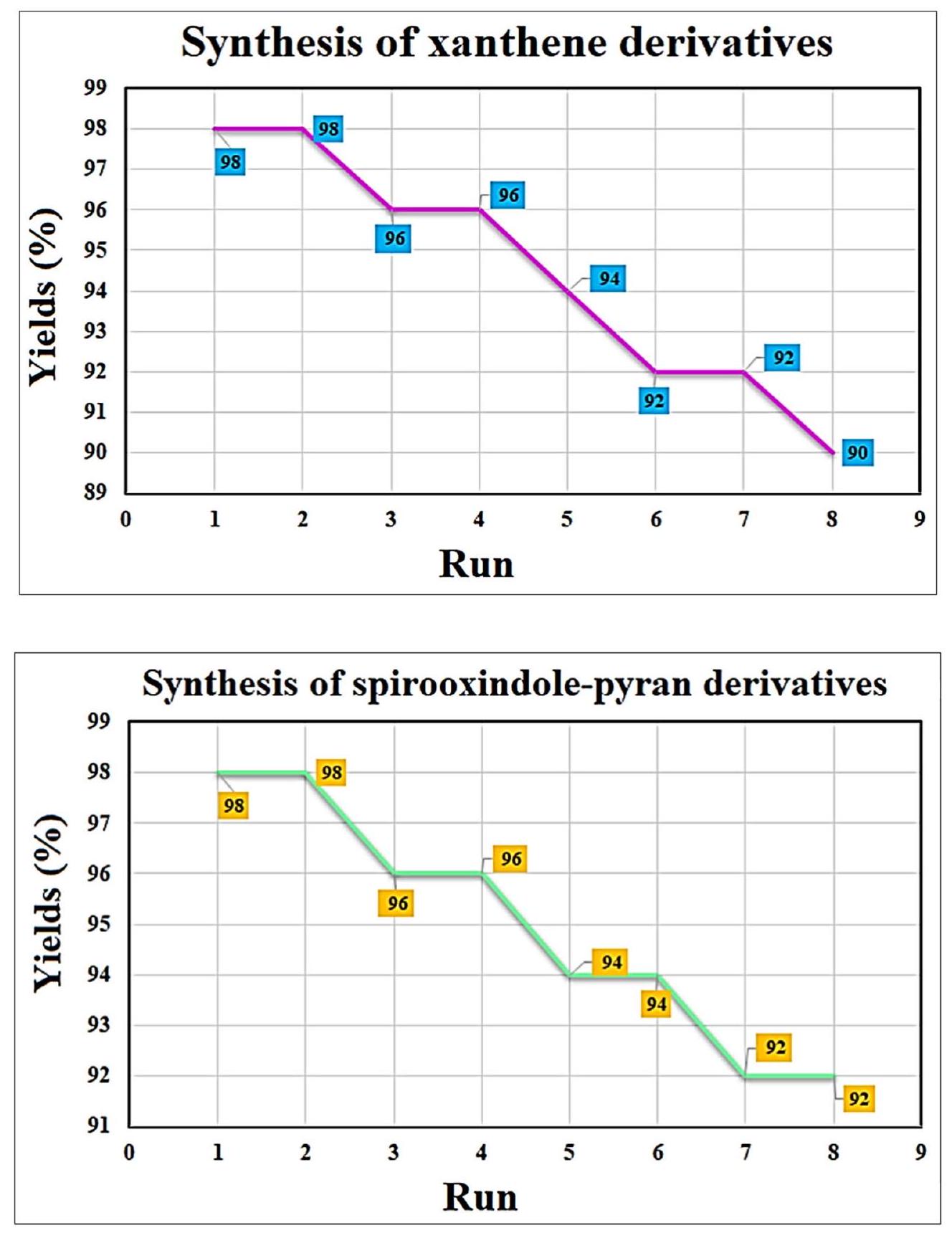
أحد التحديات الرئيسية التي يواجهها الكيميائيون المشاركون في تخليق المحفزات هو ضمان إمكانية إعادة استخدام المحفزات. لذلك، فإن البحث في هذه القضية الكبيرة أمر لا مفر منه. في هذه التجربة، بعد فصل المحفز، قمنا بغسله بالإيثانول وتجفيفه لإعادة استخدامه. أظهرت الدراسات أنه يمكن إجراء ما لا يقل عن ثمانية خطوات باستخدام هذا المحفز دون تغيير كبير في الأداء (الشكل 9). أيضًا، للدراسة الإضافية، تم فحص صورة FE-SEM، وطيف FT-IR، وأنماط XRD بعد 8 دورات إعادة تدوير، والتي لا تظهر أي اختلاف كبير. (الشكل 10).
تم أيضًا تحليل فحص تسرب جزيئات النحاس النانوية من المحفز النانوي في التفاعلات النموذجية. وأشارت نتائج تحليل ICP-OES إلى أن كمية تسرب النحاس في المحفز بعد 7 خطوات إعادة تدوير هي
الخاتمة
من أجل إنشاء نانو محفزات خضراء ذات أداء عالٍ وصديقة للبيئة وقابلة لإعادة الاستخدام وإعادة التدوير لمدة لا تقل عن 8 دورات متتالية دون فقدان كبير في النشاط، قمنا بنجاح بتخليق محفز جديد ومستقر ذو نواة مغناطيسية على شكل قشرة. تم تحديد المحفز باستخدام طرق تحليلية مختلفة. أداء
| مدخل | منتج | الوقت (دقيقة) | العائد (%) | نائب برلماني
|
||
| 1 |
|
12 | 97 |
|
||
| ٢ |
|
10 | 98 | 232-233
|
||
| ٣ |
|
15 | 98 |
|
||
| ٤ |
|
20 | 92 | 229-230
|
||
| ٥ |
|
20 | 94 |
|
||
| مستمر | ||||||
| دخول | منتج | الوقت (دقيقة) | العائد (%) | نائب برلماني
|
||
| ٦ |
|
٢٥ | 96 |
|
||
| ٧ |
|
20 | 96 | 286-287
|
||
| ٨ |
|
60 | 92 |
|
||
| 9 |
|
50 | 92 | 151-152
|
||
| 10 |
|
12 | 96 |
|
||
| مستمر | ||||||
| مدخل | منتج | الوقت (دقيقة) | العائد (%) | نائب برلماني
|
||
| 11 |
|
10 | 98 |
|
||
| 12 |
|
10 | 96 |
|
||
| ١٣ |
|
10 | 96 |
|
||
| 14 |
|
10 | 96 | 316-318
|
||
| مستمر |
| دخول | منتج | الوقت (دقيقة) | العائد (%) | نائب برلماني
|
||
| 15 |
|
15 | 92 | ٢٢٠-٢٢١
|
||
| 16 |
|
15 | 90 | ٢٠٢-٢٠٤
|
||
| 17 |
|
20 | 90 |
|
||
| ١٨ |
|
20 | 98 | ١٧٦-١٧٧
|
||
| مستمر | ||||||
| مدخل | منتج | الوقت (دقيقة) | العائد (%) | نائب برلماني
|
||
| 19 |
|
20 | 96 | 199-201
|
||
| 20 |
|
20 | 96 |
|
||
| 21 |
|
٢٢ | ٨٨ |
|
||
| ٢٢ |
|
90 | ٨٠ |
|
الجدول 2. تخليق المشتقات 4a-f و 5a-f و 6a-d بواسطة
| مدخل | المحفز (ملغ) | مذيب | درجة الحرارة (
|
الوقت (دقيقة) | العائد (%) |
| 1 |
|
إيثانول | ٢٥ | ٤ | 98 |
| ٢ |
|
THF | ٢٥ | ٤ | 75 |
| ٣ |
|
|
٢٥ | ٤ | 65 |
| ٤ |
|
|
25 | ٤ | 95 |
| ٥ |
|
خالي من المذيبات | ٢٥ | ٤ | ٩٨ |
| ٦ |
|
خالي من المذيبات | 40 | ٤ | 98 |
| ٧ |
|
خالي من المذيبات | 60 | ٤ | 98 |
| ٨ |
|
خالي من المذيبات | ٢٥ | ٤ | 92 |
| 9 |
|
خالي من المذيبات | 25 | ٤ | 98 |
| 10 |
|
خالي من المذيبات | ٢٥ | ٤ | 98 |
| 11 |
|
خالي من المذيبات | 25 | ٤ | 30 |
| 12 |
|
خالي من المذيبات | ٢٥ | ٤ | ٨٨ |
| ١٣ | – | خالي من المذيبات | 25 | ٤ | – |
الجدول 3. تخليق سبيروكسيندول-بيران باستخدام
| دخول | منتج | الوقت (دقيقة) | العائد (%) |
|
| 1 | 10 أ | 12 | 97 |
|
| ٢ | 10 ب | 10 | 98 |
|
| ٣ | 10 ج | 15 | 98 |
|
| ٤ | 10 د | 20 | 92 |
|
| مستمر |
| مدخل | منتج | الوقت (دقيقة) | العائد (%) | نائب برلماني
|
||
| ٥ | 10 يورو | 20 | 94 | 229-230
|
||
| ٦ | 10 ف | ٢٥ | 96 |
|
||
| ٧ | 10 جرام | 20 | 96 |
|
||
| ٨ | 10 ساعات | 12 | 96 |
|
||
| 9 |
|
10 | 98 |
|
||
| مستمر |
| مدخل | منتج | الوقت (دقيقة) | العائد (%) |
|
| 10 | 10 ج | 10 | 96 |
|
| 11 | 10 ك | 10 | 96 |
|
| 12 | ١٠١ | 10 | 96 |
|
| ١٣ | 10 م | 15 | 92 |
|
| 14 | 10 ن | 15 | 90 |
|
| مستمر |
| مدخل | منتج | الوقت (دقيقة) | العائد (%) | نائب برلماني
|
| 15 | 100 | 20 | 90 |
|
| 16 | 10 ب | 20 | 98 |
|
| 17 | 10 ق | 20 | 96 |
|
| 18 | 10 ر | 20 | 96 |
|
الجدول 4. تخليق سبيروكسيندول-بيران بواسطة
| عينة | الشروط | الوقت | العائد (%) |
 |
هذا البحث/خالي من المذيبات/
|
12 دقيقة | ٩٨ |
| أمبرليست-15/
|
٢ | 93 | |
| مدعوم بالسيليكا
|
ح | 98 | |
| SBA-15/
|
30 دقيقة | 95 | |
| كبريتات السليلوز/ بدون مذيبات/
|
24 ساعة | 97 | |
|
|
1 ساعة | 93 | |
| كبريتات الألمنيوم والبوتاسيوم
|
3 ساعات | 90 | |
|
|
3 ساعات | 98 | |
| هذا البحث / خالي من المذيبات
|
4 دقائق | 98 | |
| L-برولين /
|
20 دقيقة | 94 | |
|
|
120 دقيقة | 95 | |
|
|
20 دقيقة | 95 | |
| مغنيسيا
|
120 دقيقة | 95 | |
| PSGO-
|
120 دقيقة | 96 | |
| حمض السيليكا الكبريتي NPs/إيثانول/80
|
30 دقيقة | 96 |
الجدول 5. مقارنة المحفزات
المخطط 4. الآلية الاصطناعية لمشتقات الزانثين.
المخطط 5. الآلية التركيبية لمشتقات سبيروكسيندول-بيران.
الشكل 9. قابلية إعادة تدوير المحفز في تفاعل نموذج تخليق الزانثين والسبيروكسيندول-بيران.
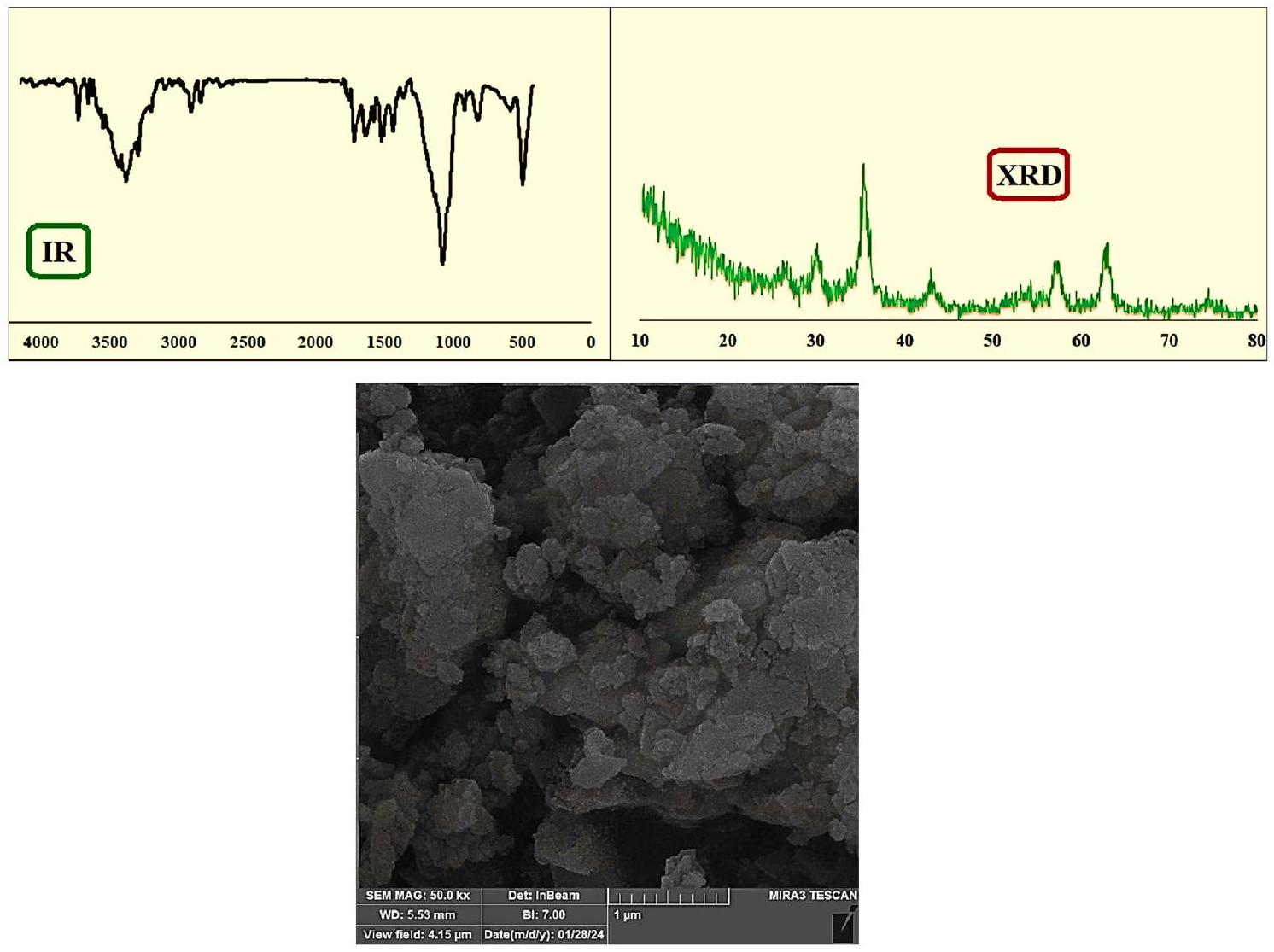
الشكل 10. FE-SEM، أطياف FTIR، وأنماط XRD بعد إعادة التدوير.
توفر البيانات
تتوفر مجموعات البيانات المستخدمة و/أو التي تم تحليلها خلال الدراسة الحالية من المؤلف المراسل عند الطلب المعقول.
تاريخ الاستلام: 17 مايو 2024؛ تاريخ القبول: 22 يوليو 2024
نُشر على الإنترنت: 29 يوليو 2024
نُشر على الإنترنت: 29 يوليو 2024
References
- Venkatesan, K., Sundarababu, J. & Anandan, S. S. The recent developments of green and sustainable chemistry in multidimensional way: Current trends and challenges. Green Chem. Lett. Rev. 17, 2312848 (2024).
- Hoffman, K. C. & Dicks, A. P. Incorporating the United Nations sustainable development goals and green chemistry principles into high school curricula. Green Chem. Lett. Rev. 16, 2185108 (2023).
- Peiman, S., Maleki, B. & Ghani, M.
Mel-Rh-Cu: A high-performance, green catalyst for efficient xanthene synthesis and its application for magnetic solid phase extraction of diazinon followed by its determination through HPLC-UV. Chem. Methodol. 8, 257-278. https://doi.org/10.48309/chemm.2024.442693.1767 (2024). - Azizi, M., Maleki, A. & Hakimpoor, F. Solvent, metal and halogen-free synthesis of sulfoxides by using a recoverable heterogeneous urea-hydrogen peroxide silica-based oxidative catalytic system. Catal. Commun. 100, 62-65 (2017).
- Maleki, A. An efficient magnetic heterogeneous nanocatalyst for the synthesis of pyrazinoporphyrazine macrocycles. Polycycl. Aromat. Compd. 38, 402-409 (2018).
- Maleki, A. & Kari, T. Novel leaking-free, green, double core/shell, palladium-loaded magnetic heterogeneous nanocatalyst for selective aerobic oxidation. Catal. Lett. 148, 2929-2934 (2018).
- Dourandish, Z. et al. Recent advances in electrochemical sensing of anticancer drug doxorubicin: A mini-review. Chem. Methodol. 8, 293-315. https://doi.org/10.48309/chemm.2024.441220.1761 (2024).
- Mittelheisser, V. et al. Evidence and therapeutic implications of biomechanically regulated immunosurveillance in cancer and other diseases. Nat. Nanotechnol. 19, 1-17 (2024).
- Jabar, S. M. & Al-Shammaree, S. A. W. Cytotoxicity and anticancer effect of chitosan-Ag NPs-doxorubicin-folic acid conjugate on lungs cell line. Chem. Methodol. 7, 1-14. https://doi.org/10.22034/chemm.2023.359769.1604 (2023).
- Peiman, S., Baharfar, R. & Maleki, B. Immobilization of trypsin onto polyamidoamine dendrimer functionalized iron oxide nanoparticles and its catalytic behavior towards spirooxindole-pyran derivatives in aqueous media. Mater. Today Commun. 26, 101759 (2021).
- Farajpour, M., Vahdat, S. M., Baghbanian, S. M. & Hatami, M. Ag-SiO
nanoparticles: Benign, expedient, and facile nano catalyst in synthesis of decahydroacridines. Chem. Methodol. 7, 540-551. https://doi.org/10.22034/chemm.2023.386678.1653 (2023). - Eldeeb, B. A., El-Raheem, W. M. A. & Elbeltagi, S. Green synthesis of biocompatible
magnetic nanoparticles using Citrus sinensis peels extract for their biological activities and magnetic-hyperthermia applications. Sci. Rep. 13, 19000 (2023). - Gao, G., Di, J.-Q., Zhang, H.-Y., Mo, L.-P. & Zhang, Z.-H. A magnetic metal organic framework material as a highly efficient and recyclable catalyst for synthesis of cyclohexenone derivatives. J. Catal. 387, 39-46 (2020).
- Zhang, M., Liu, Y.-H., Shang, Z.-R., Hu, H.-C. & Zhang, Z.-H. Supported molybdenum on graphene oxide/
: An efficient, magnetically separable catalyst for one-pot construction of spiro-oxindole dihydropyridines in deep eutectic solvent under microwave irradiation. Catal. Commun. 88, 39-44 (2017). - Chen, M.-N., Mo, L.-P., Cui, Z.-S. & Zhang, Z.-H. Magnetic nanocatalysts: Synthesis and application in multicomponent reactions. Curr. Opin. Green Sustain. Chem. 15, 27-37 (2019).
- Maleki, A. Synthesis of imidazo [1,2-a] pyridines using
@ as an efficient nanomagnetic catalyst via a one-pot multicomponent reaction. Helv. Chim. Acta 97, 587-593 (2014). - Baharfar, R., Peiman, S. & Maleki, B.
@ @ D-NHCS-Tr as an efficient and reusable catalyst for the synthesis of indol-3-yl-4 H-chromene via a multi-component reaction under solvent-free conditions. J. Heterocycl. Chem. 58, 1302-1310 (2021). - Peiman, S., Baharfar, R. & Hosseinzadeh, R. CuI NPs immobilized on a ternary hybrid system of magnetic nanosilica, PAMAM dendrimer and trypsin, as an efficient catalyst for
-coupling reaction. Res. Chem. Intermed. 48, 1365-1382 (2022). - Maleki, A., Rahimi, R. & Maleki, S. Efficient oxidation and epoxidation using a chromium (VI)-based magnetic nanocomposite. Environ. Chem. Lett. 14, 195-199 (2016).
- Suetsuna, T., Suenaga, S., Takahashi, T. & Harada, K. Synthesis of self-forming core/shell nanoparticles of magnetic metal/nonmagnetic oxide. Acta Mater. 78, 320-327 (2014).
- Zhao, F. et al. Synthesis of
-zeolite materials and application to the adsorption of gallium and indium. J. Chem. Eng. Data 60, 1338-1344 (2015). - Wang, Y.-M. et al. Molybdenum disulfide-catalyzed direct
-hydroxymethylation of amides employing methanol as a sustainable C1 source under photoirradiation. J. Catal. 427, 115100 (2023). - Naghizadeh, M., Taher, M. A., Tamaddon, A.-M., Borandeh, S. & Abolmaali, S. S. Microextraction of gadolinium MRI contrast agent using core-shell
@ SiO nanoparticles: Optimization of adsorption conditions and in-vitro study. Environ. Nanotechnol. Monit. Manag. 12, 100250 (2019). - Hasani, M. & Ghods, M. M-polynomials and topological indices of porphyrin-cored dendrimers. Chem. Methodol. 7, 288-306. https://doi.org/10.22034/chemm.2023.370497.1626 (2023).
- Bodaghifard, M. A., Allahbakhshi, H. & Ahangarani-Farahani, R. Efficient synthesis of benzoacridines and indenoquinolines catalyzed by acidic magnetic dendrimer. Sci. Rep. 14, 8736 (2024).
- Shailey Singhal, S. S., Shefali Arora, S. A., Shilpi Agarwal, S. A., Rajan Sharma, R. S. & Naveen Singhal, N. S. A review on potential biological activities of thiosemicarbazides. World J. Pharm. Pharm. Sci. 6, 4661 (2013).
- Arora, S., Agarwal, S. & Singhal, S. Anticancer activities of thiosemicarbazides/thiosemicarbazones: A review. Int. J. Pharm. Pharm. Sci. 6, 34 (2014).
- El-Atawy, M. A., Omar, A. Z., Hagar, M. & Shashira, E. M. Transalkylidation reaction: Green, catalyst-free synthesis of thiosemicarbazones and solving the NMR conflict between their acyclic structure and intramolecular cycloaddition products. Green Chem. Lett. Rev. 12, 364-376 (2019).
- Azizi, M., Maleki, A., Hakimpoor, F., Ghalavand, R. & Garavand, A. A mild, efficient and highly selective oxidation of sulfides to sulfoxides catalyzed by lewis acid-urea-hydrogen peroxide complex at room temperature. Catal. Lett. 147, 2173-2177 (2017).
- Alipour, A. & Naeimi, H. Design, fabrication and characterization of magnetic nickel copper ferrite nanocomposites and their application as a reusable nanocatalyst for sonochemical synthesis of 14-aryl-14-H-dibenzo [a, j] xanthene derivatives. Res. Chem. Intermed. 49, 2705-2723 (2023).
- Zare, A. & Mostaghar, F. Construction of a novel magnetic nanomaterial, and its utility as an effectual catalyst for the fabrication of 1, 8-dioxo-octahydroxanthenes. Chem. Methodol. 8, 23-36. https://doi.org/10.48309/chemm.2024.422175.1733 (2023).
- Azizi, N., Farzaneh, F. & Farhadi, E. Streamlining efficient and selective synthesis of benzoxanthenones and xanthenes with dual catalysts on a single support. Sci. Rep. 13, 16469 (2023).
- Ardeshirfard, H. & Elhamifar, D. Magnetic cobalt oxide supported organosilica-sulfonic acid as a powerful nanocatalyst for the synthesis of tetrahydrobenzo [a] xanthen-11-ones. Sci. Rep. 13, 14134 (2023).
- Mohammadi Ziarani, G. et al. Convenient one-pot synthesis of spirooxindole-4H-pyrans in the presence of SBA-Pr-NH2 and evaluation of their urease inhibitory activities. J. Nanostruct. 2, 489-500 (2012).
- Maghsoodlou, M. T., Heydari, R., Mohamadpour, F. & Lashkari, M.
as an environmentally benign natural catalyst for onepot and solvent-free synthesis of spiro-4H-pyran derivatives. Iran. J. Chem. Chem. Eng. IJCCE 36, 31-38 (2017). - Tufail, F. et al. A practical green approach to diversified spirochromene/spiropyran scaffolds via a glucose-water synergy driven organocatalytic system. New J. Chem. 42, 17279-17290 (2018).
- Nasri, S., Bayat, M. & Miankooshki, F. R. Synthesis of diverse spiro-imidazo pyridine-indene derivatives via acid-promoted annulation reaction of bindone and heterocyclic ketene aminals. Sci. Rep. 12, 12550 (2022).
- Naderi, S., Sandaroos, R., Peiman, S. & Maleki, B. Novel crowned cobalt (II) complex containing an ionic liquid: A green and efficient catalyst for the one-pot synthesis of chromene and xanthene derivatives starting from benzylic alcohols. J. Phys. Chem. Solids 180, 111459 (2023).
- Darvishy, S., Alinezhad, H., Vafaeezadeh, M., Peiman, S. & Maleki, B. S-(+) Camphorsulfonic acid glycine (CSAG) as surfactantlikes brønsted acidic ionic liquid for one-pot synthesis of
-amino carbonyl. Polycycl. Aromat. Compd. https://doi.org/10.1080/ 10406638.2022.2094419 (2022). - Sandaroos, R., Maleki, B., Naderi, S. & Peiman, S. Efficient synthesis of sulfones and sulfoxides from sulfides by cobalt-based Schiff complex supported on nanocellulose as catalyst and Oxone as the terminal oxidant. Inorg. Chem. Commun. 148, 110294 (2023).
- Boroumand, H., Alinezhad, H., Maleki, B. & Peiman, S. Triethylenetetramine-grafted magnetic graphene oxide (
) as a reusable heterogeneous catalyst for the one-pot synthesis of 2-amino-4 H-benzopyran derivatives. Polycycl. Aromat. Compd. 43, 7853-7869 (2023). - Maleki, B., Sandaroos, R., Naderi, S. & Peiman, S. A crowned manganese-based Schiff complex supported on nanocellulose as an efficient and sustainable heterogeneous catalyst for the oxidation of benzyl alcohols. J. Organometall. Chem. 990, 122666 (2023).
- Naderi, S., Sandaroos, R., Peiman, S. & Maleki, B. Synthesis and characterization of a novel crowned schiff base ligand linked to ionic liquid and application of its
complex in the epoxidation of olefins. Chem. Methodol. 7, 392-404 (2023). - Maleki, B., Sandaroos, R. & Peiman, S. Mn(III) Schiff base complexes containing crown ether rings immobilized onto MCM-41 matrix as heterogeneous catalysts for oxidation of alkenes. Heliyon 9, e15041 (2023).
- Maleki, B., Jamshidi, A., Peiman, S. & Housaindokht, M. R. Tri-vanadium substituted dawson-type heteropolytungstate nanocomposite (
) as a novel, green, and recyclable nanomagnetic catalyst in the synthesis of tetrahydrobenzo [b] pyrans. Polycycl. Aromat. Compd. 44, 994-1010 (2024). - Bhale, P. S., Dongare, S. B. & Mule, Y. B. An efficient synthesis of 1, 8-dioxooctahydroxanthenes catalysed by thiourea dioxide (TUD) in aqueous media. Chem. Sci. Trans. 4, 246-250 (2015).
- Gong, K., Fang, D., Wang, H.-L., Zhou, X.-L. & Liu, Z.-L. The one-pot synthesis of 14-alkyl-or aryl-14H-dibenzo [a, j] xanthenes catalyzed by task-specific ionic liquid. Dyes pigments 80, 30-33 (2009).
- Mir, E., Hazeri, N., Faroughi Niya, H. & Fatahpour, M. Synthesis, identification and application of
@ THAM-mercaptopyrimidine nanoparticles as a novel and highly recyclable nanocatalyst in one-pot multicomponent synthesis of 1, 8-dioxooctahydroxanthenes and polyhydroquinolines. Res. Chem. Intermed. 49, 1439-1462 (2023). - Kundu, K. & Nayak, S. K. Camphor-10-sulfonic acid catalyzed condensation of 2-naphthol with aromatic/aliphatic aldehydes to 14-aryl/alkyl-14H-dibenzo [a, j] xanthenes. J. Serb. Chem. Soc. 79, 1051-1058 (2014).
- Rekunge, D. S., Khatri, C. K. & Chaturbhuj, G. U. Rapid and efficient protocol for Willgerodt-Kindler’s thioacetamides catalyzed by sulfated polyborate. Mon. Chem. Chem. Mon. 148, 2091-2095 (2017).
- Mohammadi, R., Eidi, E., Ghavami, M. & Kassaee, M. Z. Chitosan synergistically enhanced by successive
and silver nanoparticles as a novel green catalyst in one-pot, three-component synthesis of tetrahydrobenzo xanthene-11-ones. J. Mol. Catal. A Chem. 393, 309-316 (2014). - Mane, P. et al. Sodium acetate/MWI: A green protocol for the synthesis of tetrahydrobenzo
xanthen-11-ones with biological screening. Res. Chem. Intermed. 46, 231-241 (2020). - Zhang, M. et al. Catalyst-free, visible-light promoted one-pot synthesis of spirooxindole-pyran derivatives in aqueous ethyl lactate. ACS Sustain. Chem. Eng. 5, 6175-6182 (2017).
- Langroudi, J. M., Mazloumi, M., Nahzomi, H. T., Shirini, F. & Tajik, H. Tropine-based dicationic molten salt: An active catalyst in the acceleration of one-pot synthesis of spiro- 2 -amino- 4 H -pyran-oxindoles and bis- 2 -amino- 4 H -pyrans. J. Mol. Struct. 1274, 134410 (2023).
- Guo, R.-Y. et al. Meglumine: A novel and efficient catalyst for one-pot, three-component combinatorial synthesis of functionalized 2-amino-4 H-pyrans. ACS Comb. Sci. 15, 557-563 (2013).
- Umar Basha, K. N. & Gnanamani, S. An efficient and easy method for the one-pot synthesis of spirooxindoles in the presence of
. J. Heterocycl. Chem. 56, 2008-2016 (2019). - Li, Y., Chen, H., Shi, C., Shi, D. & Ji, S. Efficient one-pot synthesis of spirooxindole derivatives catalyzed by l-proline in aqueous medium. J. Comb. Chem. 12, 231-237 (2010).
- Goli-Jolodar, O., Shirini, F. & Seddighi, M. Introduction of a novel basic ionic liquid containing dual basic functional groups for the efficient synthesis of spiro-4H-pyrans. J. Mol. Liq. 224, 1092-1101 (2016).
- Raheja, B. K. & Dalal, D. S. Ammonium acetate mediated simple, rapid, and one-pot multicomponent synthesis of spirooxindole derivatives. Synth. Commun. 53, 808-822 (2023).
- Chandam, D. R., Mulik, A. G., Patil, D. R. & Deshmukh, M. B. Oxalic acid dihydrate: Proline as a new recyclable designer solvent: A sustainable, green avenue for the synthesis of spirooxindole. Res. Chem. Intermed. 42, 1411-1423 (2016).
- Thongni, A. et al. Ultrasound assisted synthesis of spirooxindole analogs catalyzed by
@ PPCA NPs: Experimental, theoretical and in vitro biological studies. J. Mol. Struct. 1284, 135363 (2023). - Pan, F.-F., Yu, W., Qi, Z.-H., Qiao, C. & Wang, X.-W. Efficient construction of chiral spiro [benzo [g] chromene-oxindole] derivatives via organocatalytic asymmetric cascade cyclization. Synthesis 46, 1143-1156 (2014).
- Zhao, H. W. et al. Highly enantioselective synthesis of chiral pyranonaphthoquinone-fused spirooxindoles through organocatalytic three-component cascade reactions. Eur. J. Org. Chem. 2015, 3320-3326 (2015).
- Kumar, C. N. S. S. P., Srinivas, C., Sadhu, P. S., Rao, V. J. & Palaniappan, S. Efficient synthesis of 14-substituted-14-H-dibenzo [a, j] xanthenes using silica supported sodium hydrogen sulfate or amberlyst-15 catalyst. J. Heterocycl. Chem. 46, 997-999 (2009).
- Liu, Y.-H., Tao, X.-Y., Lei, L.-Q. & Zhang, Z.-H. Fluoroboric acid adsorbed on silica-gel-catalyzed synthesis of 14-aryl-14 H-dibenzo [
] xanthene derivatives. Synth. Commun. 39, 580-589 (2009). - Alireza, G. M. Z. N. L. Sulfonic acid-functionalized mesoporous silica. Gen 466, 116 (2013).
- Yue, X. et al. High acidity cellulose sulfuric acid from sulfur trioxide: A highly efficient catalyst for the one step synthesis of xanthene and dihydroquinazolinone derivatives. RSC Adv. 9, 28718-28723 (2019).
- Wu, L., Yang, C., Yang, L. & Yang, L. Synthesis of 14 -substituted-14 H-dibenzo [a, j] xanthenes and 1, 8-dioxo-octahydroxanthenes using silica chloride (
) under solvent-free conditions. Phosphorus Sulfur Silicon 185, 903-909 (2010). - Mohamadpour,
as an efficient and environmentally benign natural catalyst for facile and solvent-free synthesis of xanthene derivatives. J. Appl. Chem. Res. 13, 66-80 (2019). - Tayebee, R. & Tizabi, S. Highly efficient and environmentally friendly preparation of 14 -aryl-14H dibenzo [ a , j ] xanthenes catalyzed by tungsto-divanado-phosphoric acid. Chin. J. Catal. 33, 962-969 (2012).
- Nemati, R., Elhamifar, D., Zarnegaryan, A. & Shaker, M. Magnetic silica nanocomposite supported
amine: A powerful catalyst for the synthesis of biologically active spirooxindole-pyrans. Inorg. Chem. Commun. 145, 109934 (2022). - Amini Moqadam, Z., Allahresani, A. & Hassani, H. An efficiently and quickly synthesized NiO@g-C3
nanocomposite-catalyzed green synthesis of spirooxindole derivatives. Res. Chem. Intermed. 46, 299-311 (2020). - Karmakar, B., Nayak, A. & Banerji, J. A clean and expedient synthesis of spirooxindoles in aqueous media catalyzed over nanocrystalline MgO. Tetrahedron Lett. 53, 5004-5007 (2012).
- Hojati, S. F., Amiri, A. & Mahamed, M. Polystyrene@graphene oxide-
as a novel and magnetically recyclable nanocatalyst for the efficient multi-component synthesis of spiro indene derivatives. Res. Chem. Intermed. 46, 1091-1107 (2020). - Sadeghi, B., Ghasemi Pirbaluti, M., Farokhi Nezhad, P. & Abbasi Nezhad, R. A clean and expedient synthesis of spirooxindoles catalyzed by silica-sulfuric acid nanoparticles as an efficient and reusable reagent. Res. Chem. Intermed. 41, 4047-4055 (2015).
شكر وتقدير
تم دعم هذه الدراسة من خلال منحة بحثية (رقم 33/38554) من جامعة مازندران.
مساهمات المؤلفين
الكتابة: س.ب.; ب.م. التصور: س.ب.; ب.م. تنظيم البيانات: س.ب.; ب.م. التحليل الرسمي: س.ب.; ب.م. إدارة المشروع: س.ب.; ب.م. المنهجية: س.ب.; ب.م. التحقق: س.ب.; ب.م. المراجعة والتحرير: س.ب.; ب.م. جميع المؤلفين راجعوا المخطوطة.
المصالح المتنافسة
يعلن المؤلفون عدم وجود مصالح متنافسة.
معلومات إضافية
يجب توجيه المراسلات والطلبات للحصول على المواد إلى ب.م.
معلومات إعادة الطباعة والتصاريح متاحة علىwww.nature.com/reprints.
ملاحظة الناشر: تظل شركة سبرينجر ناتشر محايدة فيما يتعلق بالمطالبات القضائية في الخرائط المنشورة والانتماءات المؤسسية.
معلومات إعادة الطباعة والتصاريح متاحة علىwww.nature.com/reprints.
ملاحظة الناشر: تظل شركة سبرينجر ناتشر محايدة فيما يتعلق بالمطالبات القضائية في الخرائط المنشورة والانتماءات المؤسسية.
الوصول المفتوح هذه المقالة مرخصة بموجب رخصة المشاع الإبداعي النسبية – غير التجارية – بدون مشتقات 4.0 الدولية، التي تسمح بأي استخدام غير تجاري، ومشاركة، وتوزيع، واستنساخ في أي وسيلة أو صيغة، طالما أنك تعطي الائتمان المناسب للمؤلفين الأصليين والمصدر، وتوفر رابطًا لرخصة المشاع الإبداعي، وتوضح إذا قمت بتعديل المادة المرخصة. ليس لديك إذن بموجب هذه الرخصة لمشاركة المواد المعدلة المشتقة من هذه المقالة أو أجزاء منها. الصور أو المواد الأخرى من طرف ثالث في هذه المقالة مشمولة في رخصة المشاع الإبداعي الخاصة بالمقالة، ما لم يُشار إلى خلاف ذلك في سطر الائتمان للمادة. إذا لم تكن المادة مشمولة في رخصة المشاع الإبداعي الخاصة بالمقالة وكان استخدامك المقصود غير مسموح به بموجب اللوائح القانونية أو يتجاوز الاستخدام المسموح به، فستحتاج إلى الحصول على إذن مباشرة من صاحب حقوق الطبع والنشر. لعرض نسخة من هذه الرخصة، قم بزيارةhttp://creativecommons.org/licenses/by-nc-nd/4.0/.
© المؤلف(ون) 2024
© المؤلف(ون) 2024
- قسم الكيمياء العضوية، كلية الكيمياء، جامعة مازندران، صندوق بريد 47416-95447، بابلسر، إيران.
البريد الإلكتروني:b.maleki@umz.ac.ir
Journal: Scientific Reports, Volume: 14, Issue: 1
DOI: https://doi.org/10.1038/s41598-024-68316-8
PMID: https://pubmed.ncbi.nlm.nih.gov/39075155
Publication Date: 2024-07-29
DOI: https://doi.org/10.1038/s41598-024-68316-8
PMID: https://pubmed.ncbi.nlm.nih.gov/39075155
Publication Date: 2024-07-29
scientific reports
Keywords Green chemistry, Magnetic nanoparticles, Dendrimer, Spirooxindole-pyran, Xanthene
The emphasis on advanced and green chemistry in trendy organic synthesis has increased significantly in the past few years, such as not utilizing hazardous or harmful reagents and solvents, using recyclable and inexpensive catalysts, and avoiding inappropriate reaction conditions. Through the years, there has been a growing interest in the use of environmentally friendly reagents or solvents, acceptable atom economy, and optimizing organic synthesis conditions to minimize energy consumption
The emphasis on advanced and green chemistry in trendy organic synthesis has increased significantly in the past few years, such as not utilizing hazardous or harmful reagents and solvents, using recyclable and inexpensive catalysts, and avoiding inappropriate reaction conditions. Through the years, there has been a growing interest in the use of environmentally friendly reagents or solvents, acceptable atom economy, and optimizing organic synthesis conditions to minimize energy consumption
Today, one of the greatest challenges in the industry or organic developments is finding ways to utilize clean and sustainable chemical technologies to produce beneficial chemicals. Including methods to achieve this important goal is to use stable catalysts that work in the green chemistry. Researchers’ investigation indicates that the use of heterogeneous catalysts in chemical industrial processes has gained a special place. These catalysts are environmentally friendly and help produce sustainable fuels and many essential chemicals
Nanotechnology is one of the most important parts of modern scientific fields. Nanoscience allows scientists in various fields like medicine, engineering, and chemistry to achieve significant progress in line with their goals at the molecular and cellular levels. In recent years, due to their unique size and high surface area, magnetic nanoparticles have found special applications in industry and the biological sciences, such as gene therapy, drug delivery, information storage, sensors, etc
Magnetic nanoparticles have been considered due to special features such as low toxicity, compatibility with the environment, cheapness of the surface that can be changed with different groups, and easy magnetic removal
attention in studies
Dendrimers, which are a type of branched polymer composed of repeating units that extend outward from a central core, have gained popularity. Significant attention because of their high geometric symmetry controllable, molecular weight, and well-defined molecular structure. In addition to their water solubility, multivalency, and entrapment of hydrophilic drug molecules, dendrimers have been referred to as polymeric drug delivery systems
Thiosemicarbazide is a beneficial structural component that has the potential to perform chemical functions in biologically active molecules, and further investigation of this structure can lead to the discovery of a basis for a novel type of therapeutic agent. Research shows that their derivatives have antibacterial, anti-tumor, antifungal, and anti-seizure activities. On the other hand, they are also considered good antioxidants (Fig. 1). They are a special group of organic compounds that is known not only for its diverse biological activities but also as a metal chelating and anti-corrosion agent
Xanthenes are heterocyclic compounds. This group of organic compounds has a vast array of biological and medicinal properties, including anti-cancer, photodynamic therapy, antibacterial, antiviral, and anti-inflammatory
Based on our previous research on the synthesis of catalysts and their application
Experimental
All chemicals were purchased from Merck and Sigma Aldrich and used without purification. X-ray diffraction (XRD) patterns were obtained using the Philips PW-1830. The Electro thermal 9100 apparatus was used to determine of melting points. Magnetic analysis curves were recorded using the VSM model MDKB from Danesh Pajohan Kavir Co. Kashan, Iran. The FT-IR Spectra were detected using the Shimadzu IR-470 spectrophotometer. The
Preparation of
The synthetic steps of

Figure 1. Some thiosemicarbazide structures have biological properties.

Figure 2. Biologically active compounds with xanthene and spirooxindole skeletons.
Preparation of
1 g of the nanoparticle from the previous step was subjected to ultrasonic waves in dry THF ( 40 ml ). In the next step, cyanuric chloride (TCT) ( 0.5 g ) and
Preparation of
1 g of
Preparation of
1 g of
Preparation of
General procedure for the synthesis of xanthenes
A mixture of dimedone ( 2 mmol ), and/or
General procedure for the synthesis of spirooxindole-pyran derivatives (10a-t)
1 mmol of isatins, 1 mmol of malononitrile, 1 mmol of 1,3 -dicarbonyl compounds, and

Scheme 1. Preparation of
Spectral data for selected products
Compound
Compound
Compound (5a)
Compound (5c)
Compound (5f)

Scheme 2. Preparation of xanthenes in the presence of

Scheme 3. Preparation of spirooxindole-pyran derivatives in the presence of
Compound (6b)
Compound (6d)
Compound (10a)
Compound ( 10 f)
Compound (10m)
Compound (10o)
Compound (10l)
Ethical approval
This work does not contain any studies with human participants or animals performed by any of the authors.
Results and discussions
A rational design aimed at preparing a novel high-performance and recyclable dendrimer-templated nanocatalyst containing thiosemicarbazide is brought up (Scheme 1). First, magnetic nanoparticles were synthesized using the co-precipitation method, then they were covered with a coating of silica to protect and achieve a modifiable surface with spherical morphology. In the following step, the surface was modified with APTES, and after that, 1, 3-dibromopropane, cyanuric chloride, melamine, and thiosemicarbazide were placed in the last step. Then Cu metal was placed in suitable conditions to perform the preparation of xanthene and spirooxindole-pyran derivative reactions.
Functional groups in the catalyst synthesis periods were checked using FT-IR spectroscopy (Fig. 3). The peak in the region of

Figure 3. FT-IR synthesis steps of
thiosemicarbazide covalent binding of carbazide with IR absorption bands of 3177,3264 , and
The crystallinity of
The thermal stability of

Figure 4. XRD patterns of the

Figure 5. TGA thermograms of (A)

Figure 6. FE-SEM images of

Figure 7. TEM images of
TEM and FE-SEM morphological examination shows that magnetic nanoparticles. By placing the silica layer and immobilizing the ligands on the substrate, they have a spherical structure with an average particle size of 25.5 nm. TEM images of
The magnetic behavior of
In this manuscript, we have sought to utilize the fundamental property of copper metal on a dendrimer. Considering the advantages of employing heterogeneous catalytic systems, the synthesis of these systems is of great importance. To achieve this goal, it was necessary to select a suitable support and ligands for the desired outcome. Nano silica presents itself as an appropriate option due to the presence of suitable functional groups on its surface. After that, cyanuric chloride, followed by melamine and thiosemicarbazide were used to produce dendrimer template multi-branched grafts. Lastly, the copper metal complex was formed with the aid of the atoms in thiosemicarbazide. Moreover, for the purpose of facilitating the separation and reusability of the catalyst, the nanocatalyst was magnetized. This allowed for easy separation from the reaction environment through the use of an external magnetic field, enabling reusability in subsequent steps.
The synthesis reaction of xanthenes, and spirooxindole-pyrans in the presence of
To detect the optimal conditions for synthesizing xanthenes, the reaction of
After determining the optimal conditions, the catalyst’s performance was assessed. Employing the reaction of aryl aldehydes,
Following that, to determine the optimal conditions in the synthesis of spirooxindole-pyran derivatives, malonitrile ( 1 mmol ), dimedone ( 1 mmol ), and isatin ( 1 mmol ) were selected as model reactions. First, the reaction in the adjacency of

Figure 8. VSM spectra of
| Entry | Catalyst (mg) | Solvent | Temp (
|
Time (min) | Yield (%) |
| 1 |
|
EtOH | 25 | 12 | 85 |
| 2 |
|
|
25 | 12 | 60 |
| 3 |
|
|
25 | 12 | 75 |
| 4 |
|
|
25 | 12 | 80 |
| 5 |
|
Solvent-free | 25 | 12 | 97 |
| 6 |
|
Solvent-free | 40 | 12 | 97 |
| 7 |
|
Solvent-free | 60 | 12 | 97 |
| 8 |
|
Solvent-free | 25 | 12 | 90 |
| 9 |
|
Solvent-free | 25 | 12 | 97 |
| 10 |
|
Solvent-free | 25 | 12 | 97 |
| 11 |
|
Solvent-free | 25 | 12 | 97 |
| 12 | – | Solvent-free | 25 | 12 | Trace |
Table 1. Synthesis xanthenes using
entries 8-10). The model reaction was not efficient in the absence of the catalyst, and in the presence of
To expand the reaction scope, we operated
In the previous literature, numerous catalysts have been used in the synthesis of xanthene and spirooxindolepyran derivatives. In continuation, the performance of the synthesized catalyst was assessed by comparing it to other catalysts in model reactions (Table 5). As shown,
The synthetic mechanism of xanthenes and spirooxindole-pyran derivatives is given in Schemes 4 and 5.
Synthetic mechanism of xanthene derivatives: At first, by activating the carbonyl group, the catalyst makes aldehydes more sensitive to nucleophilic attack by dimedone to form intermediate (A), in the next step, another molecule of dimedone is added by Michael to form intermediate (B). By eliminating
Synthetic mechanism of xanthene derivatives: At first, by activating the carbonyl group, the catalyst makes aldehydes more sensitive to nucleophilic attack by dimedone to form intermediate (A), in the next step, another molecule of dimedone is added by Michael to form intermediate (B). By eliminating
The possible route for synthesizing spirooxindole-pyran in the presence of
Recycling of catalyst
One of the major challenges faced by chemists involved in catalyst synthesis is to ensure that the catalysts can be reused. Therefore, researching about this great issue is inevitable. In this experiment, after separating the catalyst, we washed it with EtOH and dried it for reuse. Studies have shown that at least eight steps can be performed using this catalyst without much change in performance (Fig. 9). Also, for further study, FE-SEM image, FT-IR spectrum, and XRD patterns have been checked after 8 recycling cycles, which do not show any significant difference. (Fig. 10).
Examination of the possible leaching of copper nanoparticles from the nanocatalyst on the model reactions was also analyzed. The consequences of ICP-OES analysis indicated that the amount of Cu leaching in the catalyst after 7 recycling steps is
Conclusion
In order to create green nanocatalysts that are high-performing, environmentally friendly, reusable, and recyclable for a minimum of 8 consecutive cycles without a considerable loss of activity, we have successfully synthesized a novel and stable pseudo-dendrimeric magnetic core-shell catalyst. The catalyst was identified using different analytical methods. The performance of
| Entry | Product | Time (min) | Yield (%) | MP
|
||
| 1 |
|
12 | 97 |
|
||
| 2 |
|
10 | 98 | 232-233
|
||
| 3 |
|
15 | 98 |
|
||
| 4 |
|
20 | 92 | 229-230
|
||
| 5 |
|
20 | 94 |
|
||
| Continued | ||||||
| Entry | Product | Time (min) | Yield (%) | MP
|
||
| 6 |
|
25 | 96 |
|
||
| 7 |
|
20 | 96 | 286-287
|
||
| 8 |
|
60 | 92 |
|
||
| 9 |
|
50 | 92 | 151-152
|
||
| 10 |
|
12 | 96 |
|
||
| Continued | ||||||
| Entry | Product | Time (min) | Yield (%) | MP
|
||
| 11 |
|
10 | 98 |
|
||
| 12 |
|
10 | 96 |
|
||
| 13 |
|
10 | 96 |
|
||
| 14 |
|
10 | 96 | 316-318
|
||
| Continued |
| Entry | Product | Time (min) | Yield (%) | MP
|
||
| 15 |
|
15 | 92 | 220-221
|
||
| 16 |
|
15 | 90 | 202-204
|
||
| 17 |
|
20 | 90 |
|
||
| 18 |
|
20 | 98 | 176-177
|
||
| Continued | ||||||
| Entry | Product | Time (min) | Yield (%) | MP
|
||
| 19 |
|
20 | 96 | 199-201
|
||
| 20 |
|
20 | 96 |
|
||
| 21 |
|
22 | 88 |
|
||
| 22 |
|
90 | 80 |
|
Table 2. Synthesis of derivatives 4a-f, 5a-f and 6a-d by
| Entry | Catalyst (mg) | Solvent | Temp (
|
Time (min) | Yield (%) |
| 1 |
|
EtOH | 25 | 4 | 98 |
| 2 |
|
THF | 25 | 4 | 75 |
| 3 |
|
|
25 | 4 | 65 |
| 4 |
|
|
25 | 4 | 95 |
| 5 |
|
Solvent-free | 25 | 4 | 98 |
| 6 |
|
Solvent-free | 40 | 4 | 98 |
| 7 |
|
Solvent-free | 60 | 4 | 98 |
| 8 |
|
Solvent-free | 25 | 4 | 92 |
| 9 |
|
Solvent-free | 25 | 4 | 98 |
| 10 |
|
Solvent-free | 25 | 4 | 98 |
| 11 |
|
Solvent-free | 25 | 4 | 30 |
| 12 |
|
Solvent-free | 25 | 4 | 88 |
| 13 | – | Solvent-free | 25 | 4 | – |
Table 3. Synthesis spirooxindole-pyran using
| Entry | Product | Time (min) | Yield (%) |
|
| 1 | 10 a | 12 | 97 |
|
| 2 | 10 b | 10 | 98 |
|
| 3 | 10 c | 15 | 98 |
|
| 4 | 10 d | 20 | 92 |
|
| Continued |
| Entry | Product | Time (min) | Yield (%) | MP
|
||
| 5 | 10 e | 20 | 94 | 229-230
|
||
| 6 | 10 f | 25 | 96 |
|
||
| 7 | 10 g | 20 | 96 |
|
||
| 8 | 10 h | 12 | 96 |
|
||
| 9 |
|
10 | 98 |
|
||
| Continued |
| Entry | Product | Time (min) | Yield (%) |
|
| 10 | 10 j | 10 | 96 |
|
| 11 | 10 k | 10 | 96 |
|
| 12 | 101 | 10 | 96 |
|
| 13 | 10 m | 15 | 92 |
|
| 14 | 10 n | 15 | 90 |
|
| Continued |
| Entry | Product | Time (min) | Yield (%) | MP
|
| 15 | 100 | 20 | 90 |
|
| 16 | 10 p | 20 | 98 |
|
| 17 | 10 q | 20 | 96 |
|
| 18 | 10 r | 20 | 96 |
|
Table 4. Synthesis spirooxindole-pyran by
| Sample | Conditions | Time | Yield (%) |
 |
This research/solvent free/
|
12 min | 98 |
| Amberlyst-15/
|
2 | 93 | |
| Silica-supported
|
h | 98 | |
| SBA-15/
|
30 min | 95 | |
| Cellulose sulphate/no solvent/
|
24 h | 97 | |
|
|
1 h | 93 | |
| Potassium aluminum sulfate
|
3 h | 90 | |
|
|
3 h | 98 | |
| This research /solvent free
|
4 min | 98 | |
| L-proline /
|
20 min | 94 | |
|
|
120 min | 95 | |
|
|
20 min | 95 | |
| Magnesia
|
120 min | 95 | |
| PSGO-
|
120 min | 96 | |
| Silica sulfuric acid NPs/EtOH/80
|
30 min | 96 |
Table 5. Catalyst comparison of

Scheme 4. Synthetic mechanism of xanthene derivatives.

Scheme 5. Synthetic mechanism of spirooxindole-pyran derivatives.

Figure 9. Recyclability of the catalyst in xanthene and spirooxindole-pyran synthesis model reaction.

Figure 10. FE-SEM, FTIR spectra, and XRD patterns after recycling.
Data availability
The datasets used and/or analysed during the current study available from the corresponding author on reasonable request.
Received: 17 May 2024; Accepted: 22 July 2024
Published online: 29 July 2024
Published online: 29 July 2024
References
- Venkatesan, K., Sundarababu, J. & Anandan, S. S. The recent developments of green and sustainable chemistry in multidimensional way: Current trends and challenges. Green Chem. Lett. Rev. 17, 2312848 (2024).
- Hoffman, K. C. & Dicks, A. P. Incorporating the United Nations sustainable development goals and green chemistry principles into high school curricula. Green Chem. Lett. Rev. 16, 2185108 (2023).
- Peiman, S., Maleki, B. & Ghani, M.
Mel-Rh-Cu: A high-performance, green catalyst for efficient xanthene synthesis and its application for magnetic solid phase extraction of diazinon followed by its determination through HPLC-UV. Chem. Methodol. 8, 257-278. https://doi.org/10.48309/chemm.2024.442693.1767 (2024). - Azizi, M., Maleki, A. & Hakimpoor, F. Solvent, metal and halogen-free synthesis of sulfoxides by using a recoverable heterogeneous urea-hydrogen peroxide silica-based oxidative catalytic system. Catal. Commun. 100, 62-65 (2017).
- Maleki, A. An efficient magnetic heterogeneous nanocatalyst for the synthesis of pyrazinoporphyrazine macrocycles. Polycycl. Aromat. Compd. 38, 402-409 (2018).
- Maleki, A. & Kari, T. Novel leaking-free, green, double core/shell, palladium-loaded magnetic heterogeneous nanocatalyst for selective aerobic oxidation. Catal. Lett. 148, 2929-2934 (2018).
- Dourandish, Z. et al. Recent advances in electrochemical sensing of anticancer drug doxorubicin: A mini-review. Chem. Methodol. 8, 293-315. https://doi.org/10.48309/chemm.2024.441220.1761 (2024).
- Mittelheisser, V. et al. Evidence and therapeutic implications of biomechanically regulated immunosurveillance in cancer and other diseases. Nat. Nanotechnol. 19, 1-17 (2024).
- Jabar, S. M. & Al-Shammaree, S. A. W. Cytotoxicity and anticancer effect of chitosan-Ag NPs-doxorubicin-folic acid conjugate on lungs cell line. Chem. Methodol. 7, 1-14. https://doi.org/10.22034/chemm.2023.359769.1604 (2023).
- Peiman, S., Baharfar, R. & Maleki, B. Immobilization of trypsin onto polyamidoamine dendrimer functionalized iron oxide nanoparticles and its catalytic behavior towards spirooxindole-pyran derivatives in aqueous media. Mater. Today Commun. 26, 101759 (2021).
- Farajpour, M., Vahdat, S. M., Baghbanian, S. M. & Hatami, M. Ag-SiO
nanoparticles: Benign, expedient, and facile nano catalyst in synthesis of decahydroacridines. Chem. Methodol. 7, 540-551. https://doi.org/10.22034/chemm.2023.386678.1653 (2023). - Eldeeb, B. A., El-Raheem, W. M. A. & Elbeltagi, S. Green synthesis of biocompatible
magnetic nanoparticles using Citrus sinensis peels extract for their biological activities and magnetic-hyperthermia applications. Sci. Rep. 13, 19000 (2023). - Gao, G., Di, J.-Q., Zhang, H.-Y., Mo, L.-P. & Zhang, Z.-H. A magnetic metal organic framework material as a highly efficient and recyclable catalyst for synthesis of cyclohexenone derivatives. J. Catal. 387, 39-46 (2020).
- Zhang, M., Liu, Y.-H., Shang, Z.-R., Hu, H.-C. & Zhang, Z.-H. Supported molybdenum on graphene oxide/
: An efficient, magnetically separable catalyst for one-pot construction of spiro-oxindole dihydropyridines in deep eutectic solvent under microwave irradiation. Catal. Commun. 88, 39-44 (2017). - Chen, M.-N., Mo, L.-P., Cui, Z.-S. & Zhang, Z.-H. Magnetic nanocatalysts: Synthesis and application in multicomponent reactions. Curr. Opin. Green Sustain. Chem. 15, 27-37 (2019).
- Maleki, A. Synthesis of imidazo [1,2-a] pyridines using
@ as an efficient nanomagnetic catalyst via a one-pot multicomponent reaction. Helv. Chim. Acta 97, 587-593 (2014). - Baharfar, R., Peiman, S. & Maleki, B.
@ @ D-NHCS-Tr as an efficient and reusable catalyst for the synthesis of indol-3-yl-4 H-chromene via a multi-component reaction under solvent-free conditions. J. Heterocycl. Chem. 58, 1302-1310 (2021). - Peiman, S., Baharfar, R. & Hosseinzadeh, R. CuI NPs immobilized on a ternary hybrid system of magnetic nanosilica, PAMAM dendrimer and trypsin, as an efficient catalyst for
-coupling reaction. Res. Chem. Intermed. 48, 1365-1382 (2022). - Maleki, A., Rahimi, R. & Maleki, S. Efficient oxidation and epoxidation using a chromium (VI)-based magnetic nanocomposite. Environ. Chem. Lett. 14, 195-199 (2016).
- Suetsuna, T., Suenaga, S., Takahashi, T. & Harada, K. Synthesis of self-forming core/shell nanoparticles of magnetic metal/nonmagnetic oxide. Acta Mater. 78, 320-327 (2014).
- Zhao, F. et al. Synthesis of
-zeolite materials and application to the adsorption of gallium and indium. J. Chem. Eng. Data 60, 1338-1344 (2015). - Wang, Y.-M. et al. Molybdenum disulfide-catalyzed direct
-hydroxymethylation of amides employing methanol as a sustainable C1 source under photoirradiation. J. Catal. 427, 115100 (2023). - Naghizadeh, M., Taher, M. A., Tamaddon, A.-M., Borandeh, S. & Abolmaali, S. S. Microextraction of gadolinium MRI contrast agent using core-shell
@ SiO nanoparticles: Optimization of adsorption conditions and in-vitro study. Environ. Nanotechnol. Monit. Manag. 12, 100250 (2019). - Hasani, M. & Ghods, M. M-polynomials and topological indices of porphyrin-cored dendrimers. Chem. Methodol. 7, 288-306. https://doi.org/10.22034/chemm.2023.370497.1626 (2023).
- Bodaghifard, M. A., Allahbakhshi, H. & Ahangarani-Farahani, R. Efficient synthesis of benzoacridines and indenoquinolines catalyzed by acidic magnetic dendrimer. Sci. Rep. 14, 8736 (2024).
- Shailey Singhal, S. S., Shefali Arora, S. A., Shilpi Agarwal, S. A., Rajan Sharma, R. S. & Naveen Singhal, N. S. A review on potential biological activities of thiosemicarbazides. World J. Pharm. Pharm. Sci. 6, 4661 (2013).
- Arora, S., Agarwal, S. & Singhal, S. Anticancer activities of thiosemicarbazides/thiosemicarbazones: A review. Int. J. Pharm. Pharm. Sci. 6, 34 (2014).
- El-Atawy, M. A., Omar, A. Z., Hagar, M. & Shashira, E. M. Transalkylidation reaction: Green, catalyst-free synthesis of thiosemicarbazones and solving the NMR conflict between their acyclic structure and intramolecular cycloaddition products. Green Chem. Lett. Rev. 12, 364-376 (2019).
- Azizi, M., Maleki, A., Hakimpoor, F., Ghalavand, R. & Garavand, A. A mild, efficient and highly selective oxidation of sulfides to sulfoxides catalyzed by lewis acid-urea-hydrogen peroxide complex at room temperature. Catal. Lett. 147, 2173-2177 (2017).
- Alipour, A. & Naeimi, H. Design, fabrication and characterization of magnetic nickel copper ferrite nanocomposites and their application as a reusable nanocatalyst for sonochemical synthesis of 14-aryl-14-H-dibenzo [a, j] xanthene derivatives. Res. Chem. Intermed. 49, 2705-2723 (2023).
- Zare, A. & Mostaghar, F. Construction of a novel magnetic nanomaterial, and its utility as an effectual catalyst for the fabrication of 1, 8-dioxo-octahydroxanthenes. Chem. Methodol. 8, 23-36. https://doi.org/10.48309/chemm.2024.422175.1733 (2023).
- Azizi, N., Farzaneh, F. & Farhadi, E. Streamlining efficient and selective synthesis of benzoxanthenones and xanthenes with dual catalysts on a single support. Sci. Rep. 13, 16469 (2023).
- Ardeshirfard, H. & Elhamifar, D. Magnetic cobalt oxide supported organosilica-sulfonic acid as a powerful nanocatalyst for the synthesis of tetrahydrobenzo [a] xanthen-11-ones. Sci. Rep. 13, 14134 (2023).
- Mohammadi Ziarani, G. et al. Convenient one-pot synthesis of spirooxindole-4H-pyrans in the presence of SBA-Pr-NH2 and evaluation of their urease inhibitory activities. J. Nanostruct. 2, 489-500 (2012).
- Maghsoodlou, M. T., Heydari, R., Mohamadpour, F. & Lashkari, M.
as an environmentally benign natural catalyst for onepot and solvent-free synthesis of spiro-4H-pyran derivatives. Iran. J. Chem. Chem. Eng. IJCCE 36, 31-38 (2017). - Tufail, F. et al. A practical green approach to diversified spirochromene/spiropyran scaffolds via a glucose-water synergy driven organocatalytic system. New J. Chem. 42, 17279-17290 (2018).
- Nasri, S., Bayat, M. & Miankooshki, F. R. Synthesis of diverse spiro-imidazo pyridine-indene derivatives via acid-promoted annulation reaction of bindone and heterocyclic ketene aminals. Sci. Rep. 12, 12550 (2022).
- Naderi, S., Sandaroos, R., Peiman, S. & Maleki, B. Novel crowned cobalt (II) complex containing an ionic liquid: A green and efficient catalyst for the one-pot synthesis of chromene and xanthene derivatives starting from benzylic alcohols. J. Phys. Chem. Solids 180, 111459 (2023).
- Darvishy, S., Alinezhad, H., Vafaeezadeh, M., Peiman, S. & Maleki, B. S-(+) Camphorsulfonic acid glycine (CSAG) as surfactantlikes brønsted acidic ionic liquid for one-pot synthesis of
-amino carbonyl. Polycycl. Aromat. Compd. https://doi.org/10.1080/ 10406638.2022.2094419 (2022). - Sandaroos, R., Maleki, B., Naderi, S. & Peiman, S. Efficient synthesis of sulfones and sulfoxides from sulfides by cobalt-based Schiff complex supported on nanocellulose as catalyst and Oxone as the terminal oxidant. Inorg. Chem. Commun. 148, 110294 (2023).
- Boroumand, H., Alinezhad, H., Maleki, B. & Peiman, S. Triethylenetetramine-grafted magnetic graphene oxide (
) as a reusable heterogeneous catalyst for the one-pot synthesis of 2-amino-4 H-benzopyran derivatives. Polycycl. Aromat. Compd. 43, 7853-7869 (2023). - Maleki, B., Sandaroos, R., Naderi, S. & Peiman, S. A crowned manganese-based Schiff complex supported on nanocellulose as an efficient and sustainable heterogeneous catalyst for the oxidation of benzyl alcohols. J. Organometall. Chem. 990, 122666 (2023).
- Naderi, S., Sandaroos, R., Peiman, S. & Maleki, B. Synthesis and characterization of a novel crowned schiff base ligand linked to ionic liquid and application of its
complex in the epoxidation of olefins. Chem. Methodol. 7, 392-404 (2023). - Maleki, B., Sandaroos, R. & Peiman, S. Mn(III) Schiff base complexes containing crown ether rings immobilized onto MCM-41 matrix as heterogeneous catalysts for oxidation of alkenes. Heliyon 9, e15041 (2023).
- Maleki, B., Jamshidi, A., Peiman, S. & Housaindokht, M. R. Tri-vanadium substituted dawson-type heteropolytungstate nanocomposite (
) as a novel, green, and recyclable nanomagnetic catalyst in the synthesis of tetrahydrobenzo [b] pyrans. Polycycl. Aromat. Compd. 44, 994-1010 (2024). - Bhale, P. S., Dongare, S. B. & Mule, Y. B. An efficient synthesis of 1, 8-dioxooctahydroxanthenes catalysed by thiourea dioxide (TUD) in aqueous media. Chem. Sci. Trans. 4, 246-250 (2015).
- Gong, K., Fang, D., Wang, H.-L., Zhou, X.-L. & Liu, Z.-L. The one-pot synthesis of 14-alkyl-or aryl-14H-dibenzo [a, j] xanthenes catalyzed by task-specific ionic liquid. Dyes pigments 80, 30-33 (2009).
- Mir, E., Hazeri, N., Faroughi Niya, H. & Fatahpour, M. Synthesis, identification and application of
@ THAM-mercaptopyrimidine nanoparticles as a novel and highly recyclable nanocatalyst in one-pot multicomponent synthesis of 1, 8-dioxooctahydroxanthenes and polyhydroquinolines. Res. Chem. Intermed. 49, 1439-1462 (2023). - Kundu, K. & Nayak, S. K. Camphor-10-sulfonic acid catalyzed condensation of 2-naphthol with aromatic/aliphatic aldehydes to 14-aryl/alkyl-14H-dibenzo [a, j] xanthenes. J. Serb. Chem. Soc. 79, 1051-1058 (2014).
- Rekunge, D. S., Khatri, C. K. & Chaturbhuj, G. U. Rapid and efficient protocol for Willgerodt-Kindler’s thioacetamides catalyzed by sulfated polyborate. Mon. Chem. Chem. Mon. 148, 2091-2095 (2017).
- Mohammadi, R., Eidi, E., Ghavami, M. & Kassaee, M. Z. Chitosan synergistically enhanced by successive
and silver nanoparticles as a novel green catalyst in one-pot, three-component synthesis of tetrahydrobenzo xanthene-11-ones. J. Mol. Catal. A Chem. 393, 309-316 (2014). - Mane, P. et al. Sodium acetate/MWI: A green protocol for the synthesis of tetrahydrobenzo
xanthen-11-ones with biological screening. Res. Chem. Intermed. 46, 231-241 (2020). - Zhang, M. et al. Catalyst-free, visible-light promoted one-pot synthesis of spirooxindole-pyran derivatives in aqueous ethyl lactate. ACS Sustain. Chem. Eng. 5, 6175-6182 (2017).
- Langroudi, J. M., Mazloumi, M., Nahzomi, H. T., Shirini, F. & Tajik, H. Tropine-based dicationic molten salt: An active catalyst in the acceleration of one-pot synthesis of spiro- 2 -amino- 4 H -pyran-oxindoles and bis- 2 -amino- 4 H -pyrans. J. Mol. Struct. 1274, 134410 (2023).
- Guo, R.-Y. et al. Meglumine: A novel and efficient catalyst for one-pot, three-component combinatorial synthesis of functionalized 2-amino-4 H-pyrans. ACS Comb. Sci. 15, 557-563 (2013).
- Umar Basha, K. N. & Gnanamani, S. An efficient and easy method for the one-pot synthesis of spirooxindoles in the presence of
. J. Heterocycl. Chem. 56, 2008-2016 (2019). - Li, Y., Chen, H., Shi, C., Shi, D. & Ji, S. Efficient one-pot synthesis of spirooxindole derivatives catalyzed by l-proline in aqueous medium. J. Comb. Chem. 12, 231-237 (2010).
- Goli-Jolodar, O., Shirini, F. & Seddighi, M. Introduction of a novel basic ionic liquid containing dual basic functional groups for the efficient synthesis of spiro-4H-pyrans. J. Mol. Liq. 224, 1092-1101 (2016).
- Raheja, B. K. & Dalal, D. S. Ammonium acetate mediated simple, rapid, and one-pot multicomponent synthesis of spirooxindole derivatives. Synth. Commun. 53, 808-822 (2023).
- Chandam, D. R., Mulik, A. G., Patil, D. R. & Deshmukh, M. B. Oxalic acid dihydrate: Proline as a new recyclable designer solvent: A sustainable, green avenue for the synthesis of spirooxindole. Res. Chem. Intermed. 42, 1411-1423 (2016).
- Thongni, A. et al. Ultrasound assisted synthesis of spirooxindole analogs catalyzed by
@ PPCA NPs: Experimental, theoretical and in vitro biological studies. J. Mol. Struct. 1284, 135363 (2023). - Pan, F.-F., Yu, W., Qi, Z.-H., Qiao, C. & Wang, X.-W. Efficient construction of chiral spiro [benzo [g] chromene-oxindole] derivatives via organocatalytic asymmetric cascade cyclization. Synthesis 46, 1143-1156 (2014).
- Zhao, H. W. et al. Highly enantioselective synthesis of chiral pyranonaphthoquinone-fused spirooxindoles through organocatalytic three-component cascade reactions. Eur. J. Org. Chem. 2015, 3320-3326 (2015).
- Kumar, C. N. S. S. P., Srinivas, C., Sadhu, P. S., Rao, V. J. & Palaniappan, S. Efficient synthesis of 14-substituted-14-H-dibenzo [a, j] xanthenes using silica supported sodium hydrogen sulfate or amberlyst-15 catalyst. J. Heterocycl. Chem. 46, 997-999 (2009).
- Liu, Y.-H., Tao, X.-Y., Lei, L.-Q. & Zhang, Z.-H. Fluoroboric acid adsorbed on silica-gel-catalyzed synthesis of 14-aryl-14 H-dibenzo [
] xanthene derivatives. Synth. Commun. 39, 580-589 (2009). - Alireza, G. M. Z. N. L. Sulfonic acid-functionalized mesoporous silica. Gen 466, 116 (2013).
- Yue, X. et al. High acidity cellulose sulfuric acid from sulfur trioxide: A highly efficient catalyst for the one step synthesis of xanthene and dihydroquinazolinone derivatives. RSC Adv. 9, 28718-28723 (2019).
- Wu, L., Yang, C., Yang, L. & Yang, L. Synthesis of 14 -substituted-14 H-dibenzo [a, j] xanthenes and 1, 8-dioxo-octahydroxanthenes using silica chloride (
) under solvent-free conditions. Phosphorus Sulfur Silicon 185, 903-909 (2010). - Mohamadpour,
as an efficient and environmentally benign natural catalyst for facile and solvent-free synthesis of xanthene derivatives. J. Appl. Chem. Res. 13, 66-80 (2019). - Tayebee, R. & Tizabi, S. Highly efficient and environmentally friendly preparation of 14 -aryl-14H dibenzo [ a , j ] xanthenes catalyzed by tungsto-divanado-phosphoric acid. Chin. J. Catal. 33, 962-969 (2012).
- Nemati, R., Elhamifar, D., Zarnegaryan, A. & Shaker, M. Magnetic silica nanocomposite supported
amine: A powerful catalyst for the synthesis of biologically active spirooxindole-pyrans. Inorg. Chem. Commun. 145, 109934 (2022). - Amini Moqadam, Z., Allahresani, A. & Hassani, H. An efficiently and quickly synthesized NiO@g-C3
nanocomposite-catalyzed green synthesis of spirooxindole derivatives. Res. Chem. Intermed. 46, 299-311 (2020). - Karmakar, B., Nayak, A. & Banerji, J. A clean and expedient synthesis of spirooxindoles in aqueous media catalyzed over nanocrystalline MgO. Tetrahedron Lett. 53, 5004-5007 (2012).
- Hojati, S. F., Amiri, A. & Mahamed, M. Polystyrene@graphene oxide-
as a novel and magnetically recyclable nanocatalyst for the efficient multi-component synthesis of spiro indene derivatives. Res. Chem. Intermed. 46, 1091-1107 (2020). - Sadeghi, B., Ghasemi Pirbaluti, M., Farokhi Nezhad, P. & Abbasi Nezhad, R. A clean and expedient synthesis of spirooxindoles catalyzed by silica-sulfuric acid nanoparticles as an efficient and reusable reagent. Res. Chem. Intermed. 41, 4047-4055 (2015).
Acknowledgements
This study was supported by a research grant (Number 33/38554) from the University of Mazandaran.
Author contributions
Writing: S.P.; B.M. Conceptualization: S.P.; B.M. Data curation: S.P.; B.M. Formal analysis: S.P.; B.M. Project administration: S.P.; B.M. Methodology: S.P.; B.M. Validation: S.P.; B.M. Review and editing: S.P.; B.M. All authors reviewed the manuscript.
Competing interests
The authors declare no competing interests.
Additional information
Correspondence and requests for materials should be addressed to B.M.
Reprints and permissions information is available at www.nature.com/reprints.
Publisher’s note Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.
Reprints and permissions information is available at www.nature.com/reprints.
Publisher’s note Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.
Open Access This article is licensed under a Creative Commons Attribution-NonCommercialNoDerivatives 4.0 International License, which permits any non-commercial use, sharing, distribution and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons licence, and indicate if you modified the licensed material. You do not have permission under this licence to share adapted material derived from this article or parts of it. The images or other third party material in this article are included in the article’s Creative Commons licence, unless indicated otherwise in a credit line to the material. If material is not included in the article’s Creative Commons licence and your intended use is not permitted by statutory regulation or exceeds the permitted use, you will need to obtain permission directly from the copyright holder. To view a copy of this licence, visit http://creativecommons.org/licenses/by-nc-nd/4.0/.
© The Author(s) 2024
© The Author(s) 2024
- Department of Organic Chemistry, Faculty of Chemistry, University of Mazandaran, P.O. Box 47416-95447, Babolsar, Iran.
email: b.maleki@umz.ac.ir
