DOI: https://doi.org/10.1038/s41415-024-7405-9
PMID: https://pubmed.ncbi.nlm.nih.gov/38789758
تاريخ النشر: 2024-05-24
العلاج الجراحي لالتهاب المحيط بالزرع
النقاط الرئيسية
الملخص
مع استمرار استخدام زراعة الأسنان في الارتفاع، تزداد أيضًا حالات المضاعفات البيولوجية. عندما يتسبب التهاب المحيط بالزرع في فقدان كبير للعظام، يواجه طبيب الأسنان معضلة حول أي علاج هو الأنسب للحفاظ على الزرع. نظرًا لأن الأساليب غير الجراحية لالتهاب المحيط بالزرع أظهرت فعالية محدودة، تصف الورقة الحالية طرق العلاج الجراحي المختلفة، مع التأكيد على مؤشرات استخدامها وقيودها. الهدف الرئيسي في إدارة التهاب المحيط بالزرع هو تطهير سطح الزرع المصاب وإزالة جيوب المحيط العميقة. لهذا الغرض، أظهرت إزالة الأنسجة باستخدام شريحة الوصول، مع أو بدون إجراءات استئصالية، فعاليتها في عدد كبير من الحالات. ومع ذلك، قد تكون هذه العلاجات الجراحية مرتبطة بتراجع ما بعد الجراحة في حافة الغشاء المخاطي. بالإضافة إلى حل المرض، تسعى الأساليب الترميمية أيضًا إلى تجديد عيب العظام وتحقيق إعادة الاندماج العظمي.
مؤشرات الإدارة الجراحية لالتهاب المحيط بالزرع
a. إجراءات شريحة الوصول، ربما تكون مصحوبة بتقنيات استئصالية أو زراعة الزرع، و
b. إجراءات ترميمية تهدف إلى استعادة العظام المفقودة حول الزرع باستخدام بدائل العظام.
إزالة الأنسجة باستخدام شريحة الوصول بدون إجراءات استئصالية
تطهير سطح الزرع باستخدام طرق ميكانيكية وكيميائية، وربما طرق مساعدة أخرى مثل العلاج الضوئي الديناميكي أو العلاج بالليزر. ثم يتم إعادة وضع الشريحة وخياطتها في مكانها.
إزالة الأنسجة باستخدام شريحة الوصول مع إجراءات استئصالية
قيمت الدراسات المقارنة فعالية زراعة الزرع مقابل التطهير البديل باستخدام تلميع الهواء مع مسحوق الجلايسين.
مؤشرات وفعالية الأساليب الترميمية
- المريض مستعد للخضوع للتدخل والمشاركة بفعالية في برنامج رعاية داعمة مخصص حول الزرع
- توقعات واقعية من المريض
- درجات لويحات الفم الكاملة المنخفضة (<20%)
- درجات نزيف الفم الكاملة المنخفضة (<20%)
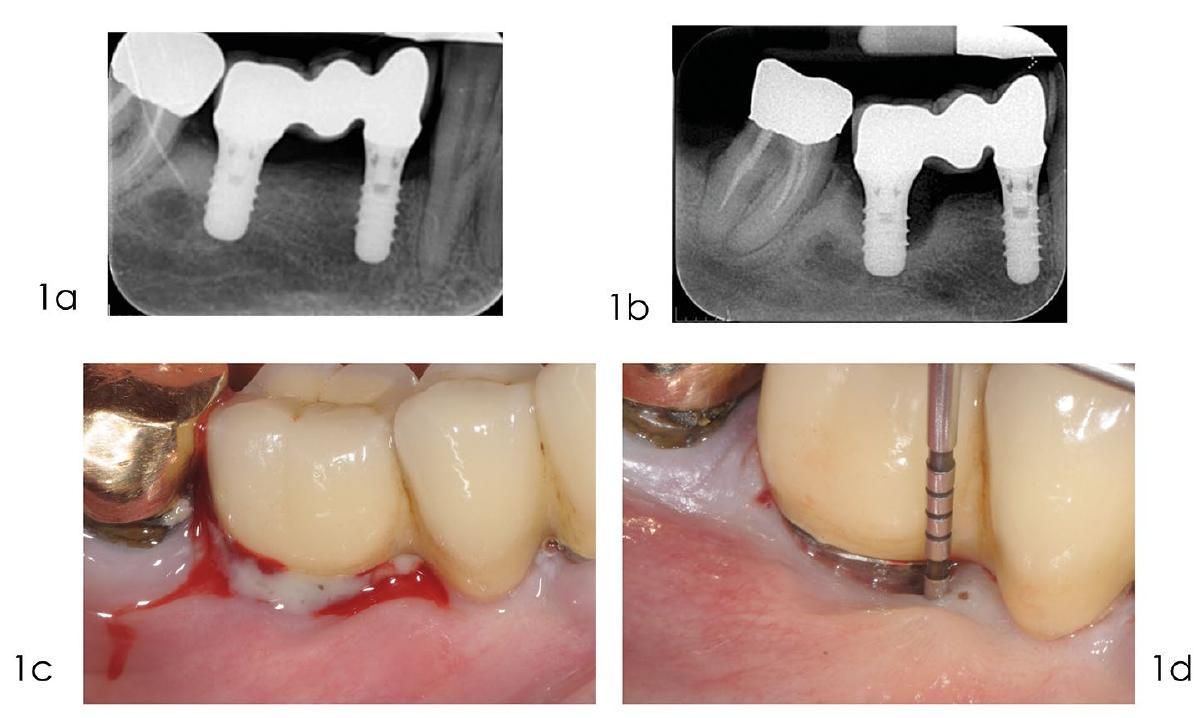
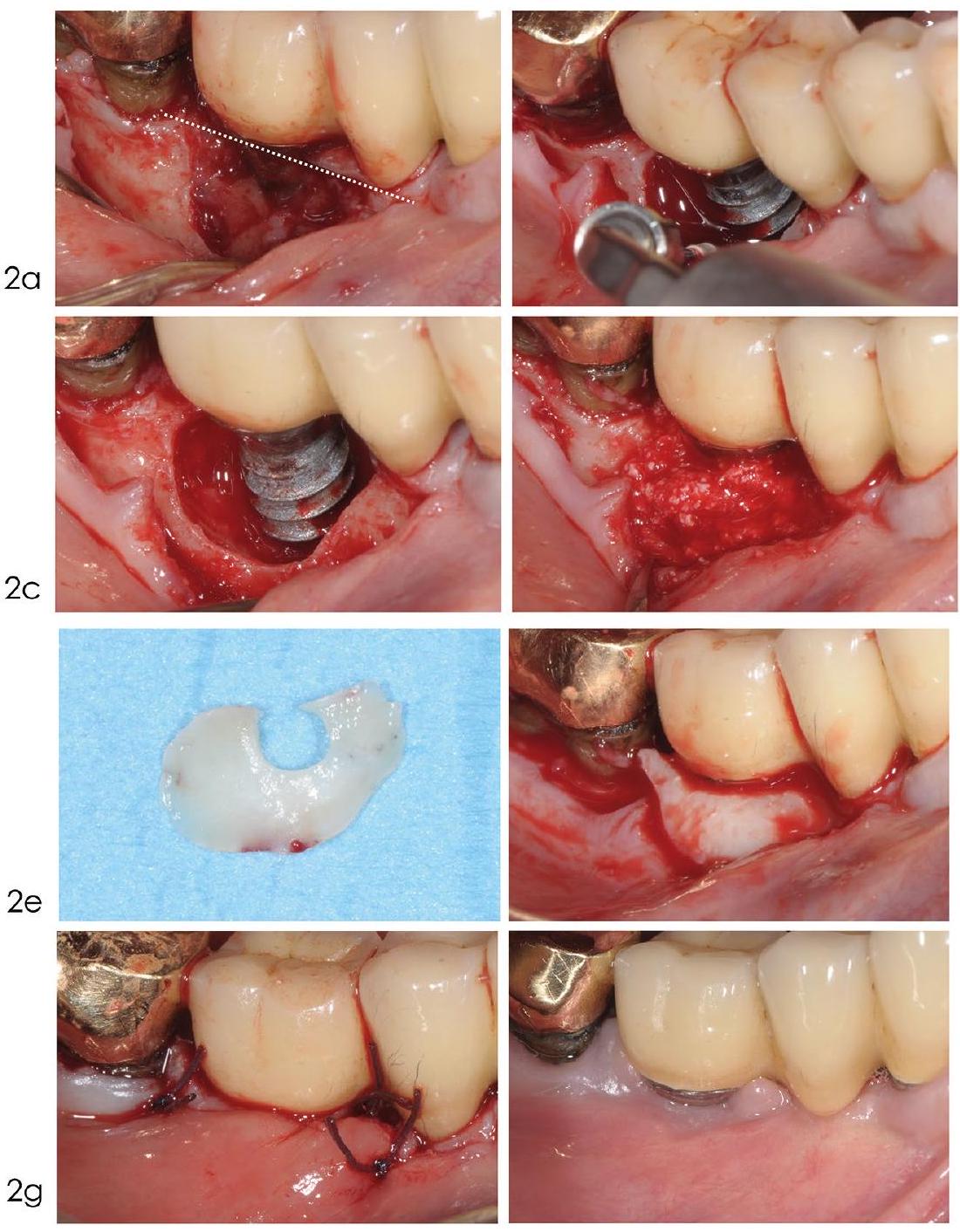
- التدخين <10 سجائر/يوم
- لا توجد موانع طبية للتدخل الجراحي/الترميمي.
- عمق العيب تحت العظمي
- تكوين العيب: من الناحية المثالية، عيب محصور بثلاث أو أربع جدران
- وجود شريط من الغشاء المخاطي الكيراتيني حول الزرع.
كان الهدف الرئيسي من ورشة العمل الأوروبية الثامنة عشرة حول علم اللثة هو تلخيص التوصيات المستندة إلى الأدلة للتدخلات الفردية المستخدمة في إدارة التهاب ما حول الزرع
الأمراض، استنادًا إلى أفضل الأدلة المتاحة و/أو توافق الخبراء. لعملية تطوير الإرشادات بشأن فعالية العلاجات الترميمية للعظام في إدارة عيوب التهاب ما حول الزرع، تم إجراء مراجعة منهجية بواسطة دونوس وزملائه.
- العيوب العميقة والضيقة أكثر ملاءمة لاستقرار الطعم وتكوين العظام الجديدة الناتجة
- يجب التخطيط لامتداد الطية الكاملة بعناية، مع موازنة الهدف لتقليل تدخّل الإجراء والحاجة للوصول إلى قاع العيب
- يجب اختيار المادة الحيوية التجديدية بناءً على التحقق العلمي المناسب وتطبيقها دون ملء العيب بشكل مفرط
- يجب إدخال الطعم فقط بعد القضاء التام على نسيج التكوين وتعقيم سطح الزرع
- في حالة عدم كفاية عرض الغشاء المخاطي الكيراتيني، يجب تقليم طعم النسيج الضام وتكييفه على كامل العيب بحيث يغطي
العظم المحيط بالسن لضمان استقرار مادة الطعم. إذا كان العيب دائريًا في منطقة لا تحتوي على مخاطية مكرمشة، يمكن قص طعم كبير من الأنسجة الضامة باستخدام شفرة دائرية، وتكييفه دائريًا حول العيب. - يجب توجيه المرضى حول كيفية حماية ورعاية والحفاظ على نظافة الجرح الجراحي
الموقع بحيث يفضل الشفاء الأولي للجراحة.
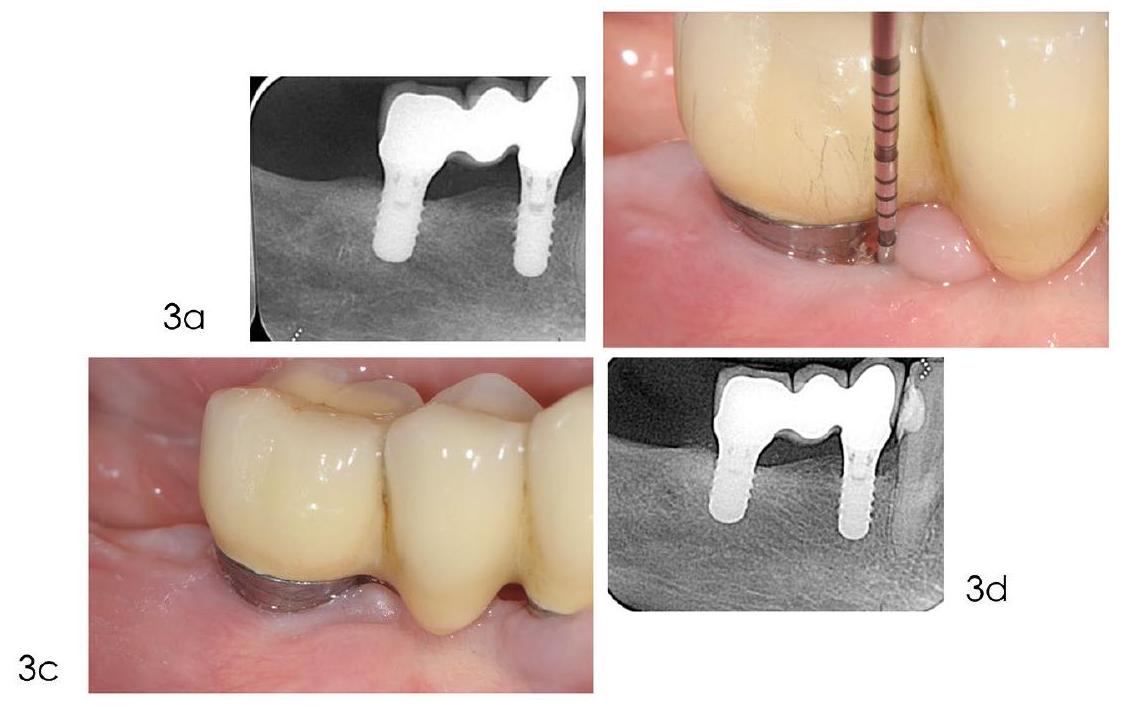

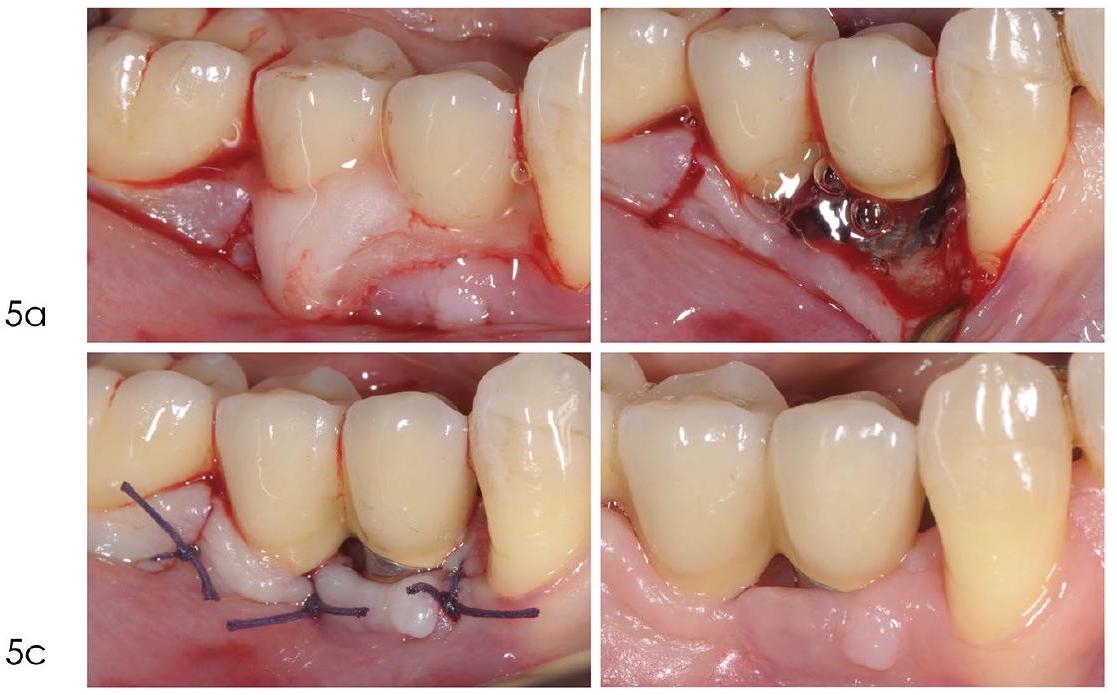

الاستنتاجات
خطوة من خطوات الرعاية، حيث تخلق ظروفًا أفضل حول الزرع قبل التدخل الجراحي.
لتسهيل الصيانة على المدى الطويل وللحفاظ على الجمالية.
إعلان الأخلاقيات
معلومات التمويل
مساهمات المؤلفين
References
- Salvi G E, Stähli A, Imber J C et al. Physiopathology of peri-implant diseases. Clin Implant Dent Relat Res 2023; 25: 629-639.
- Figuero E, Graziani F, Sanz I et al. Management of peri-implant mucositis and peri-implantitis. Periodontol 2000 2014; 66: 255-273.
- Roccuzzo A, Klossner S, Stähli A et al. Non-surgical mechanical therapy of peri-implantitis with or without repeated adjunctive diode laser application. A 6-month double-blinded randomized clinical trial. Clin Oral Implants Res 2022; 33: 900-912.
- Cosgarea R, Roccuzzo A, Jepsen K etal. Efficacy of mechanical/physical approaches for implant surface decontamination in non-surgical submarginal instrumentation of peri-implantitis. A systematic review. J Clin Periodontol 2023; 50: 188-211.
- Herrera D, Berglundh T, Schwarz F etal. Prevention and treatment of peri-implant diseases – The EFP S3 level clinical practice guideline. J Clin Periodontol 2023; 50: 4-76.
- Roccuzzo A, De Ry S P, Sculean A. Current Approaches for the Non-surgical Management of Peri-implant Diseases. Current Oral Health Reports 2020; 7: 274-282.
- Monje A, Amerio E, Cha J K etal. Strategies for implant surface decontamination in peri-implantitis therapy. Int J Oral Implantol 2022; 15: 213-248.
- Schlee M, Wang H L, Stumpf T et al. Treatment of Periimplantitis with Electrolytic Cleaning versus Mechanical and Electrolytic Cleaning: 18-Month Results from a Randomized Controlled Clinical Trial. J Clin Med 2021; 10: 3475.
- Roccuzzo A, Stähli A, Monje A, Sculean A, Salvi G E. Peri-Implantitis: A Clinical Update on Prevalence and Surgical Treatment Outcomes. J Clin Med 2021; 10: 1107.
- Ramanauskaite A, Cafferata E A, Begic A et al. Surgical interventions for the treatment of peri-implantitis. Clin Implant Dent Relat Res 2023; 25: 682-695.
- Schwarz F, Jepsen S, Obreja K et al. Surgical therapy of peri-implantitis. Periodontol 2000 2022; 88: 145-181.
- Heitz-Mayfield L J A, Salvi G E, Mombelli A etal. Supportive peri-implant therapy following anti-infective surgical peri-implantitis treatment: 5-year survival and success. Clin Oral Implants Res 2018; 29: 1-6.
- Carcuac 0 , Derks J, Abrahamsson I et al. Risk for recurrence of disease following surgical therapy of periimplantitis. A prospective longitudinal study. Clin Oral Implants Res 2020; 31: 1072-1077.
- Berglundh T, Wennström J L, Lindhe J. Long-term outcome of surgical treatment of peri-implantitis. A 2-11-year retrospective study. Clin Oral Implants Res 2018; 29: 404-410.
- Roccuzzo M, Pittoni D, Roccuzzo A etal. Surgical treatment of peri-implantitis intrabony lesions by means of deproteinized bovine bone mineral with 10% collagen: 7-year-results. Clin Oral Implants Res 2017; 28: 1577-1583.
- Roccuzzo M, Fierravanti L, Pittoni D etal. Implant survival after surgical treatment of peri-implantitis lesions by means of deproteinized bovine bone mineral with 10% collagen: 10-year results from a prospective study. Clin Oral Implants Res 2020; 31: 768-776.
- Lasserre J F, Brecx M C, Toma S. Implantoplasty Versus Glycine Air Abrasion for the Surgical Treatment of
18. Stavropoulos A, Bertl K, Eren Setal. Mechanical and biological complications after implantoplasty -A systematic review. Clin Oral Implants Res 2019; 30: 833-848.
19. Stavropoulos A, Bertl K, Isidor F et al. Implantoplasty and the risk of fracture of narrow implants with advanced bone loss: A laboratory study. Clin Oral Implants Res 2023; 34: 1038-1046.
20. Schwarz F, Alcoforado G, Guerrero A et al. Periimplantitis: Summary and consensus statements of group 3. The 6th EAO Consensus Conference 2021 Clin Oral Implants Res 2021; 32: 245-253.
21. Derks J, Ortiz-Vigón A, Guerrero A et al. Reconstructive surgical therapy of peri-implantitis: A multicenter randomized controlled clinical trial. Clin Oral Implants Res 2022; 33: 921-944.
22. Jepsen S, Schwarz F, Cordaro Letal. Regeneration of alveolar ridge defects. Consensus report of group 4 of the 15th European Workshop on Periodontology on Bone Regeneration. J Clin Periodontol 2019; 46: 277-286.
23. Donos N, Calciolari E, Ghuman M etal. The efficacy of bone reconstructive therapies in the management of peri-implantitis. A systematic review and metaanalysis. J Clin Periodontol 2023; 50: 285-316.
24. Roccuzzo M, Bonino F, Bonino Let al. Surgical therapy of peri-implantitis lesions by means of a bovine- derived xeno-graft: Comparative results of a prospective study on two different implant surfaces. J Clin Periodontol 2011; 38: 738-745.
25. Roccuzzo M, Gaudioso L, Lungo M et al. Surgical therapy of single peri-implantitis intrabony defects, by means of depro- teinized bovine bone mineral with 10% collagen. J Clin Periodontol 2016; 43: 311-318.
26. Rotenberg S A, Steiner R, Tatakis D N. Collagen-Coated Bovine Bone in Peri-implantitis Defects: A Pilot Study on a Novel Approach. Int J Oral Maxillofac Implants 2016; 31: 701-707.
27. Mercado F, Hamlet S, Ivanovski S. Regenerative surgical therapy for peri-implantitis using deproteinized bovine bone mineral with 10% collagen, enamel matrix derivative and Doxycycline-A prospective 3 -year cohort study. Clin Oral Implants Res 2018; 29: 583-591.
28. Ichioka Y, Trullenque-Eriksson A, Ortiz-Vigón A etal. Factors influencing outcomes of surgical therapy of periimplantitis: A secondary analysis of 1-year results from a randomized clinical study. J Clin Periodontol 2023; 50: 1282-1304.
29. Roos-Jansåker A M, Persson G R, Lindahl C et al. Surgical treatment of peri-implantitis using a bone substitute with or without a resorbable membrane: a 5-year follow-up. J Clin Periodontol 2014; 41: 1108-1114.
30. Monje A, Pons R, Vilarrasa J et al. Significance of barrier membrane on the reconstructive therapy of periimplantitis: A randomized controlled trial.J Periodontol 2023; 94: 323-335.
31. Roccuzzo M, Mirra D, Pittoni D etal. Reconstructive treatment of peri-implantitis infrabony defects of various configurations: 5-year survival and success. Clin Oral Implants Res 2021; 32: 1209-1217.
Private Practice, Torino, Italy; Division of Maxillofacial Surgery, University of Torino, Italy; ³Department of Periodontics and Oral Medicine, University of Michigan, Ann Arbor, Michigan, USA; Department of Periodontology, School of Dental Medicine, University of Bern, Bern, Switzerland; Department of Oral and Maxillofacial Surgery, Copenhagen University Hospital (Rigshospitalet), Copenhagen, Denmark.
*Correspondence to: Andrea Roccuzzo
Email address: andrea.roccuzzo@unibe.ch
Refereed Paper.
Submitted 13 February 2024
Revised 22 April 2024
Accepted 22 April 2024
https://doi.org/10.1038/s41415-024-7405-9
DOI: https://doi.org/10.1038/s41415-024-7405-9
PMID: https://pubmed.ncbi.nlm.nih.gov/38789758
Publication Date: 2024-05-24
Surgical treatment of peri-implantitis
Key points
Abstract
As utilisation of dental implants continues to rise, so does the incidence of biological complications. When periimplantitis has already caused extensive bone resorption, the dentist faces the dilemma of which therapy is the most appropriate to maintain the implant. Since non-surgical approaches of peri-implantitis have shown limited effectiveness, the present paper describes different surgical treatment modalities, underlining their indications and limitations. The primary goal in the management of peri-implantitis is to decontaminate the surface of the infected implant and to eliminate deep peri-implant pockets. For this purpose, access flap debridement, with or without resective procedures, has shown to be effective in a large number of cases. These surgical treatments, however, may be linked to post-operative recession of the mucosal margin. In addition to disease resolution, reconstructive approaches also seek to regenerate the bone defect and to achieve re-osseointegration.
Indications for surgical management of peri-implantitis
a. Access flap procedures, possibly combined with resective techniques or implantoplasty, and
b. Reconstructive procedures aimed at restoring lost peri-implant bone using bone substitutes.
Access flap debridement without resective procedures
is decontaminated using mechanical, chemical, and potentially other adjunctive methods such as photodynamic therapy or laser treatment. The flap is then repositioned and sutured in place.
Access flap debridement with resective procedures
Comparative studies have evaluated the efficacy of implantoplasty against alternative decontamination with air-polishing with glycine powder.
Indications and efficacy of reconstructive approaches
- Patient willing to undergo the intervention and effectively participate in a tailored supportive care peri-implant programme
- Realistic patient expectations
- Low full-mouth plaque scores (<20%)
- Low full-mouth bleeding scores (<20%)


- Smoking<10 cigarettes/day
- No medical contraindications for surgical/ reconstructive intervention.
- The depth of the intrabony defect
- The defect configuration: ideally, an isolated three- or four-wall-contained defect
- Presence of a band of peri-implant keratinised mucosa.
The main objective of the XVIII European Workshop on Periodontology was to summarise the evidence-based recommendations for individual interventions used in the management of peri-implant
diseases, based on the best available evidence and/or expert consensus. For the guideline development process on the efficacy of bone reconstructive therapies in the management of peri-implantitis defects, a systematic review was conducted by Donos and co-workers.
- Deep and narrow defects are more favourable for the stabilisation of the graft and the consequent formation of new bone
- The extension of the full-thickness flap should be planned carefully, balancing the aim to minimise the invasiveness of the procedure and the need to have access to the bottom of the defect
- The regenerative biomaterial should be selected on the basis of proper scientific validation and applied without overfilling the defect
- The graft should be inserted only after complete elimination of the granulation tissue and the decontamination of the implant surface
- In case of insufficient keratinised mucosa width, a connective tissue graft should be trimmed and adapted over the entire defect so as to cover
of the surrounding alveolar bone to ensure stability of the graft material. Should the defect be circumferential in an area with no keratinised mucosa, a large connective tissue graft could be punched, by means of a circular blade, and adapted circumferentially around the defect - Patients should be instructed on how to protect, care for, and keep clean the surgical
site so as to favour primary healing of the surgical wound.




Conclusions
step of care, as it creates better peri-implant conditions before surgical intervention.
to facilitate the long-term maintenance and to preserve aesthetics.
Ethics declaration
Funding information
Author contributions
References
- Salvi G E, Stähli A, Imber J C et al. Physiopathology of peri-implant diseases. Clin Implant Dent Relat Res 2023; 25: 629-639.
- Figuero E, Graziani F, Sanz I et al. Management of peri-implant mucositis and peri-implantitis. Periodontol 2000 2014; 66: 255-273.
- Roccuzzo A, Klossner S, Stähli A et al. Non-surgical mechanical therapy of peri-implantitis with or without repeated adjunctive diode laser application. A 6-month double-blinded randomized clinical trial. Clin Oral Implants Res 2022; 33: 900-912.
- Cosgarea R, Roccuzzo A, Jepsen K etal. Efficacy of mechanical/physical approaches for implant surface decontamination in non-surgical submarginal instrumentation of peri-implantitis. A systematic review. J Clin Periodontol 2023; 50: 188-211.
- Herrera D, Berglundh T, Schwarz F etal. Prevention and treatment of peri-implant diseases – The EFP S3 level clinical practice guideline. J Clin Periodontol 2023; 50: 4-76.
- Roccuzzo A, De Ry S P, Sculean A. Current Approaches for the Non-surgical Management of Peri-implant Diseases. Current Oral Health Reports 2020; 7: 274-282.
- Monje A, Amerio E, Cha J K etal. Strategies for implant surface decontamination in peri-implantitis therapy. Int J Oral Implantol 2022; 15: 213-248.
- Schlee M, Wang H L, Stumpf T et al. Treatment of Periimplantitis with Electrolytic Cleaning versus Mechanical and Electrolytic Cleaning: 18-Month Results from a Randomized Controlled Clinical Trial. J Clin Med 2021; 10: 3475.
- Roccuzzo A, Stähli A, Monje A, Sculean A, Salvi G E. Peri-Implantitis: A Clinical Update on Prevalence and Surgical Treatment Outcomes. J Clin Med 2021; 10: 1107.
- Ramanauskaite A, Cafferata E A, Begic A et al. Surgical interventions for the treatment of peri-implantitis. Clin Implant Dent Relat Res 2023; 25: 682-695.
- Schwarz F, Jepsen S, Obreja K et al. Surgical therapy of peri-implantitis. Periodontol 2000 2022; 88: 145-181.
- Heitz-Mayfield L J A, Salvi G E, Mombelli A etal. Supportive peri-implant therapy following anti-infective surgical peri-implantitis treatment: 5-year survival and success. Clin Oral Implants Res 2018; 29: 1-6.
- Carcuac 0 , Derks J, Abrahamsson I et al. Risk for recurrence of disease following surgical therapy of periimplantitis. A prospective longitudinal study. Clin Oral Implants Res 2020; 31: 1072-1077.
- Berglundh T, Wennström J L, Lindhe J. Long-term outcome of surgical treatment of peri-implantitis. A 2-11-year retrospective study. Clin Oral Implants Res 2018; 29: 404-410.
- Roccuzzo M, Pittoni D, Roccuzzo A etal. Surgical treatment of peri-implantitis intrabony lesions by means of deproteinized bovine bone mineral with 10% collagen: 7-year-results. Clin Oral Implants Res 2017; 28: 1577-1583.
- Roccuzzo M, Fierravanti L, Pittoni D etal. Implant survival after surgical treatment of peri-implantitis lesions by means of deproteinized bovine bone mineral with 10% collagen: 10-year results from a prospective study. Clin Oral Implants Res 2020; 31: 768-776.
- Lasserre J F, Brecx M C, Toma S. Implantoplasty Versus Glycine Air Abrasion for the Surgical Treatment of
18. Stavropoulos A, Bertl K, Eren Setal. Mechanical and biological complications after implantoplasty -A systematic review. Clin Oral Implants Res 2019; 30: 833-848.
19. Stavropoulos A, Bertl K, Isidor F et al. Implantoplasty and the risk of fracture of narrow implants with advanced bone loss: A laboratory study. Clin Oral Implants Res 2023; 34: 1038-1046.
20. Schwarz F, Alcoforado G, Guerrero A et al. Periimplantitis: Summary and consensus statements of group 3. The 6th EAO Consensus Conference 2021 Clin Oral Implants Res 2021; 32: 245-253.
21. Derks J, Ortiz-Vigón A, Guerrero A et al. Reconstructive surgical therapy of peri-implantitis: A multicenter randomized controlled clinical trial. Clin Oral Implants Res 2022; 33: 921-944.
22. Jepsen S, Schwarz F, Cordaro Letal. Regeneration of alveolar ridge defects. Consensus report of group 4 of the 15th European Workshop on Periodontology on Bone Regeneration. J Clin Periodontol 2019; 46: 277-286.
23. Donos N, Calciolari E, Ghuman M etal. The efficacy of bone reconstructive therapies in the management of peri-implantitis. A systematic review and metaanalysis. J Clin Periodontol 2023; 50: 285-316.
24. Roccuzzo M, Bonino F, Bonino Let al. Surgical therapy of peri-implantitis lesions by means of a bovine- derived xeno-graft: Comparative results of a prospective study on two different implant surfaces. J Clin Periodontol 2011; 38: 738-745.
25. Roccuzzo M, Gaudioso L, Lungo M et al. Surgical therapy of single peri-implantitis intrabony defects, by means of depro- teinized bovine bone mineral with 10% collagen. J Clin Periodontol 2016; 43: 311-318.
26. Rotenberg S A, Steiner R, Tatakis D N. Collagen-Coated Bovine Bone in Peri-implantitis Defects: A Pilot Study on a Novel Approach. Int J Oral Maxillofac Implants 2016; 31: 701-707.
27. Mercado F, Hamlet S, Ivanovski S. Regenerative surgical therapy for peri-implantitis using deproteinized bovine bone mineral with 10% collagen, enamel matrix derivative and Doxycycline-A prospective 3 -year cohort study. Clin Oral Implants Res 2018; 29: 583-591.
28. Ichioka Y, Trullenque-Eriksson A, Ortiz-Vigón A etal. Factors influencing outcomes of surgical therapy of periimplantitis: A secondary analysis of 1-year results from a randomized clinical study. J Clin Periodontol 2023; 50: 1282-1304.
29. Roos-Jansåker A M, Persson G R, Lindahl C et al. Surgical treatment of peri-implantitis using a bone substitute with or without a resorbable membrane: a 5-year follow-up. J Clin Periodontol 2014; 41: 1108-1114.
30. Monje A, Pons R, Vilarrasa J et al. Significance of barrier membrane on the reconstructive therapy of periimplantitis: A randomized controlled trial.J Periodontol 2023; 94: 323-335.
31. Roccuzzo M, Mirra D, Pittoni D etal. Reconstructive treatment of peri-implantitis infrabony defects of various configurations: 5-year survival and success. Clin Oral Implants Res 2021; 32: 1209-1217.
Private Practice, Torino, Italy; Division of Maxillofacial Surgery, University of Torino, Italy; ³Department of Periodontics and Oral Medicine, University of Michigan, Ann Arbor, Michigan, USA; Department of Periodontology, School of Dental Medicine, University of Bern, Bern, Switzerland; Department of Oral and Maxillofacial Surgery, Copenhagen University Hospital (Rigshospitalet), Copenhagen, Denmark.
*Correspondence to: Andrea Roccuzzo
Email address: andrea.roccuzzo@unibe.ch
Refereed Paper.
Submitted 13 February 2024
Revised 22 April 2024
Accepted 22 April 2024
https://doi.org/10.1038/s41415-024-7405-9
